염화나트륨 특성//염화나트륨은 당신에게 좋은가요?
제목
나트륨 염화물이온성 화합물의 화학식 NaCl. 그것은 무색 입방 결정 또는 미세 결정 성 분말이며 짠 맛이납니다.
외관은 백색 결정이고,그것의 근원은 주로 식탁 용 소금의 주요 성분 인 바닷물이다. 물,글리세린,에탄올(알코올),액체 암모니아에 약간 용해,농축 염산에 불용성. 불순한 염화나트륨은 공기 중에 조해성이 있습니다.
안정성은 비교적 양호하며 수용액은 중성이다. 산업으로,메서드의 전해질으로 포화 나트륨 염화 솔루션을 사용하여 일반적으로 수소를 생성하,염소와 가성소다(수산화 나트륨)기타 화학제품(일반적으로 불리는 chlor 알칼리 업계).
에서 사용할 수 있습 oresmelting(전해 녹는 나트륨 염화물 결정을 생산하는 activemetal 나트륨),의학을 구성하는 데 사용되는 생리 식염수,그리고 매일 lifecan 위해 사용될 예약하십시오.
화합물을 소개
기본적인 정보
영어 이름:염화나트륨
영어 별칭:나트륨 염;Sodiumchloride
CAS 번호:7647-14-5
분자식:NaCl
분자량:58.44280
정확한 질량: 57.95860
정보 보안
통관 코드:2501002000
위험 카테고리 코드:R36;R22
안전 지침:S24/25-S26
위험한 상품명:시
의 물리적 특성 염화나트륨
외관과 속성:무색의 크리스탈 orwhite 분말
Density:2.165g/cm3(25°C)
물 가용성:360g/L(25ºC)
안정성:정상적인 선박 및 취급 조건 하에서 안정되어 있는.
보관 조건:저온,통풍 anddry 창고에 있
증기압:1mm Hg(865°C)
녹는 점:801°C
끓는점:1465℃
나트륨 염화물은 백색 무취의 크리스탈 분말입니다. Mp801℃.]C,1465℃의 끓는점.]C,에탄올,프로판올,부탄,부탄에 약간 용해되고,플라즈마가 물,35.9g(실온)의 물 용해도,혼합 될 후.
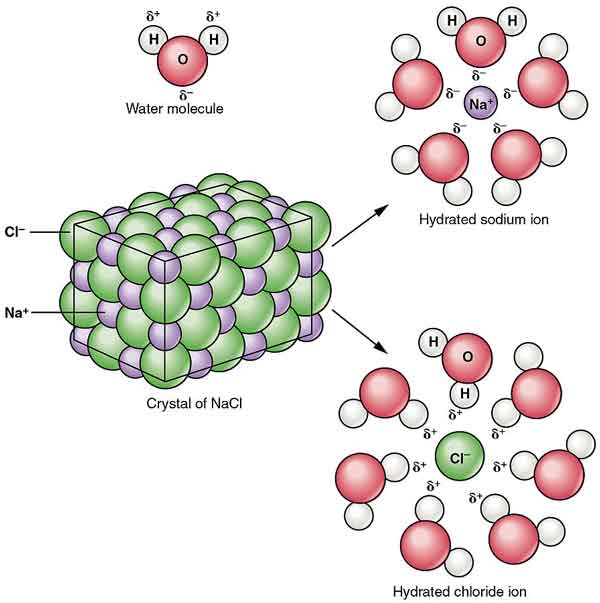
NaCl 분산에서 알코올을 형성 colloids. 물에서의 용해도는 염화수소의 존재에 의해 감소되며,농축 염산에는 거의 불용성이다.
염화나트륨의 화학적 성질
염화나트륨의 결정은 스테레오 대칭을 형성합니다. 결정 구조,큰 염화물 이온 양식 densest 에서 포장,큐브는 작은 나트륨이온을 채우 팔면체 사이의 간격은 염화물 이온입니다. Each ion is surrounded by six other ions. This structure is also found in many other compounds, called sodium chloride type structure or stone salt structure.

1. Preparationof sodium metal by electrolytic melting of sodium chloride
2NaCl(molten) = 2Na + Cl2
2. Electrolytic saltwater
2NaCl + 2H2O = H2 + Cl2 + 2NaOH
3. React withsilver nitrate
NaCl + AgNO3 = NaNO3 + AgCl
Ionic equation:
Cl– + Ag+ = AgCl
(Which is theessence CI – property)
4. Reaction withconcentrated sulfuric acid (laboratory hydrogen chloride)
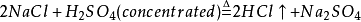

( Concentrated behalfconcentrated, Excess Representative excess)
5.NaCl test
A: 염화물은 질산의 용액에 산성화 된 질산은을 첨가하고,백색 침전물(침전 된 염화은)이 생성되어 ci-를 입증 하였다.
B:백금 와이어로 소량의 용액을 담그고 알코올 램프에 넣어 태우십시오. 화염은 노란색이며 Na+가 포함되어 있음을 입증 할 수 있습니다.
C:간섭을 제거하기 위해 원래의 시험 용액은 분명히 알칼리성 일 때까지 포화 된 수산화 바륨으로 첨가 할 수 있습니다. 이때,PO43−및 AsO43−와 같은 대부분의 양이온 및 음이온이 침전 될 것이다.
시험 용액에 도입 된 Ba2+는 탄산 암모늄에 의해 제거되어야하며,마지막으로 암모늄염은 연소에 의해 제거되어야한다. 후에는 잔류물 침출되었으로 물,해결책은 산성화된 학과 uranyl 아연 아세테이트 시약에 따라 추가 수울의 1:8,튜브 벽으로 문질러 유리는 막대입니다. 레몬-황색 결정이 형성되면 Na+가 존재했다.
염화나트륨의 제조
산업 방법
바닷물에 의해 염장으로 도입(평균 2.4%염화나트륨)및 햇볕에 건조시켜 결정화시켜 조 생성물을 얻는다. 바닷물을 수도 있습에 의해 가열 증기,필터링하여 모래 여과기,그리고 집중하여 이온교환 멤브레인기 투석을 얻는 소금물(염화 나트륨을 포함하는 160-180g/L).
후광 석고는 증발에 의해 침전되고,얻어진 염소는 원심 분리된다. 95%이상의 나트륨(2%수분)을 건조시켜 얻을 수 있습니다.일반적인 소금. 암염과 소금 호수 소금물은 또한 원료로 사용될 수 있습니다.재료 및 원시 소금을 얻기 위해 햇볕에 건조.
경우 지하물하고 잘 소금으로 사용되는 원자재,그들은 areconcentrated 에 의해 또는 효과 증발,크리스탈 침전시키고,원심 분리하여 얻을 수 있습니다.
험 방법
원금에 녹여 물을 제거하는 불용성,불순물을하고 세련된 준비과 같은 수산화나트륨 및 탄산나트륨은 추가 할 수용성 불순물 등과 같은 SO42-,Ca2+고 Mg2+가 침전물,필터링하여 제거하고,마지막 순화와 pH 조절하였 7 염산 및 솔루션 집중을 획득 순수 염화 나트륨을 결정합니다.
준비실험실의 방법은 동일한 양의 염산과 수산화 나트륨을 혼합하여 염화나트륨 용액을 형성하는 것입니다. 용액은염화나트륨 결정을 얻기 위해 고안되었다. 주요 반응:
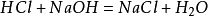
또한,염화나트륨 또한 생산 나트륨 염화면 점화에서 환경의 염소가스입니다. 화학 방정식입니다:
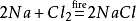
은 무엇인 염화나트륨용
산업
1. 전해 염화나트륨 용액이전자화되면 수소 및 염소 가스가 생성됩니다. 염소 가스는 awide 응용 프로그램의 범위를 화학 산업에서 사용할 수 있습 tosynthesize 폴리비닐화 염화물,살충제,염산,etc.2. Dangs 방법에 의한 나트륨 금속의 제조:sodiumchloride 와 calcium chloride 의 혼합물을 전기 분해하여 나트륨 금속의 제조. 염화칼슘은 700℃이하의 염화나트륨의 융점을 낮추는 플럭스로 사용됩니다.칼슘은 나트륨보다 덜 유도하며 불순물을 도입하지 않습니다.4. 무기 및 유기농업으로 사용되는 원료의 생산에 대한 부식성 소다,염소산염,차아염소산염,표백제,냉매에 대한 냉각 시스템,원재료에 대한 유기 합성과 염장 밖으로 에이전트. 철강 산업은 열처리제로 사용됩니다. 고온 열원은 염화칼륨,염화 바륨 등으로 소금 욕을 형성하는 데 사용됩니다. 할 수 있는 사용으로 난방 중간 온도를 유지하기 위해 사 820-960°C. 외에도,그것은 또한에서 사용되는 유리,염료,금속 및 다른 산업에 있습니다.6. 소다회 생산에 의해 허우의 알칼리법:두 번째 단계:중탄산 암모늄 솔루션이 준비하는 첫 번째 단계 ismixed 와 염화나트륨 용액을 얻을 중탄산나트륨 andammonium 염화에서 10°C
식품 산업
식품 산업 및 수산은소금뿐만 아니라 조미료 및 정제 된 식탁 용 소금의 원료.
요리 요리에 소금을 첨가하면 원재료의 일부 냄새를 제거하고 맛을 높일 수 있으며 이는 소금의 효과입니다. “약간 맛이없고 짠맛이없고 맛이 없다”는 의미입니다.적절한 양의 소금을 사용하여 고유 한 기능을 발휘할 수 있습니다.
의료
염화나트륨은 생명에 매우 중요합니다. 대부분의 생물학적 조직에는 여러 개의 염이 포함되어 있습니다. 혈중 나트륨의 농도는 규제와 직접 관련이 있습니다.안전한 수준의 체액. 에 의해 유발 된 신경 자극의 전도신경 변환은 또한 나트륨 이온에 의해 조절됩니다.
0.9%염화나트륨을 함유 한 물 염분이라고합니다.혈장과 동일한 삼투압을 가지기 때문입니다. 정상적인 식염수는체액 대체물. 그것은에서 널리 이용되는 치료 및 preventionof 탈수,그리고 그것은 또한 치료에 사용되는 정맥 injectionand 예방의 저 혈량 충격입니다.
다른 영장류와 달리 인간은 땀을 통해 많은 양의 염화나트륨을 분비합니다.
염화나트륨은인간. 성인에 함유 된 나트륨 이온의 총량은 약 60g 이며,80%는 세포 외액,즉 혈장 및 세포 간 유체에 있습니다. 염화물은 또한 주로 세포 외액에 존재합니다. 나트륨 및 염화물 이온의 생리 학적 기능은 다음과 같습니다:
(1)세포 외액의 삼투압을 유지합니다.
(2)신체의 산-염기 균형 조절에 참여하십시오.염화물은 체내의 위산 생성에 관여합니다. 또한,염화나트륨은 또한신경 및 근육의 정상적인 흥분성을 유지합니다.
농업
그것의 수용액은 seedselection 를 위해 이용될 수 있습니다. NaCl 용액은종류의 필요에 따라 구성되며 밀도는 물보다 큽니다. 씨앗은아클 용액,전체 부동 및 전체 침몰.
기타
에 따라 새로운 연구 결과에 의해 발표 SingaporeScience 및 기술 연구소,나트륨 염화할 수 있습 significantlyincrease 용량의 하드 드라이브입니다. 특히,존재전기적인하드 디스크는 무작위로 할당 된 자기 디스크 저장 기술을 사용하여 평방 인치당 0.5TB 의 데이터 밀도 만 달성 할 수 있습니다.
신기술은 sodiumchloride 의 도움으로 이익을 얻습니다. 새로운 고해상도 리소그래피 팩터 기술을 사용하면 데이터 밀도가 더 정돈되어 3 에 도달하게됩니다.필요없이 평방 인치 당 3 테라바이트복잡한 장비 업그레이드. 이와 함께 1TB 하드 디스크 사용기술은 디스크를 추가하지 않고도 6tb 용량에 도달 할 수 있습니다.
- 암모니아 공식||왜 암모니아는 독성||암모니아 중독
- 왜 오존층은 중요한||오존층이 고갈
- 농도가 무엇인지의 솔루션||는 방법은 농도 영향을 미치는 반응
- 왜 탄소 주기가 중요||그것이 작동하는 방법
- Haloalkanes 및 Haloarenes NCERT 솔루션||Haloalkane 구조
- 이산화탄소기 및 포뮬러||는 방법 이산화탄소 생성
Leave a Reply