Propiedades del cloruro de sodio / / ¿El cloruro de sodio es bueno para usted?
Temas del artículo
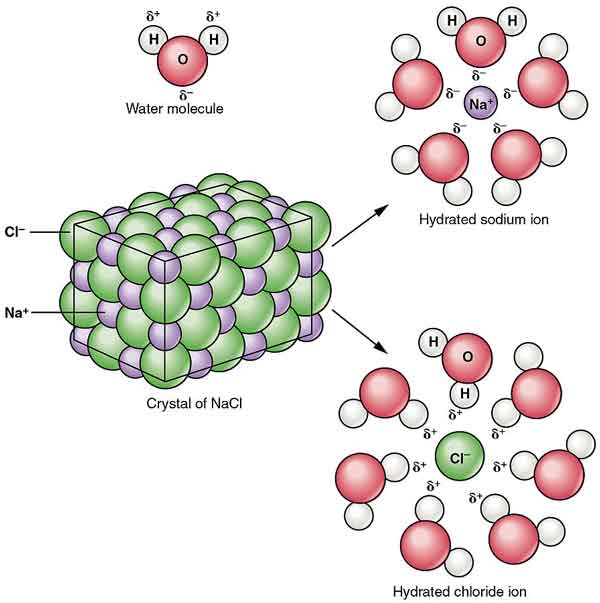
El cloruro de sodio es un compuesto iónico con la fórmula química NaCl. Es un cristal cúbico incoloro o polvo cristalino fino y tiene un sabor salado.
La apariencia es un cristal blanco, y su fuente es principalmente agua de mar, que es el componente principal de la sal de mesa. Soluble en agua, glicerina, ligeramente soluble en etanol (alcohol), amoníaco líquido, insoluble en ácido clorhídrico concentrado. El cloruro de sodio impuro es delicuescente en el aire.
La estabilidad es relativamente buena, y su solución acuosa es neutra. Industrialmente, el método de solución de cloruro de sodio electrolíticamente saturada se usa generalmente para producir hidrógeno, cloro y sosa cáustica (hidróxido de sodio) y otros productos químicos (comúnmente llamados industria cloroalcalina).
Se puede usar en la fusión de minerales (fusión electrolítica de cristales de cloruro de sodio para producir sodio activometal), se usa médicamente para configurar la solución salina fisiológica y se puede usar para condimentos de vida diaria.
Introducción del compuesto
Información básica
Nombre en inglés: cloruro de sodio
Alias en inglés: clorhidrato de sodio; Cloruro de sodio
Número CAS: 7647-14-5
Fórmula molecular: NaCl
Peso molecular: 58.44280
Masa exacta: 57.95860
Información de seguridad
Código de aduanas: 2501002000
Código de categoría de peligro: R36; R22
Instrucciones de seguridad: S24 / 25-S26
Signo de mercancías peligrosas: Xi
Propiedades físicas del cloruro de sodio
Apariencia y propiedades: cristal incoloro o polvo blanco
Densidad: 2.165 g / cm3 (25 ° C)
Solubilidad en agua: 360 g / L (25 ºC)
Estabilidad: Estable en condiciones normales de envío y manipulación.
Condiciones de almacenamiento: baja temperatura, ventilación y secado en almacén
Presión de vapor: 1 mm Hg (865 ° C)
Punto de fusión: 801 ° C
Punto de ebullición: 1465 ℃
El cloruro de sodio es un polvo cristalino inodoro blanco. Mp 801 grados] C, un punto de ebullición de 1465 grados.] C, ligeramente soluble en etanol, propanol, butano, butano, y después de que el plasma se vuelve miscible, soluble en agua, la solubilidad en agua de 35,9 g (temperatura ambiente).
NaCl se dispersa en alcohol para formar coloides. Su solubilidad en agua se reduce por la presencia de cloruro de hidrógeno, y es casi insoluble en ácido clorhídrico concentrado.
Propiedades químicas del cloruro de sodio
Los cristales de cloruro de sodio forman simetría estéreo. En su estructura cristalina, los iones de cloruro más grandes forman el embalaje más denso en el cubo, y los iones de sodio más pequeños llenan el espacio octaédrico entre los iones de cloruro. Each ion is surrounded by six other ions. This structure is also found in many other compounds, called sodium chloride type structure or stone salt structure.

1. Preparationof sodium metal by electrolytic melting of sodium chloride
2NaCl(molten) = 2Na + Cl2
2. Electrolytic saltwater
2NaCl + 2H2O = H2 + Cl2 + 2NaOH
3. React withsilver nitrate
NaCl + AgNO3 = NaNO3 + AgCl
Ionic equation:
Cl– + Ag+ = AgCl
(Which is theessence CI – property)
4. Reaction withconcentrated sulfuric acid (laboratory hydrogen chloride)
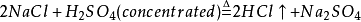

( Concentrated behalfconcentrated, Excess Representative excess)
5.NaCl test
A: se añadió cloruro de forma gota a gota a una solución de ácido nítrico con solución acidificada de nitrato de plata, se genera un precipitado blanco (cloruro de plata precipitado), probado CI– .
B: Sumerge una pequeña cantidad de solución con alambre de platino y colócala en una lámpara de alcohol para quemarla. La llama es amarilla y se puede probar que contiene Na+.
C: Para eliminar la interferencia, la solución de prueba original se puede agregar con hidróxido de bario saturado hasta que sea obviamente alcalina. En este momento, la mayoría de los cationes y aniones, como PO43 y AsO43, se precipitarán.
El Ba2 + introducido en la solución de ensayo debe eliminarse mediante carbonato de amonio y, finalmente, la sal de amonio debe eliminarse mediante combustión. Después de lixiviar el residuo con agua, la solución se acidificó con HAc, y se añadió el reactivo de acetato de uranil-zinc de acuerdo con el número de gotas de 1: 8, y se frotó la pared del tubo con una varilla de vidrio. Si se formaron cristales de color amarillo limón, estaba presente Na+.
Preparación de cloruro de sodio
Método industrial
Introducido en campos de sal por agua de mar (promedio de 2.cloruro de sodio al 4%) y secado al sol, Concentrado para cristalizar y obtener un producto crudo. El agua de mar también puede calentarse con vapor, filtrarse con un filtro de arena y concentrarse mediante electrodiálisis de membrana de intercambio iónico para obtener salmuera (que contiene cloruro de sodio 160-180 g / L).
El yeso de halo se precipita por evaporación y el cloro obtenido se centrifuga. Se puede secar más del 95% de sodio (2% de humedad)para obtener sal común. La sal de roca y la salmuera de lago salado también se pueden usar como materias primas y secarse al sol para obtener sal cruda.
Cuando se utilizan salmuera subterránea y sal de pozo como materias primas, se concentran mediante evaporación de tres o cuatro efectos, se precipitan cristales y se centrifugan para obtenerlos.
Método de laboratorio
La sal cruda se disuelve en agua para eliminar impurezas insolubles, y se agregan preparaciones refinadas como hidróxido de sodio y carbonato de sodio para hacer que las impurezas solubles como SO42-, Ca2+ y Mg2+ se conviertan en precipitados, se filtran para eliminarlas y finalmente se purifican con el pH ajustado a 7 con ácido clorhídrico, y la solución se concentró para obtener cristales puros de cloruro de sodio.
El método de preparación en el laboratorio consiste en mezclar una cantidad igual de ácido clorhídrico con hidróxido de sodio para formar una solución de cloruro sódico. La solución se destiló para obtener cristales de cloruro sódico. La reacción principal:
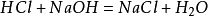
Además,el cloruro de sodio también producirá cloruro de sodio cuando se encienda en el entorno de gas de cloro. Su ecuación química es:
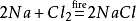
¿qué es el Cloruro de Sodio se utiliza para
Industria
1. Cuando la solución electrolítica de cloruro de sodio se selectroliza, se generarán gas de hidrógeno y cloro. El gas de cloro tiene una amplia gama de aplicaciones en la industria química y se puede utilizar para sintetizar cloruro de polivinilo, pesticidas, ácido clorhídrico, etc.
2. Preparación de sodio metálico por el método Dangs: Preparación de sodio metálico por fusión electrolítica de una mezcla de cloruro de sodio y cloruro de calcio. El cloruro de calcio se utiliza como fundente para bajar el punto de fusión del cloruro de sodio por debajo de 700 ° C. El calcio es menos reductor que el sodio y no introduce impurezas.
3. El cloruro de sodio es necesario para muchas reacciones biológicas. Por ejemplo, varias fórmulas de solución en experimentos de biología molecular contienen cloruro de sodio, y la mayoría del medio de cultivo bacteriano contiene cloruro de sodio. También es la materia prima en la producción de ceniza de soda por el método de amoníaco-álcali.
4. Las industrias inorgánicas y orgánicas se utilizan como materias primas para la producción de sosa cáustica, clorato, hipoclorito, polvo blanqueador, refrigerantes para sistemas de refrigeración, materias primas para síntesis orgánica y agentes de salazón. La industria del acero se utiliza como agente de tratamiento térmico. Se utiliza una fuente de calor de alta temperatura para formar un baño de sal con cloruro de potasio, cloruro de bario, etc., que se puede usar como medio de calentamiento para mantener la temperatura entre 820-960 ° C. Además, también se usa en vidrio, tintes, metalurgia y otras industrias.
5. Los reactivos analíticos se utilizan como reactivos de análisis de flúor y sílice.
6. Producción de ceniza de sosa por el método alcalino de Hou: segundo paso: la solución de bicarbonato de amonio preparada en el primer paso se mezcla con la solución de cloruro de sodio para obtener bicarbonato de sodio y cloruro de amonio a 10°C.
Industria alimentaria
La industria alimentaria y la pesca se utilizan para la sal, así como materias primas para condimentos y sal de mesa refinada.
Agregar sal a los platos de cocina puede eliminar algunos olores de materias primas y aumentar el sabor, que es el efecto de la frescura de la sal. «Ligeramente insípido, salado e insípido» significa que la cantidad adecuada de sal se puede usar para ejercer sus funciones únicas.
Médico
El cloruro de sodio es muy importante para la vida en la tierra. La mayoría de los tejidos biológicos contienen múltiples sales. La concentración de sodio en la sangre está directamente relacionada con la regulación del nivel seguro de fluidos corporales. La conducción de los impulsos nerviosos causados por la conversión de señales también está regulada por iones de sodio.
El agua que contiene cloruro de sodio al 0,9% se llama salina porque tiene la misma presión osmótica que el plasma. La solución salina normal es el principal sustituto del fluido corporal. Es ampliamente utilizado en el tratamiento y la prevención de la deshidratación, y también se utiliza en el tratamiento de la inyección intravenosa y la prevención del choque hipovolémico.
A diferencia de otros primates, los humanos secretan grandes cantidades de cloruro de sodio a través de la sudoración.
El cloruro de sodio es indispensable para los humanos. La cantidad total de iones de sodio contenidos en adultos es de aproximadamente 60 g, el 80% de los cuales se encuentra en el fluido extracelular, es decir, en el plasma y el fluido intercelular. El cloruro también está presente principalmente en el líquido extracelular. Las funciones fisiológicas de los iones de sodio y cloruro son:
(1) mantener la presión osmótica del fluido extracelular.
(2) participar en la regulación del equilibrio ácido-base en el cuerpo.
(3) El cloruro participa en la producción de ácido gástrico en el cuerpo. Además, el cloruro de sodio también desempeña un papel en el mantenimiento de la excitabilidad normal de nervios y músculos.
Agricultura
Su solución acuosa se puede utilizar para la selección de semillas. La solución NaCl se configura de acuerdo con las necesidades de la especie, y su densidad es mayor que la del agua. Las semillas se ponen en solución entoNaCl, flotando lleno y hundiéndose lleno.
otros
Según los nuevos hallazgos publicados por el Instituto de Investigación de Ciencia y Tecnología de Singapur, el cloruro de sodio puede aumentar significativamente la capacidad de los discos duros. Específicamente, el disco duro convencional existente utiliza una tecnología de almacenamiento de disco magnético asignada aleatoriamente, que solo puede lograr una densidad de datos de 0,5 TB por pulgada cuadrada.
La nueva tecnología se beneficia de la ayuda del cloruro de sodio. Con la nueva tecnología de factor de litografía de alta resolución, la densidad de datos será más ordenada, llegando a 3.3 TB por pulgada cuadrada sin necesidad de complicadas actualizaciones de equipos. El uso de un disco duro de 1 TB con esta tecnología puede alcanzar una capacidad de 6 TB sin agregar discos.
- Fórmula de amoníaco || por qué el amoníaco es tóxico || Envenenamiento por amoníaco
- Por qué es importante la Capa de Ozono || Agotamiento de la capa de ozono
- Cuál es la Concentración de la solución || Cómo la concentración Afecta la Reacción
- Por qué es importante el Ciclo de Carbono || Cómo Funciona
- Soluciones NCERT de Haloalcanos y Haloarenos || Estructura de Haloalcano
- Ciclo y Fórmula del Dióxido de Carbono || Cómo se Produce El Dióxido de Carbono
Leave a Reply