Proprietăți de clorură de sodiu || clorura de sodiu este bună pentru tine?
subiecte de articol
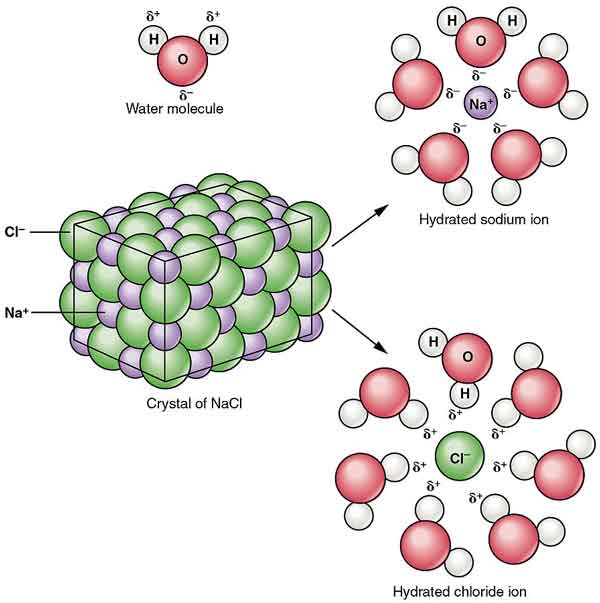
clorura de sodiu este un compus ionic cu formula chimică NaCl. Este un cristal cubic incolor sau o pulbere cristalină fină și are un gust sărat.
aspectul este un cristal alb, iar sursa sa este în principal apa de mare, care este componenta principală a sării de masă. Solubil în apă, glicerină, ușor solubil în etanol (alcool), amoniac lichid, insolubil în acid clorhidric concentrat. Clorura de sodiu impură este delicvescentă în aer.
stabilitatea este relativ bună, iar soluția sa apoasă este neutră. Industrial, metoda soluției de clorură de sodiu saturată electrolitic este utilizată în general pentru a produce hidrogen, clor și sodă caustică (hidroxid de sodiu) și alte produse chimice (denumite în mod obișnuit Industrie clor-alcalină).
poate fi utilizat în topirea minereurilor (topirea electrolitică a cristalelor de clorură de sodiu pentru a produce sodiu activemetal), utilizat medical pentru configurarea Salinei fiziologice și viața zilnicăpoate fi utilizat pentru condimente.
Introducere compus
informații de bază
engleză nume: clorură de sodiu
engleză alias: clorhidrat de sodiu; clorură de sodiu
Număr CAS: 7647-14-5
Formulă moleculară: NaCl
greutate moleculară: 58.44280
masa exactă: 57.95860
informații de securitate
Codul vamal: 2501002000
codul categoriei de pericol: R36; R22
instrucțiuni de siguranță: S24 / 25-S26
semnul mărfurilor periculoase: XI
proprietățile fizice ale clorurii de sodiu
aspect și proprietăți: cristal incolor saupulbere albă
densitate: 2.165g/cm3 (25 inqut C)
solubilitate în apă: 360 g/L (25 INQUTC)
stabilitate: stabilă în condiții normale de transport și manipulare.
conditii de depozitare: temperatura scazuta, ventilata si uscata in depozit
presiunea vaporilor: 1 mm Hg (865 inox C)
punct de topire: 801 inox c
punct de fierbere: 1465 inox
clorura de sodiu este o pulbere cristalina alba inodora. Mp 801 grade.] C, un punct de fierbere de 1465 grade.] C, ușor solubil în etanol, propanol, Butan, Butan și după ce plasma devine miscibilă, solubilă în apă, solubilitatea în apă de 35,9 g (temperatura camerei).
NaCl este dispersat în alcool pentru a forma coloizi. Solubilitatea sa în apă este redusă prin prezența clorurii de hidrogen și este aproape insolubilă în acid clorhidric concentrat.
proprietățile chimice ale clorurii de sodiu
cristalele de clorură de sodiu formează simetrie stereo. În structura sa cristalină, ionii de clorură mai mari formează cel mai dens ambalaj din cub, iar ionii de sodiu mai mici umple golul octaedric dintre ionii de clorură. Each ion is surrounded by six other ions. This structure is also found in many other compounds, called sodium chloride type structure or stone salt structure.

1. Preparationof sodium metal by electrolytic melting of sodium chloride
2NaCl(molten) = 2Na + Cl2
2. Electrolytic saltwater
2NaCl + 2H2O = H2 + Cl2 + 2NaOH
3. React withsilver nitrate
NaCl + AgNO3 = NaNO3 + AgCl
Ionic equation:
Cl– + Ag+ = AgCl
(Which is theessence CI – property)
4. Reaction withconcentrated sulfuric acid (laboratory hydrogen chloride)
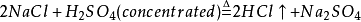

( Concentrated behalfconcentrated, Excess Representative excess)
5.NaCl test
A: clorura a fost adăugată prin picurare la o soluție de acid azotic a acidulat soluție de azotat de argint, un precipitat alb (clorură de argint precipitat) este generat, sa dovedit CI– .
B: înmuiați o cantitate mică de soluție cu sârmă de platină și puneți-o pe o lampă cu alcool pentru a arde. Flacăra este galbenă și se poate dovedi că conține Na+.
C: pentru a elimina interferențele, soluția de testare originală poate fi adăugată cu hidroxid de bariu saturat până când este evident alcalină. În acest moment, majoritatea cationilor și anionilor, cum ar fi PO43− și AsO43− vor fi precipitate.
Ba2+ introdus în soluția de testare trebuie îndepărtat cu carbonat de amoniu și, în final, sarea de amoniu trebuie îndepărtată prin ardere. După ce reziduul a fost levigat cu apă, soluția a fost acidificată cu HAc, iar reactivul de acetat de uranil zinc a fost adăugat în funcție de numărul de picături de 1: 8, iar peretele tubului a fost frecat cu o tijă de sticlă. Dacă s-au format cristale galbene de lămâie, Na+ a fost prezent.
prepararea clorurii de sodiu
metoda industrială
introdusă în câmpurile de sare de apa de mare (medie de 2.4% clorură de sodiu) și uscat la soare, concentrat pentru a cristaliza pentru a obține un produs brut. Apa de mare poate fi, de asemenea, încălzită cu abur, filtrată de un filtru de nisip și concentrată prin electrodializă cu membrană schimbătoare de ioni pentru a obține saramură (conținând clorură de sodiu 160-180g / L).
gipsul halo este precipitat prin evaporare, iar clorina obținutăeste centrifugat. Mai mult de 95% sodiu (2% umiditate) pot fi uscate pentru a obținesare comună. Sarea de rocă și saramura de lac sărat pot fi, de asemenea, folosite ca primemateriale și uscate la soare pentru a obține sare brută.
când saramura subterană și sarea de puț sunt utilizate ca materii prime, acestea suntconcentrate prin evaporare cu trei sau patru efecte, cristalele sunt precipitate și centrifugate pentru a obține.
metoda de laborator
sarea brută este dizolvată în apă pentru a îndepărta impuritățile insolubile, iar preparatele rafinate precum hidroxidul de sodiu și carbonatul de sodiu sunt adăugate pentru a face impuritățile solubile precum SO42-, Ca2+ și Mg2+ să devină precipitate, filtrate pentru a îndepărta și, în final, purificate cu pH-ul a fost ajustat la 7 cu acid clorhidric, iar soluția a fost concentrată pentru a obține cristale pure de clorură de sodiu.metoda preparării în laborator este de a amesteca o cantitate egală de acid clorhidric cuhidroxid de sodiu pentru a forma o soluție de clorură de sodiu. Soluția a fost atuncidistilat pentru a obține cristale de clorură de sodiu. Reacția principală:
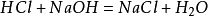
În plus,clorura de sodiu va produce, de asemenea, clorură de sodiu atunci când este aprinsă înmediul gazului de clor. Ecuația sa chimică este:
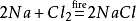
pentru ce se folosește clorura de sodiu
Industrie
1. Când este o soluție electrolitică de clorură de sodiuelectrolizat, hidrogen și clor gazos vor fi generate. Gazul de clor are o gamă largă de aplicații în industria chimică și poate fi utilizat pentru a sintetiza clorura de polivinil, pesticidele, acidul clorhidric etc.
2. Prepararea metalului de sodiu prin metoda Dangs: prepararea metalului de sodiu prin topirea electrolitică a unui amestec de clorură de sodiu și clorură de calciu. Clorura de calciu este utilizată ca flux pentru a scadepunctul de topire al clorurii de sodiu sub 700 de centi C. calciul este mai puțin reductiv decât sodiul și nu introduce impurități.
3. Clorura de sodiu este necesară pentru multe biologicereacții. De exemplu, diferite formule de soluție în biologie molecularăexperimentele conțin clorură de sodiu, iar cea mai mare parte a mediului de cultură bacterianconține clorură de sodiu. Este, de asemenea, materia primă în producția desoda cenușă prin metoda amoniacului-alcalin.
4. Industriile anorganice și organice sunt utilizate ca materii prime pentru producerea de sodă caustică, clorat, hipoclorit, pulbere de albire, agenți frigorifici pentru sisteme de refrigerare, materii prime pentru sinteza organică și agenți de sărare. Industria siderurgică este utilizată ca agent de tratament termic. O sursă de căldură la temperaturi ridicate este utilizată pentru a forma o baie de sare cu clorură de potasiu, clorură de bariu etc., care poate fi folosit ca mediu de încălzire pentru a menține temperatura între 820-960 centi C. În plus, este utilizat și în sticlă, coloranți, metalurgie și alte industrii.
5. Reactivii analitici sunt utilizați ca fluor și silicatreactivi de analiză a urmelor.
6. Producția de sodă calcinată prin metoda alcalină a lui Hou: a doua etapă: soluția de bicarbonat de amoniu preparată în prima etapă esteamestecată cu soluția de clorură de sodiu pentru a obține bicarbonat de sodiu și clorură de amoniu la 10 C.
industria alimentară
industria alimentară și pescuitul sunt utilizate pentrusărare, precum și materii prime pentru condimente și sare de masă rafinată.
adăugarea de sare la feluri de mâncare de gătit poate elimina unele odorsof materii prime și de a crește gustul, care este efectul de saltfreshness. „Ușor fără gust, sărat și fără gust” înseamnă căcantitatea adecvată de sare poate fi utilizată pentru a-și exercita funcțiile unice.
Medical
clorura de sodiu este foarte importantă pentru viațăpământ. Majoritatea țesuturilor biologice conțin săruri multiple. Concentrația de sodiu în sânge este direct legată de reglareanivelul sigur al fluidelor corporale. Conducerea impulsurilor nervoase cauzate deconversia semnalului este, de asemenea, reglementată de ionii de sodiu.
apa care conține 0,9% clorură de sodiu se numește salinădeoarece are aceeași presiune osmotică ca și plasma. Salina normală esteprincipalul înlocuitor al fluidului corporal. Este utilizat pe scară largă în tratamentul și prevenireade deshidratare și este, de asemenea, utilizat în tratamentul injecției intravenoaseși prevenirea șocului hipovolemic.spre deosebire de alte primate, oamenii secretă cantități mari de clorură de sodiu prin transpirație.
clorura de sodiu este indispensabilă pentruoameni. Cantitatea totală de ioni de sodiu conținută la adulți este de aproximativ 60g,din care 80% este în lichidul extracelular, adică în plasmă și intercelularfluid. Clorura este, de asemenea, prezentă în principal în lichidul extracelular. Funcțiile fiziologice ale ionilor de sodiu și clorură sunt:
(1) menținerea presiunii osmotice a fluidului extracelular.(2) participă la reglarea echilibrului acido-bazic în organism.(3) clorura este implicată în producerea acidului gastric în organism. În plus, clorura de sodiu joacă, de asemenea, un rol înmenținând excitabilitatea normală a nervilor și a mușchilor.
Agricultură
soluția sa apoasă poate fi utilizată pentru selectarea semințelor. Soluția NaCl este configurată în funcție de necesitățilespecii, iar densitatea sa este mai mare decât cea a apei. Semințele sunt puse însoluție de tonacl, plutind complet și scufundând complet.
altele
conform noilor descoperiri publicate de Institutul de cercetare din Singapore și Tehnologie, clorura de sodiu poate fi semnificativăcrește Capacitatea hard disk-urilor. Mai exact, hard disk-ul existentconvențional utilizează o tehnologie de stocare a discului magnetic alocată aleatoriu, care poate atinge doar o densitate de date de 0,5 TB pe inch pătrat.
noua tehnologie beneficiază de ajutorul clorurii de sodiu. Cu noua tehnologie a factorului de litografie de înaltă rezoluție, datadensitatea va fi mai ordonată, ajungând la 3.3TB pe inch pătrat fără a fi nevoie de upgrade-uri complicate de echipamente. Folosind hard disk de 1 TB cu acest lucrutehnologia poate atinge capacitatea de 6 TB fără a adăuga discuri.
- Formula amoniacului || de ce amoniacul este toxic || otrăvirea amoniacului
- De ce stratul de ozon este Important || epuizarea stratului de ozon
- care este concentrația soluției || cum afectează concentrația reacția
- de ce este important ciclul carbonului || cum funcționează
- Haloalkani și soluții Haloarenes NCERT || structura Haloalkanului
- ciclul și Formula dioxidului de Carbon || cum se produce dioxidul de Carbon
Leave a Reply