塩化ナトリウムの特性|/塩化ナトリウムはあなたのためによいですか。
記事のトピック
塩化ナトリウムは、化学式NaClを有するイオン性化合物である。 それは無色の立方晶または微結晶性粉末であり、塩辛い味がする。
外観は白い結晶であり、その源は主に食塩の主成分である海水である。 水に可溶、グリセリン、エタノール(アルコール)にわずかに可溶、液体アンモニア、濃塩酸に不溶。 不純な塩化ナトリウムは空気中で潮解性である。
安定性は比較的良好であり、その水溶液は中性である。 工業的には、電解的に飽和した塩化ナトリウム溶液の方法は、一般に、水素、塩素および苛性ソーダ(水酸化ナトリウム)および他の化学製品(一般に塩素アルカリそれはoresmelting(activemetalナトリウムを作り出す塩化ナトリウムの水晶の電気分解の溶けること)で、生理学的な塩を形成するのに医学的に使用する使用することがでP>
CAS番号:7647-14-5分子式:NaCl分子量:58.44280正確な質量:57.95860
セキュリティ:10.00000
10.00000
10.00000
10.00000
10.00000
10.00000
10.00000
10.00000
10.00000
10.00000
10.00000
10.00000
10.00000
情報
税関コード:2501002000
危険カテゴリコード:r36;r22
安全上の注意事項:S24/25-s26
危険物記号:xi
塩化ナトリウムの物理的性質
外観と特性:無色の結晶orwhite粉末
密度:2。165g/cm3(25°C)
水容解性:360g/L(25º C)
安定性:正常な船積みおよび処理の条件の下で安定した。
保管条件:低温、換気および倉庫内で乾燥
蒸気圧:1mmhg(865°C)
融点:801°C
沸点:1465℃
塩化ナトリウムは白色無臭の結晶性粉末である。 Mp801deg.]C、沸点は1465℃である。]C、エタノール、プロパノール、ブタン、ブタンにわずかに溶解し、血漿が混和性になった後、水に可溶、35.9g(室温)の水溶解度。
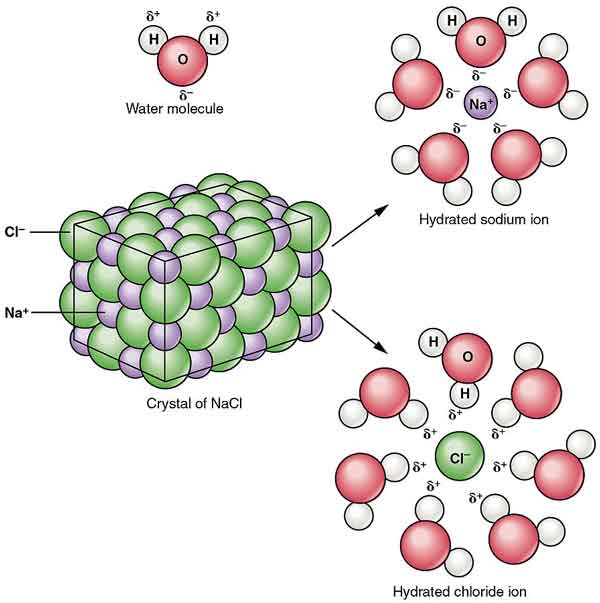
NaClはアルコール中に分散してコロイドを形成する。 水のその容解性は塩化水素の存在によって減り、集中された塩酸でほとんど不溶解性です。
塩化ナトリウムの化学的性質
塩化ナトリウムの結晶は立体対称性を形成する。 結晶構造では、より大きい塩化物イオンは立方体の最も密なパッキングを形作り、より小さいナトリウムイオンは塩化物イオン間の八面体のギャップを Each ion is surrounded by six other ions. This structure is also found in many other compounds, called sodium chloride type structure or stone salt structure.

1. Preparationof sodium metal by electrolytic melting of sodium chloride
2NaCl(molten) = 2Na + Cl2
2. Electrolytic saltwater
2NaCl + 2H2O = H2 + Cl2 + 2NaOH
3. React withsilver nitrate
NaCl + AgNO3 = NaNO3 + AgCl
Ionic equation:
Cl– + Ag+ = AgCl
(Which is theessence CI – property)
4. Reaction withconcentrated sulfuric acid (laboratory hydrogen chloride)
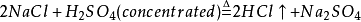

( Concentrated behalfconcentrated, Excess Representative excess)
5.NaCl test
A: 硝酸銀の溶液を酸性化していた硝酸の溶液に塩化物を滴下し、白色の沈殿物(塩化銀の析出)が発生し、CI–を証明した。
B:少量の溶液を白金線で浸し、アルコールランプの上に置いて燃焼させます。 炎は黄色で、Na+が含まれていることが証明できます。
C:干渉を排除するために、元の試験溶液に飽和水酸化バリウムを加えて明らかにアルカリ性になるまで加えることができます。
C: この時点で、PO43−およびAso43−のようなほとんどの陽イオンおよび陰イオンは沈殿します。
試験溶液に導入されたBa2+は炭酸アンモニウムによって除去され、最終的にアンモニウム塩は燃焼によって除去されるべきである。 残渣を水で浸出した後、溶液をHAcで酸性化し、酢酸ウラニル亜鉛試薬を1:8の滴数に従って添加し、管壁をガラス棒で擦った。 レモンイエロー結晶が形成された場合,Na+が存在した。
塩化ナトリウムの調製
工業的方法
海水によって塩田に導入された(平均2。4%塩化ナトリウム)を天日で乾燥し、濃縮して結晶化させ、粗生成物を得た。 海水はまた、蒸気で加熱し、砂フィルターで濾過し、イオン交換膜電気透析によって濃縮して塩水(塩化ナトリウム160-180g/Lを含む)を得ることができる。
ハロー石膏は蒸発によって沈殿し、得られた塩素は遠心分離される。 95%以上ナトリウム(2%の湿気)はobtaincommonの塩に乾燥することができます。 岩塩と塩湖の塩水は、生の塩を得るために太陽の下で乾燥させた材料としても使用することができます。
地下塩水および井戸塩を原料として使用する場合、それらは三効果または四効果蒸発によって濃縮され、結晶が沈殿し、遠心分離されて得られる。
実験室法
粗塩を水に溶解して不溶性不純物を除去し、水酸化ナトリウムや炭酸ナトリウムなどの精製された調製物を加えてSO42-、Ca2+、Mg2+などの可溶性不純物を沈殿物にし、濾過して除去し、最後にphを塩酸で7に調整し、溶液を濃縮して純粋な塩化ナトリウム結晶を得た。
実験室での調製方法は、等量の塩酸を水酸化ナトリウムと混合して塩化ナトリウム溶液を形成することである。 この溶液を用いて塩化ナトリウム結晶を得た。 主な反応:
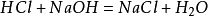
塩素ガスの環境で点火すると、塩化ナトリウムも塩化ナトリウムを生成します。 その化学式は次のとおりです。
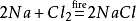
塩化ナトリウムは何のために使用されていますか
産業
1。 電気分解の塩化ナトリウムの解決がiselectrolyzed場合、水素および塩素のガスは発生します。 塩素のガスに化学工業でawideの応用範囲があり、使用されたtosynthesizeポリ塩化ビニル、殺虫剤、塩酸、等である場合もあります。
2. Dangs法によるナトリウム金属の調製:塩化第二ナトリウムと塩化カルシウムの混合物を電解溶融することによるナトリウム金属の調製。 塩化カルシウムは700°c.カルシウムの下の塩化ナトリウムのlowertheの融点への変化としてナトリウムよりlessreductive、不純物をもたらさない使用されます。
3. 塩化ナトリウムは多くの生物学的に必要である反応。 例えば、分子生物学実験における様々な溶液式は塩化ナトリウムを含み、細菌培養媒体のほとんどは塩化ナトリウムを含む。 それはまたアンモナルアルカリ方法による生産のofsodaの灰の原料です。
4. 無機および有機産業は、苛性ソーダ、塩素酸塩、次亜塩素酸塩、漂白粉末、冷凍システム用冷媒、有機合成用原材料および塩析剤の製造の原料として使用され 製鉄業は熱処理の代理店として使用されます。 高温熱源は塩化カリウム、塩化バリウム、等が付いている塩の浴室を形作るのに使用されています。 さらに820-960°c.間の温度を維持するのに熱媒体として使用することができるかどれが、ガラス、染料、冶金学および他の企業でも使用されます。
5. 分析試薬は、フッ素およびケイ酸トレース分析試薬として使用される。
6. Houのアルカリ方法によるソーダ灰の生産:thesecondのステップ:10°C.で重炭酸ナトリウムのandammoniumの塩化物を得るために塩化ナトリウムの解決と最初のステッ
食品産業
食品産業と漁業は、調味料や精製された食塩の原料だけでなく、塩漬けにも使用されています。
料理に塩を加えると、原材料のいくつかの臭いを取り除き、塩味の効果である味を高めることができます。 “わずかに無味、塩辛い、無味”とは、適切な量の塩を使用して独自の機能を発揮することができます。
医療
塩化ナトリウムは人生にとって非常に重要です地球。 ほとんどの生物学的組織は、複数の塩を含む。 血液中のナトリウムの濃度は、体液の安全なレベルの調節に直接関係している。 によって引き起こされる神経インパルスの伝導信号変換はまた、ナトリウムイオンによって調節される。
0.9%塩化ナトリウムを含む水はsalinebecそれは血漿と同じ浸透圧を有するからである。 通常の生理食塩水は主な体液代用品です。 それは処置およびpreventionofの脱水で広く利用されて、静脈内のinjectionandの処置でもhypovolemic衝撃の防止使用されます。
他の霊長類とは異なり、人間は発汗によって大量の塩化ナトリウムを分泌する。
塩化ナトリウムは不可欠です人間。 成人に含まれるナトリウムイオンの総量は約60gであり、その80%は細胞外液、すなわち血漿および細胞間液中にある。 塩化物はまた、主に細胞外液中に存在する。 ナトリウムおよび塩化物イオンの生理学的機能は次のとおりである:
(1)細胞外液の浸透圧を維持する。
(2)体内の酸-塩基バランスの調節に参加する。
(3)塩化物は、体内の胃酸。 さらに、塩化ナトリウムはまた、神経および筋肉の正常な興奮性を維持する。
農業
その水溶液は、種子選択のために使用することができます。 NaCl溶液は、その密度は水の密度よりも大きい。 種子は、完全に浮遊し、完全に沈んでいる。
その他
SingaporeScience And Technology Research Instituteが発表した新しい調査結果によると、塩化ナトリウムはハードドライブの容量を大幅に増加させる可能性があります。 具体的には、existingconventionalのハードディスクは平方インチごとの0.5TBのデータ密度しか達成できない任意に割振られた磁気ディスクのstoragetechnologyを使用します。
塩化ソーダの助けからの新技術の利点。 新しい高解像の石版画の要因技術によって、datadensityはより整然として、3.に達します。Needforの複雑な装置の改善のない平方インチごとの3TB。 この技術で1TBのハードディスクを使用すると、ディスクを追加することなく6TBの容量に達することができます。
- アンモニア式||アンモニアが有毒である理由||アンモニア中毒
- オゾン層が重要である理由||オゾン層の枯渇
- 溶液の濃度は何ですか||濃度が反応にどのように影響するか
- 炭素サイクルが重要である理由||それがどのように動作するか
- ハロアルカンとハロアレンNCERT溶液||ハロアルカン構造
- 二酸化炭素サイクルと式||二酸化炭素がどのように生成されるか
Leave a Reply