Servier-Phlebolymphology
töltse le ezt a kérdést vissza az összefoglalóhoz
az alsó végtagok trombózisa:
update jelenlegi
ajánlások
Bourgoin-Jallieu, Franciaország
Absztrakt
Kezdetben, felületes vénás trombózis (SVT) ítélték meg, hogy egy jóindulatú betegség, vagy egy gyakori szövődménye a visszér. A közelmúltban végzett vizsgálatok kimutatták az SVT lehetséges súlyosságát, és meghatározták helyét a vénás thromboemboliás (VTE) betegségekben, valamint a mélyvénás trombózisban (DVT) és a tüdőembóliában (PE). Az egyidejű DVT-t a betegek 25-30% – ánál, a PE-t pedig a betegek 4-7% – ánál azonosították. Az ezt követő VTE-t a betegek 3-20% – ánál jelentették, a követés időtartamától függően. Egészen a közelmúltig számos antikoaguláns stratégiát teszteltek, egyértelműen nem bizonyított klinikai előny. Azonban a legutóbbi CALISTO tanulmány (Összehasonlítás a Arixtra az alsó Végtag Felületes vénás Trombózis, míg a placebo) validált egy antikoaguláns kezelés protokoll alapján, fondaparinux, 2,5 mg, napi 45 nap, amely a frissített ajánlások a menedzsment SVT. Ez a cikk aktualizálja az alsó lábú SVT kezelését, valamint a jelenlegi ajánlásokat és iránymutatásokat. Röviden, minden SVT-ben szenvedő betegnek kétoldalú duplex szkenneléssel kell rendelkeznie az SVT diagnózisának megerősítésére, az SVT pontos helyének és mértékének meghatározására, valamint a DVT jelenlétének diagnosztizálására vagy kizárására. Azoknál a betegeknél, akiknél a tüneti SVT legalább 5 cm hosszú, ajánlott előírni egy profilaktikus adag fondaparinux vagy kis molekulatömegű heparin 45 napig nem antikoaguláns (Grade 2b), és ha a kezelés költsége fondaparinux elfogadható, akkor ajánlott használni fondaparinux 2,5 mg naponta vs alacsony molekulatömegű heparin (Grade 2C). Az ajánlások és iránymutatások azonban ezeket a kezeléseket alacsony fokozattal rendelték el, és továbbra is kérdések merülnek fel az SVT kezelésével kapcsolatban. A VTE későbbi kialakulásának néhány kockázati tényezőjét azonosították, de további kutatásokra van szükség azon betegek alcsoportjainak meghatározásához, akiknél az SVT után nagyobb a VTE előfordulása.
Bevezető
Felületes vénás trombózis (SVT) tekinthető egy jóindulatú betegség, vagy gyakori szövődménye a visszerek; azonban a legújabb vizsgálatok kimutatták, hogy a potenciális súlyossága, valamint a meghatározott helyen belül a vénás tromboembóliás (VTE) betegségek, valamint a mélyvénás trombózis (DVT), valamint a pulmonalis embolia (PE).
az antikoaguláns terápiát ma széles körben alkalmazzák a nem szteroid gyulladáscsökkentő gyógyszerek (NSAID) helyett, amelyeket az elmúlt évtizedig általánosan használtak. Egy nemrégiben készült tanulmány először validált egy terápiás protokollt.1 az SVT kezelésével kapcsolatos kérdések azonban továbbra is fennállnak: I. szükséges-e antikoaguláns terápia az összes alsó végtagi SVT-ben szenvedő beteg kezelésére?; ii. profilaktikus vagy terápiás dózisokat kell alkalmazni?; iii. mi az ajánlott kezelés időtartama?; iv. amennyiben a menedzsment azonos SVT előforduló visszerek és nem visszerek?; (v) megjósolható-e a VTE komplikációk kockázati tényezői az SVT után?; és (vi) a műtét továbbra is javallt-e akut SVT kezelésére?
Ez a cikk bemutatja az SVT-k kezelésére vonatkozó frissítés indokait, valamint a jelenlegi ajánlásokat és iránymutatásokat.
az alsó végtagok felszíni vénás trombózisának incidenciája
az SVT gyakori betegségnek számít, de a felnőtt populációban a tényleges előfordulási gyakoriság nem ismert. Egy nemrégiben készült tanulmány, amelyet Franciaországban végeztek, 2 azt mutatta, hogy az éves diagnózis aránya 0,6% volt. Ez magasabb volt a nőknél és nőtt az életkor előrehaladtával, nemtől függetlenül. Meglepő módon az SVT éves diagnózisának aránya a vártnál alacsonyabb volt, és alacsonyabb, mint a DVT éves diagnózisának aránya (körülbelül a fele a DVT-nek). Egy másik, hasonló módszerekkel végzett francia tanulmány szerint az alsó végtag DVT és PE éves előfordulási gyakorisága 1,24%, illetve 0,6% volt.3
Felületes vénás trombózis egyidejű mélyvénás trombózis a bemutató
A POSZT (Leendő Megfigyeléses Felületes Thrombophlebitis), valamint OPTIMEV tanulmányok (Optimalizálás de l’Interrogatoire dans l létrehozott du merész thromboembolia – Embolique Veineux), két nagy megfigyeléses, illetve epidemiológiai vizsgálatok, a közelmúltban megjelent a lényeges adatokat SVT.4,5 a post-vizsgálatban összesen 844, SVT lábakkal rendelkező beteget vizsgáltak, 4-et, a PREZENTÁCIÓKOR SVT-ben szenvedő betegek 25% – ánál pedig DVT-t vagy PE-t azonosítottak, a betegek 9,7% – ánál pedig proximális DVT-t diagnosztizáltak. Hangsúlyoznunk kell, hogy a DVT a DVT-ben szenvedő betegek 41, 9% – ánál nem volt összefüggő az SVT-vel. Az OPTMEV-vizsgálatba összesen 788, SVT-ben szenvedő beteget vontak be, 5-öt, ahol a betegek 29% – ában egy SVT-vel társult a DVT, a disztális DVT pedig ezen betegek 59,5% – ában (128/215; a DVT pontos helye 12 beteg esetében hiányzott).
ezek az adatok megerősítik a korábbi vizsgálatokat, amelyek azt mutatták, hogy a DVT a betegek 23-36% – ánál társult SVT-vel, és koherenciát mutatnak a különböző vizsgálatok között (I. táblázat).2,4-10
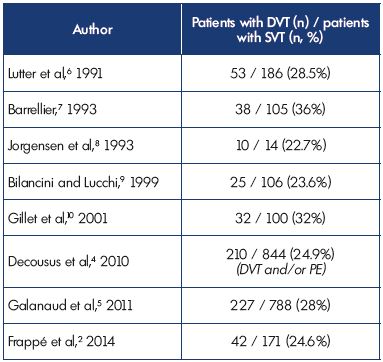
I. táblázat felületes véna trombózis egyidejű mélyvénával
trombózis prezentációkor.
rövidítések: DVT, mélyvénás trombózis; PE, tüdőembólia; SVT,
felületes vénás trombózis.
tüdőembóliával összefüggő felületes vénás trombózis
megjelenéskor a szimptómás PE-t 3, 9% – ban és 6-ban diagnosztizálták.A POST és OPTIMEV vizsgálatokban a betegek 9% – a vett részt. Azonban az SVT a PE-vel, de DVT nélkül, az összes SVT-nek csak 2, 2% – át tette ki DVT-vel vagy PE-vel. Ezek az adatok megerősítik a korábbi vizsgálatok eredményeit (II.táblázat).2,4-7,9,10
a gyakorlatban az SVT-ben szenvedő betegeknél duplex szkennelési vizsgálat szükséges a diagnózis megerősítésére (1. ábra), az SVT pontos helyének és mértékének meghatározására, valamint a DVT jelenlétének diagnosztizálására vagy kizárására.
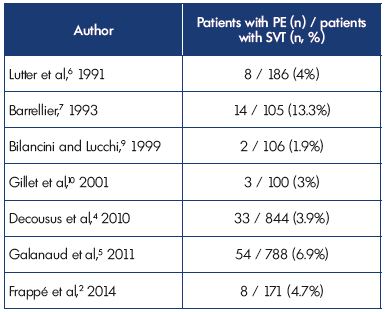
II. táblázat: felületes vénás trombózis egyidejű pulmonalis
embolia a bemutatáskor.
rövidítések: PE, tüdőembólia; SVT, felületes vénás trombózis.
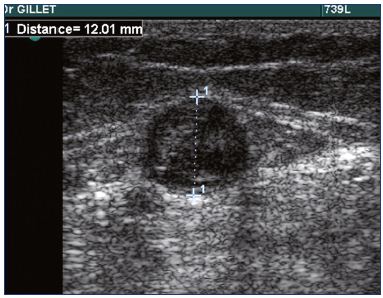
1.ábra. A kis saphena véna trombózisának ultrahangja.

kimenetel és vénás thromboemboliás kiújulás
a szakirodalomban a thromboemboliás kiújulás aránya a követés időtartamától függően 3% és 20% között mozog. Személyes tanulmány,13 jelentettük, hogy az esemény tüneti VTEs a 16.4% – a betegek elkülönített SVT, egy átlagos utánkövetési 14,5 hónap. A VTE eseményei közé tartozott a DVT (31%), A PE (6%), egy másik SVT egy másik saphenous rendszerben (37,5%), valamint egy visszatérő SVT ugyanabban a saphenous rendszerben (25%).
a POST-vizsgálatban 4 8.A befogadáskor izolált SVT-ben szenvedő betegek 3% – ánál alakult ki legalább 1 tüneti VTE-esemény 3 hónap alatt (tüneti DVT, 2,8%; tüneti PE, 0,5%; az SVT tüneti kiterjesztése, 3,3%; és az SVT tüneti kiújulása, 1,9%). Az OPTIMEV-vizsgálatban az izolált SVT-ben szenvedő betegek 5 3%-ánál, a prezentáció során DVT-vel társult SVT-ben szenvedő betegek 5,4% – ánál alakult ki VTE 3 hónap alatt; a VTE-k aránya 12,5% volt a 3 éves követés során. A Dewar és a Panpher által végzett vizsgálatban a 6 hónapos követés során az izolált SVT-vel rendelkező betegek 4%-ánál fordult elő tüneti DVT.
ezek az epidemiológiai eredmények az SVT lehetséges súlyosságát mutatják. Ezeket már nem szabad jóindulatú állapotnak tekinteni. Következésképpen helyüket most egyértelműen meghatározták a VTE betegségekben.
Kockázati tényezők a fejlődő thromboemboliás esemény
A többváltozós elemzés a POST study4 azonosított férfi nemi, történelem, MVT, illetve PE, előző rák, nincs visszér, mint kockázati tényező a szimptómás VTE 3 hónap, beleértve a kiújulás vagy kiterjesztése az SVT. A STENOX vizsgálatban (Enoxaparinnal kezelt felületes Thrombophlebitis) a VTE (DVT vagy PE), a férfi nem és a súlyos krónikus vénás elégtelenség 15 anamnézisét azonosították független prediktív tényezőként egy VTE esetében 3 hónap alatt. Csak a súlyos krónikus vénás elégtelenség volt független prediktív tényező a DVT vagy a PE esetében. A POST és OPTIMEV vizsgálatok összesített elemzésében 16 Galanaud et al kimutatta, hogy a férfi nem, a rák, a VTE személyes kórtörténete, valamint a saphenofemoral vagy a saphenopoplitealis részvétel jelentősen megnövelte a későbbi VTE vagy DVT/ PE kockázatát egy univariate elemzésben. Többváltozós elemzésekben csak a férfi nem jelentősen növelte a későbbi VTE vagy DVT/PE megismétlődésének kockázatát. A rák meg egy személyes története VTE, a kiigazított veszélyességi arány csak valamivel alacsonyabb a statisztikai szignifikancia szintje (P=0.06 egyaránt), ami arra utal, hogy ezek a tényezők, a tanulmány csupán hiányzott a kellő mennyiségű statisztikai erő.
a STEFLUX-vizsgálatban (felületes thromboembolia FLUXum) 17, 25 és 30 kg/m2 közötti testtömegindexszel (BMI) és egy korábbi SVT és/vagy VTE és/vagy családi anamnézisben szereplő VTE-vel (összetett tünetmentes és tünetmentes DVT, PE és SVT kiújulás vagy kiterjesztés) szignifikáns független kockázati tényezőként azonosították.
vena status
a varikózus véna státuszról számoltak be, hogy befolyásolja a DVT megjelenítésének kockázatát a bemutatáskor. A POST4 és OPTIMEV vizsgálatokban a nem varikózisos vénában (NVV–SVT) előforduló 5 SVT-t gyakrabban társították egyidejű DVT-vel vagy PE-vel, mint a varikózisos vénában (VV-SVT) előforduló SVTs-t. Hasonló eredményekről számolt be Gorty et al.18
az OPTIMEV-vizsgálatban végzett 3 hónapos követés során az izolált NVV-SVT nem járt a mellékhatások (azaz halál, VTE kiújulás és vérzés) nagyobb kockázatával. Elszigetelt NVV-SVT magasabb volt a szövetség tüneti MVT, illetve PE kiújulás (2.7% vs 0.6%), de ez az eredmény nem érte el a statisztikai szignifikancia (P=0.07).
a POSZT vizsgálat hiányában a visszerek azonosították, mint kockázati tényező a későbbi fejlődés a szimptómás VTE a betegek egy elszigetelt tüneti SVT a bemutató (P=0.049). A STEFLUX vizsgálatban 17 a varikózis hiánya a VTE (P=0, 004) kockázati tényezője volt az alacsony molekulatömegű heparinnal végzett kezelés leállítása után.
a placebo-csoportban a CALISTO tanulmány (Összehasonlítás a Arixtra az alsó Végtag Felületes vénás Trombózis, míg a placebo),1 thromboemboliás szövődmények gyakrabban fordult elő, amikor az SVT benne a nagy véna saphena (GSV), kiterjesztették belül 10 cm-es saphenofemoral junction (SFJ), érintett vénák a térd felett, valamint a betegeknél, akiknek kórtörténetében VTE.
a vénás pangás az SVT elsődleges mechanizmusa a varikózus vénákban szenvedő betegeknél. A gyulladás alapvető szerepet játszhat a trombusképződésben a varikózis nélküli betegeknél; ezáltal nagyobb kockázatot jelent a klinikailag súlyosabb thromboembolia. A thrombophilia szűrése nem ajánlott az NVV-SVT-ben szenvedő betegek rutinszerű kezelésére, bár a szakirodalomból származó adatok azt mutatták, hogy ebben a helyzetben gyakori a trombofília. Egy személyes prospektív vizsgálatban 10 trombofíliát azonosítottunk az NVV-SVT-ben szenvedő betegek 50% – ában, míg a VV-SVT-ben szenvedő betegek mindössze 15% – ánál volt trombofília. Egy másik prospektív vizsgálatban, amelyben 42 NVV-SVT-ben szenvedő beteg vett részt, 19 trombofíliát azonosítottunk 20 (47, 6%) betegnél. A leggyakoribb trombofília a heterozigóta V Leiden mutáció miatt következett be. Egy 63, izolált NVV-SVT-ben szenvedő beteg bevonásával végzett vizsgálatban 20 Martinelli et al a betegek 30% – ánál azonosított trombofíliát. A trombofília szűrése ajánlott az okkult rák kizárása után, különösen a megfelelő antikoaguláns terápia ellenére thrombus progresszióban szenvedő betegeknél.11,21
felületes vénás trombózis kezelése
az SVT kezelése mindig is ellentmondásos téma volt. A kezelés nagy változásairól számoltak be, különösen az antikoaguláns terápia tekintetében. A 2005 márciusa és 2006 októbere között Franciaországban elvégzett POST-vizsgálat 4 érdekes információkat szolgáltatott az SVT-kezeléssel kapcsolatban. Összesen 634 beteg kapott izolált SVT-t a felvételkor. A 3 hónapos megfigyelési időszak alatt kapott kezelésre vonatkozó információk 597 beteg számára álltak rendelkezésre, a betegek 90,5% – a kapott egy vagy több antikoaguláns gyógyszert. Az antikoaguláns kezelésben részesülő betegek 63% – a kapott terápiás dózist, 36,7% profilaktikus dózist és 16,8% K-vitamin antagonistát. A kezelés időtartama igen változó volt. Összesen 47.A betegek 2% – a kapott lokális NSAID-t, 8,2% – UK orális NSAID-t, 10%-uk pedig vénás műtétet (Sztrippelés vagy magas ligálás).
Ezek az adatok azt mutatták, hogy szükség van az antikoaguláns terápia szerepének tisztázására az SVT kezelésében. Az antikoaguláns terápia alkalmazását SVT-ben szenvedő betegeknél először 1962-ben jelentette a Zollinger et al,22 a PE előfordulásának megfigyelése után, amely halálos kimenetelű volt a 335 SVT-ben szenvedő betegből álló sorozat 34 (10, 1%) esetében. Egészen a közelmúltig, bár számos antikoaguláns stratégiát teszteltek, beleértve a nem frakcionált heparint vagy az alacsony molekulatömegű heparint, profilaktikus vagy terápiás dózisokban különböző időtartamokra, egyik sem mutatott egyértelműen klinikai előnyöket.
a STENOX-vizsgálat23 randomizált, kettős-vak vizsgálat volt 427 beteg bevonásával, kis molekulatömegű heparint (enoxaparint terápiás és profilaktikus dózisban) összehasonlítva NSAID-kel és placebóval. A betegeket 10 napig kezelték, 3 hónapos követéssel. 10 nap elteltével több VTE volt a placebo csoportban (a p24 a GSV-ben izolált SVT-ben szenvedő 163 betegnél hasonlította össze a nodraparin terápiás vs profilaktikus adagjait, a betegeket pedig 1 hónapig kezelték. A 3 hónapos követés során az eredmények mindkét csoportban hasonlóak voltak (a VTE 7,2%-os, illetve 8,6% – os előfordulása; P=0,7), ami nem mutatta a terápiás dózis előnyeit. A nyomon követés során” felzárkózási ” vagy rebound jelenséget figyeltek meg, mivel sok VTE-t jelentettek, különösen a terápiás dózissal kezelt betegek csoportjában. A STEFLUX-vizsgálatban a kis molekulatömegű heparin-kezelés 1 hónap elteltével történő abbahagyása után” felzárkózási ” jelenséget is megfigyeltek.25 Ezek az eredmények, mint a STENOX-vizsgálat eredményei, az SVT-ben a kis molekulatömegű heparin profilaktikus dózisainak megválasztására hivatkoznak. A VTE-k többségének előfordulása az alacsony molekulatömegű heparinnal történő kezelés abbahagyását követő 2-3 hónapban a terápiás dózisokat kapó csoportban ismét kiemeli az antikoaguláns terápia optimális időtartamának kérdését.
A randomizált, kettős-vak, CALISTO tanulmány1 képest fondaparinux 2,5 mg naponta 45 napon a placebo 3002 betegek egy elszigetelt tüneti alsó végtag SVT, hogy legalább 5 cm hosszú. A fő kizárási kritériumok voltak kezelés a rák belül az előző 6 hónapban, MVT, illetve PE belül az előző 6 hónapban az SVT belül található 3 cm a SFJ, súlyos veseelégtelenségben (kreatinin clearance 26 a 2,5 mg-os adag fondaparinux-válogatott a gondolat, hogy egy profilaktikus adag elegendő lenne ahhoz, hogy a betegek kezelése SVT. Ezen túlmenően, ez a dózis kimutatták, hogy a hatékonyabb megelőzése VTEs miután nagy ortopédiai műtét, mint egy profilaktikus dózisú, kis molekulatömegű heparin, majd olyan hatékony, mint a terápiás dózisú, kis molekulatömegű heparin a betegek akut koronária szindrómában, ami arra utal, hogy a 2,5 mg fondaparinux megegyezik a 2008-as American College of Chest Physicians (ACCP) recommendations27, hogy támogatják a használatát sem, profilaktikus vagy közepes dózisú, kis molekulatömegű heparin szenvedő betegek kezelésére az SVT. A 45 napos időtartamot azért választották, mert a 30 napos vagy annál rövidebb kezelési időszak túl rövid lehet, mivel a legtöbb tüneti VTE a kezelés abbahagyása után jelentkezik. Az elsődleges hatásossági eredmény bármilyen okból bekövetkező halál, tüneti PE, tüneti DVT, az SFJ tüneti kiterjesztése vagy az SVT tüneti megismétlődése volt a 47.napon. 77 napos követési időszak volt a betegek számára.
az elsődleges hatásossági eredmény a fondaparinux-csoportban a betegek 0, 9% – ánál és az 5.9% a placebo csoportban (P28

érdekes észrevenni a 2008-as ACCP iránymutatások ajánlásainak változását.27 figyelembe kell azonban vennünk, hogy ezek alacsony minőségű ajánlások (2b vagy 2C fokozat).
a Cochrane adatbázis frissítésében a “láb felületes thrombophlebitisének kezelése”szisztematikus áttekintése 29,30 Di Nisio et al ugyanazokat a következtetéseket vonta le. Ez a felülvizsgálat 30 randomizált, kontrollált vizsgálat elemzésén alapult, amelyekben 6507 résztvevő vett részt a lábak SVT-jével. A szerzők arra a következtetésre jutottak, hogy a fondaparinux profilaktikus dózisa, amelyet 6 hétig adnak, érvényes terápiás lehetőségnek tűnik a lábak SVT-jére. A szájüregi kezelésekre, a helyi kezelésre vagy a műtétre vonatkozó bizonyítékok túl korlátozottak, és nem nyújtanak információt a klinikai gyakorlatban történő alkalmazáshoz e kezeléseknek a VTE és az SVT progresszió tekintetében kifejtett hatásairól.
sebészet versus antikoaguláns terápia
a sebészeti beavatkozást antikoaguláns terápiával összehasonlító vizsgálatok áttekintése nem mutat semmilyen előnyt a sebészeti kezelésre. Az SVT progressziójának aránya hasonló volt, míg a VTE és a szövődmények incidenciája magasabb volt a műtét során.31 A Lozano et al 4 héten át nem mutatott különbséget a műtét és az enoxaparin között.32

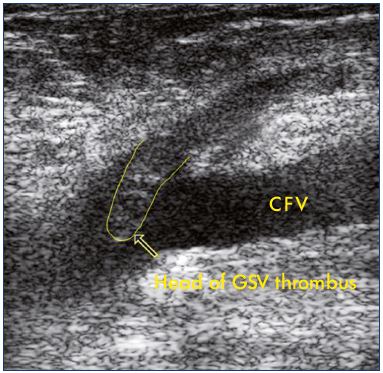
2. ábra. Ultrahang a
nagy saphena véna trombózisának a közös femorális vénába történő kiterjesztéséről.
rövidítések: CFV, common femoral vein; GSV, great saphenous vein
3. ábra. A saphenofemorális csomópont trombózisa.
Kép jóvoltából Dr. Nicolini.

a gyakorlatban a legtöbb szakértő azt javasolja, hogy az SFJ-ben vagy az SPJ-ben kiterjesztett SVT-ben szenvedő betegeket antikoaguláns terápiával kezeljék terápiás dózisokban 3 hónapig.
következtetés
SVT már nem tekinthető jóindulatú betegségnek. A közelmúltban végzett epidemiológiai vizsgálatok, amelyekben nagyszámú beteg vett részt, kimutatták az SVT-k lehetséges súlyosságát, és egyértelműen meghatározták helyüket a VTE-betegségekben. Az egyidejű DVT-t a betegek 25-30% – ánál, a PE-t pedig a betegek 4-7% – ánál azonosították. Következésképpen minden SVT-ben szenvedő betegnek kétoldalú duplex szkenneléssel kell rendelkeznie az SVT diagnózisának megerősítésére, az SVT pontos helyének és mértékének meghatározására, valamint a DVT jelenlétének diagnosztizálására vagy kizárására. Ma az SVT kezelése megváltozott, az antikoaguláns terápiát széles körben alkalmazzák az NSAID-ok helyett. A CALISTO közelmúltbeli vizsgálatáig egyetlen antikoaguláns protokoll sem mutatott egyértelmű klinikai előnyt. Az ajánlásokat azután frissítették, hogy a CALISTO-vizsgálat validálta a napi 2, 5 mg fondaparinux 45 napon alapuló antikoaguláns terápiás protokollt. Azoknál a betegeknél, akiknél a lábak tüneti SVT-je legalább 5 cm hosszú, a fondaparinux vagy az alacsony molekulatömegű heparin profilaktikus dózisa 45 napig ajánlott antikoaguláns kezelés nélkül (2b fokozat). Ha a fondaparinux-kezelés költsége elfogadható, naponta 2,5 mg fondaparinux alkalmazása ajánlott alacsony molekulatömegű heparin profilaktikus dózisánál (2C fokozat). Az ajánlások és iránymutatások azonban alacsony színvonalúak, és továbbra is kérdések merülnek fel az SVT irányításával kapcsolatban. A VTE későbbi kialakulásának néhány kockázati tényezőjét azonosították, de további kutatásokra van szükség annak érdekében, hogy egyértelműen meghatározzuk azon betegek alcsoportjait, akiknél az SVT után nagyobb a VTE előfordulása.

1. D ecousus H, Prandoni P, Mismetti P, et al; CALISTO tanulmányozócsoport. Fondaparinux felületes vénás trombózis kezelésére a lábakban. N Engl J Med. 2010;363:1222-1232.
2. Frappé P, Buchmuller-Cordier A, Bertoletti L, et al; STEPH Study Group. Az alsó végtagok felületes vénás trombózisának éves diagnózisa: a STEPH közösségi alapú tanulmány. J Thromb Haemost. 2014;12:831-838.
3. Oger E; EPI-GETBO tanulmányozócsoport. A vénás thromboembolia előfordulása: közösségi alapú vizsgálat Nyugat-Franciaországban. Thrombos Haemost. 2000;83:657- 660.
4. D ecousus H, Quéré I, Presles E, et al; POST Study Group. Felületes vénás trombózis és vénás thromboembolia: nagy, prospektív epidemiológiai vizsgálat. Ann Gyakornok Orvos. 2010;152:218-224.
5. G alanaud JP, Genty C, Sevestre MA, et al; OPTIMEV SFMV nyomozók. Felületes vénás trombózis esetén a mélyvein-trombózis és a tünetekkel járó vénás thromboemboliás kiújulás prediktív tényezői. Thrombos Haemost. 2011;105:31-39.
6. Lutter KS, Kerr TM, Roedersheimer R, Lohr JM, Sampson MG, Cranley JJ. Felületes thrombophlebitis diagnosztizált duplex szkennelés. Műtét. 1991;100:42-46.
7. Barrelier MT. Thromboses veineuses superficielles des membres inférieurs . Tényleges Vasc Int. 1993;17:7-9.
8. Jorgensen JO, Hanel KC, Mogan AM, Hunt JM. A mélyvénás trombózis előfordulása az alsó végtagok felületes thrombophlebitisében szenvedő betegeknél. Jávor Benedek 1993;18: 70-73.
9. Bilancini S, Lucchi M. Les thromboses veineuses superficielles sont-elles polymorfes ? Phlébologie. 1999;52:41-43.
10. G illet JL, Perrin M, Cayman R. az alsó végtagok felszíni vénás trombózisa: prospektív elemzés 100 betegben . J Mal Vasc. 2001;26:16-22.
11. Kalodiki E, Stvrtinova V, Allegra C, et al. Felületes vénás trombózis: konszenzus nyilatkozat. Int Angiol. 2012;31:203-216.
12. Nicolaides A. Felületes vénás trombózis a vénás thromboembolia megelőzésében és kezelésében. Int Angiol. 2013;32:237-242.
13. G illet JL, Perrin M, Cayman R. thromboemboliás kiújulás az alsó végtagok felületes thrombophlebitisét követően. J Flebológia. 2002;2:103-118.
14. D ewar C, Panpher S. a mélyvénás trombózis előfordulási gyakorisága felületes thrombophlebitisben diagnosztizált betegeknél, miután bemutatták a sürgősségi osztályon járóbeteg mélyvénás trombózis szolgáltatást. Emerg Med J. 2010;27: 758-761.
15. Quenet S, Laporte S, Décousus H, Leizorovicz A, Epinat M, Mismetti P; STENOX csoport. Az izolált felületes vénás trombózisban szenvedő betegek vénás trombotikus szövődményeinek előrejelzésére szolgáló tényezők. J. Vasc 2003;38: 944 – 949.
16. G. alanaud JP, Bosson JL, Genty C, et al. Felületes vénás trombózis és visszatérő vénás thromboembolia: két megfigyelési vizsgálat összevont elemzése. J Thromb Haemost. 2012;10:1004-1011.
17. Cosmi B, Filippini M, Campana F, et al; STEFLUX nyomozók. A SteFlux randomizált klinikai vizsgálatban (felületes thromboembolia Fluxum) a felületes vénás trombózisban szenvedő betegek recidiváló eseményeinek kockázati tényezői. Thromb Res. 2014;133: 196-202.
18. G orty s, Patton-Adkins J, DaLanno M, Starr J, Dean S, Satiani B. az alsó végtagok felszíni vénás trombózisa: kockázati tényezők elemzése, valamint a kiújulás és az antikoaguláns szerepe. Vasc Med. 2004;9:1-6.
19. G illet JL, Allaert FA, Perrin M. felületes thrombophlebitis az alsó végtagok nem varikózus vénáiban. Prospektív analízis 42 betegen . J Mal Vasc. 2004;29:263-272.
20. Martinelli I, Cattaneo M, Taioli E, De Stefano V, Chiusolo P, Mannucci PM. A felszíni vénás trombózis genetikai kockázati tényezői. Thrombos Haemost. 1999;82:1215-1217.
21. Milio G, Siragusa S, Malato a, Grimaudo S, Pinto A. felületes vénás trombózis: a természetes antikoagulánsok öröklött hiányának szerepe a mélyvénákra való kiterjesztésben. Int Angiol. 2009;28:298- 302.
22. Zollinger RW, Williams RD, Briggs DO. Problémák a thrombophlebitis diagnózisában és kezelésében. Arch Surg. 1962; 85: 34-40.
23. D ecousus H; Enoxaparin tanulmányozócsoport. Kísérleti randomizált kettős-vak összehasonlítás egy kis molekulatömegű heparinnal, egy nem szteroid gyulladáscsökkentő szerrel és placebóval a felületes vénás trombózis kezelésében. Arch Int Med. 2003;163:1657-1663.
24. Prandoni P, Tormene D, Pesavento R; Vesalio Nyomozók Csoport. Nagy vs. alacsony dózisú kis molekulatömegű heparin a lábak felületes vénás trombózisának kezelésére: kettős vak, randomizált vizsgálat. J Thromb Haemost. 2005;3:1152-1157.
25. Cosmi B, Filippini M, Tonti D, Avruscio G, Ghirarduzzi A, Bucherini E;STEFLUX. Kis molekulatömegű heparinnal (parnaparin) végzett randomizált doubleblind vizsgálat felületes vénás trombózis esetén: STEFLUX (felületes thromboembolia és Fluxum). J Thromb Haemost. 2012;10:1026-1035.
26. D ecousus H, Frappé P, Accassat S, et al. Epidemiológia, diagnózis, a lábak felületes vénás trombózisának kezelése és kezelése. Legjobb Pract Res Clin Haematol. 2012;25:275-284.
27. Kearon C, Kahn SR, Agnelli G, Goldhaber S, Raskob GE, Comerota aj; American College of Chest Physicians. Antitrombotikus terápia vénás thromboemboliás betegség: American College of Chest Physicians bizonyítékokon alapuló klinikai gyakorlat iránymutatások (8. kiadás). Mellkas. 2008;133(suppl 6): 454S-545S.
28. Kearon C, Akl EA, Comerota aj, et al; American College of Chest orvosok. Antitrombotikus terápia VTE-betegség esetén: Antitrombotikus terápia és trombózis megelőzése, 9th ed: American College of Chest Physicians bizonyítékokon alapuló klinikai gyakorlat iránymutatások. Mellkas. 2012;141 (suppl 2): e419S-e494S.
29. D I Nisio M, Wichers IM, Middeldorp S. a láb felületes thrombophlebitisének kezelése. Cochrane adatbázis Syst Rev. 2013;30; 4: CD004982.
30. D I Nisio M, Middeldorp S. az alsó végtag felületes thrombophlebitis kezelése. JAMA. 2014;311:729- 730.
31. Sullivan V, Denk PM, Sonnad SS, Eagleton MJ, Wakefield TW. Ligáció kontra antikoaguláns: a térd feletti felületes thrombophlebitis kezelése, amely nem érinti a mélyvénás rendszert. J Am Coll Surg. 2001;193: 556-562.
32. Lozano FS, Almazan A. alacsony molekulatömegű heparin versus saphenofemoral leválasztás a térd feletti nagyobb saphena thrombophlebitis kezelésére: prospektív vizsgálat. Vasc Endovaszkuláris Surg. 2003;37: 415 – 420.
33. Chengelis DL, Bendick PJ, Glover JL, Brown OW, Ranval TJ. A felületes vénás trombózis progressziója mélyvénás trombózisra. J. Vasc 1996;24: 745-749.
34. Hingorani A, Ascher E. felületes vénás thrombophlebitis. A: Gloviczki P., Szerk. A vénás rendellenességek kézikönyve. Az amerikai vénás fórum irányelvei. 3. Szerk. London, Egyesült Királyság: Hodder Arnold; 2009: 314-319.
Leave a Reply