oxálsav
Meera Senthilingam
Ezen a héten Franciaországba indulunk, és felfedezünk egy olyan vegyületet, amely befolyásolta egy nagyon jól ismert parancsnok egészségét
Lars Öhrström
1870 szeptember elseje komor nap volt Charles Louis Napoléon Bonaparte számára. A belga határhoz közeli kis francia városban, Sedanban a francia hadsereg parancsnoka, Patrice de Mac-Mahon megsebesült, és a beteg és gyenge császárnak, más néven III. Napoléonnak meg kellett adnia magát, és feladnia magát fogolyként a fékezhetetlen porosz duónak, von Moltke – nak és Bismarcknak. Tehát az 1870-es háború elveszett, és Európa hatalmi egyensúlya jelentősen kelet felé fordult, és mindannyian tudjuk, hogy ez hogyan végződött.

Forrás: ©
Sedan, Franciaország
ez az egész, mert a nagy kristályos betétek a kalcium-oxalát, hogy volt-ben alakult Napóleon vese? Valószínűleg nem: úgy tűnik, hogy a háború a porosz technikai és szervezeti fölény miatt veszett el.
A császár azonban nem nagyon szeretett fegyvert felvenni, néhány tanácsadójával, a fő melegítőkkel. Nehéz tudni, hogy mennyire képes ellenállni és ellensúlyozni őket, miközben a vesekövek néven ismert nagyon fájdalmas állapot sújtja őket.
könnyebb a vesekövekhez fordulni, mert ezek érzékenyek a tudományos kihallgatás részletes módszereire, például a röntgendiffrakcióra. Két egyszerű komponens, a pozitív kalciumionok, a Ca2+ és a negatív oxalátionok alkotják őket,így egy olyan vegyület, amely egyszerűen csak kalcium-oxalátként ismert.
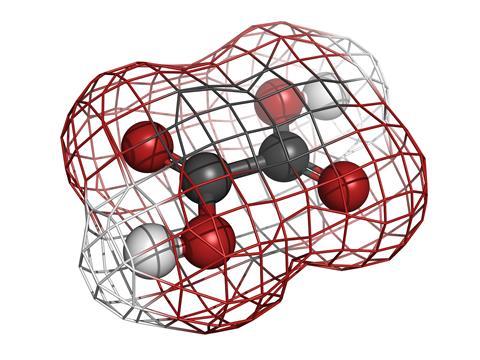
a podcast témája az oxálsav, az oxalát anionok pedig a H+ ionokkal együtt, amikor ennek az erős savnak a kristályait vízben oldjuk fel. Az oxálsav egy kis molekula, amelynek képlete C2O4H2, de talán jobb, mint a HOOC-egykötésű-COOH: csak két karbonsav-csoport csatlakozott egymáshoz, hogy ez a legegyszerűbb szerves di-sav. Lehet, hogy ezt a vegyületet, mint a vegyület, ami rebarbara van, hogy a különleges savas tang az íze, de ez is megtalálható a spenót és számos más zöldségeket, hogy a legtöbben boldogan enni. Ez is része a normális anyagcsere fordul elő teljesen természetes a testünkben.
forrás: ©
egy növényről, a közönséges erdei szalonnáról, egy kis növényről kapta a nevét, amelynek levelei külön savas ízűek, újjáélednek, ha elvesznek az erdőben, és a Latin neve Oxalis acetosella.
ennek a kis molekulának a legjellemzőbb jellemzője az alakja. Úgy néz ki, egy kicsit, mint két Y rakott össze átfedő bázisok. A szénatomok a két kereszteződésnél vannak, az oxigénatomok pedig a négy végén, a protonok (vagy H + ionok) pedig egyenként lógnak ezen oxigéneken. Sőt, teljesen lapos, és amikor elvesztette protonjait, hogy oxalát anionmá váljon, mínusz töltései vannak két oxigénatomján.
az oxálsav legtöbb technikai alkalmazása a laposságán és a negatív töltésen függ, ahogy Napoléon veseproblémái is. A Sedan-i csata során von Moltke klasszikus csipeszmozgalommal sikeresen elfoglalta a francia hadsereget, két oldalról támadva, nem pedig középen. Ugyanígy az oxalátionoknak két elektronpárja van az egyes negatív oxigénatomokon, amelyek két oldalról könnyen megtámadnak minden olyan fémionot, amely az útjába kerül. Csakúgy, mint a szedánban, több oxalátion fog követni, a fém körül két, három vagy négy oxalát ionnal, méretétől függően.
Ez a hatás a nem kívánt vasvegyületek, különösen a rozsda eltávolítására használható konyhai edényekből, sőt márványból is. Mivel a tisztítószerek, oxálsav vagy oxalátok számos technikai tisztítószer összetevői, ezek az oldatok mind azon a feltételezésen alapulnak, hogy a képződött fém-oxalátvegyületek vízben oldódnak, így könnyen lemoshatók.

forrás: ©
nem annyira kalcium-oxalát. A pozitív kalciumionok valóban szeretik a negatív oxalát oxigénatomokat, és olyan mértékben, hogy nem érdekli őket, ha az oxalát oxigénatomok negatív töltést hordoznak-e vagy sem. Tehát nem csak egy fogaskerék-mozgás lesz előre egy kalcium-ion felé, hanem visszafelé is, egy másikhoz rögzítve ebben az irányban. Mint minden kalcium ion meglehetősen nagy, négy-oxalát ionok össze körül minden fém ion (ahhoz képest, hogy három vas), minden kapcsolódó két másik kalcium ionok a másik irányba. Ily módon a kalcium-oxalát végtelen hálózatgá alakul, amely vízben teljesen oldhatatlan lesz. Ahogy egyre több kalciumion és oxalátion halad át a vesén, a kristályok növekedni fognak, amíg az állapot nagyon fájdalmas lesz.
de ne ijedjen meg, eltekintve néhány nagyon különleges egészségügyi körülmények között, a normális, vagy akár magas, bevitel kalciumionok és oxálsav természetes forrásokból nem úgy tűnik, hogy növeli a vesekő.
az oxalátok oldhatatlansága szintén hasznosnak bizonyul a technológiában. A ritkaföldfémek, vagyis a lantanoidok egyre fontosabbá válnak számos technikai alkalmazásban. Gyakran az első szakaszban a feldolgozás, finomítás, miután a kezdeti kimosódás az ércek, hogy kicsapjuk ezeket az elemeket, mint a oxalátok, mert mint a kalcium-oxalát nagyon oldhatatlan.
kivéve a szerencsétlen találkozás kalcium-oxalát, Napoléon III ismert, a kémia, történelem, mint a felbujtó, a margarin fejlesztési, valamint szorgalmazza egy olcsó, praktikus módszer, hogy a gyártás alumínium ipari méretű, a-szor, a legértékesebb fém. Nem látta ezt a későbbi célt elérni, de figyelemre méltó, hogy a sok fájdalmat okozó vegyszert, az oxálsavat is használják a kemény, kopás – és korrózióálló oxidréteg, más néven eloxált bevonat készítéséhez és színezéséhez, amely ma már olyan fontos az alumínium számos alkalmazásában.
Meera Senthilingam
tehát az egészségügy és az ipar összefogott. Ez volt Lars Öhrström a Chalmers Tekniska Högskola Svédországban hozza meg a vese gyengítő kémia oxálsav. A jövő héten Lars visszatér egy olyan vegyülettel, amely teljes mértékben képes megvédeni magát.
Lars Öhrström
nem világos, hogy mikor készült először a ferrocén, de úgy tűnik, hogy az 1940-es évek végén “sárga iszapként” vették fel a csöveket egy Union Carbide crackernél ellenőrző folyamattechnikusok, amelyet a diciklopentadiénből származó kis szénhidrogén-ciklopentadién előállításához használtak.
Ez elég nagy felfordulást okozott, mivel korábban nem ismert egyetlen, csak szénhidrogénből és átmeneti fémből álló stabil molekula sem, és ezt a vegyületet szobahőmérsékleten, spontán meggyulladás nélkül lehetett tartani. Azt is túlélte találkozó ilyen hírhedt gyilkosok fémorganikus molekulák, mint a víz, savak vagy bázisok.
Meera Senthilingam
és fedezze fel a kémia, amely lehetővé teszi ezt a jövő heti kémia elemében. Addig is köszönöm a hallgatást, Meera Senthilingam vagyok
Leave a Reply