melyik a leginkább reaktív elem a periódusos rendszerben?
a fluort a periódusos rendszer legreaktívabb és legelektronegatívabb elemeként azonosítják, így a legerősebb oxidálószer. A cézium a leginkább reaktív fém a periódusos rendszerben, annyira, hogy ezzel a fémmel való munka gyakran robbanásokkal végződik!
mit mondott az egyik kémikus a másiknak, amikor sértettnek találta? “Miért vagy szomorú? Szerintem túlreagálod!”Látod, mit csináltam ott? Néha azon tűnődöm, hogy miért-a vidámságom ellenére-nagyon nehéz barátokat szerezni …
egyébként, a szegény osztályokon kívül, az első dolog, ami eszembe jut, amikor a kémiára gondolok, laboratóriumi kabátok, furcsa alakú edények, mintha a karneváli tükrök visszaverődése, és lángoló robbanások. Hébe-hóba, valaki motyogja “reakció” vagy “reaktivitás”, kifejezések olyan mindenütt jelen van, hogy megtalálja őket beszivárgó kémia könyvek az utolsó oldalon. Pontosan ez az, amivel most foglalkozunk.

mentes minden technikai zsargon, a” reakció ” pontosan mit jelent, a válasz. A reaktivitás viszont meghatározható annak mértékeként, hogy egy kémiai faj milyen könnyen vesz részt egy reakcióban, és milyen kémiai kötéseket képez. Tehát a kérdés válik-melyik elem a legkönnyebb? De először …
mi határozza meg egy elem reaktivitását?
egyszerű szavakkal, a kémiai reakció tökéletes lehetőség a vásárlók és az eladók számára áruk vásárlására és eladására. A vevők és az eladók kémiai elemek. Az áruk elektronok, a pénznem pedig energia.
e kereskedelem célja a stabilitás, az elektronok optimális konfigurációjának elérése, amely akkor érhető el, ha egy elem valenciája (legkülső) héja teljesen kitöltött vagy kiürült. Alapvetően egy elem több elektront vásárolhat, hogy kitöltse az utolsó előtti héját, vagy eladja őket, hogy ürítse ki.

minél kevesebb elektron vesz részt, annál kisebb az energiaköltség. Bárki, aki ismeri a természet parsimonious működési módját, kitalálja, hogy a legkevesebb energiát igénylő kereskedések azok, amelyek valószínűleg előfordulnak. Ennek van értelme, mivel egy elem inkább elveszíti az elektronokat, és üressé teszi magát, ha a legkülső héja kevesebb, mint félig töltött, vagy nyerhet néhányat, hogy kitöltse magát, ha több mint félig töltött. Vásárlás hat, ha egyszerűen elveszíti két lenne egyenesen ostoba, de ami még fontosabb, drága!
így a reaktivitás annak a függvénye, hogy egy elem milyen könnyen veszít vagy nyer elektronokat.
hogyan becsüljük meg egy elem ösztönzőit?
A periódusos rendszer és annak”trendjei”
hogyan deríthetjük ki, hogy egy elem vevő vagy eladó? A periódusos rendszerre utalunk.
a periódusos rendszer emlékeztet arra,hogy a tudósok határvonalas OCD, és nem tud segíteni, de mindent rendkívül rendezett és rendezett módon szervez. A periódusos rendszer minden általunk ismert elemet összevont módon szervez.
a táblázat az elemeket atomszámuk szerint rendezi, ami megegyezik az általuk felölelt protonok vagy elektronok számával. (Nem furcsa, hogy általában pontosan ugyanazok?)
Trend 1
száma elektronok a valence shell eggyel nő, mint tudjuk értelmezni keresztül minden elem a sorban, bár a lövedékek száma nem marad ugyanaz. A héjak száma levonható a sorszámból. Például a második sor minden eleme csak két héjat tartalmaz, stb.
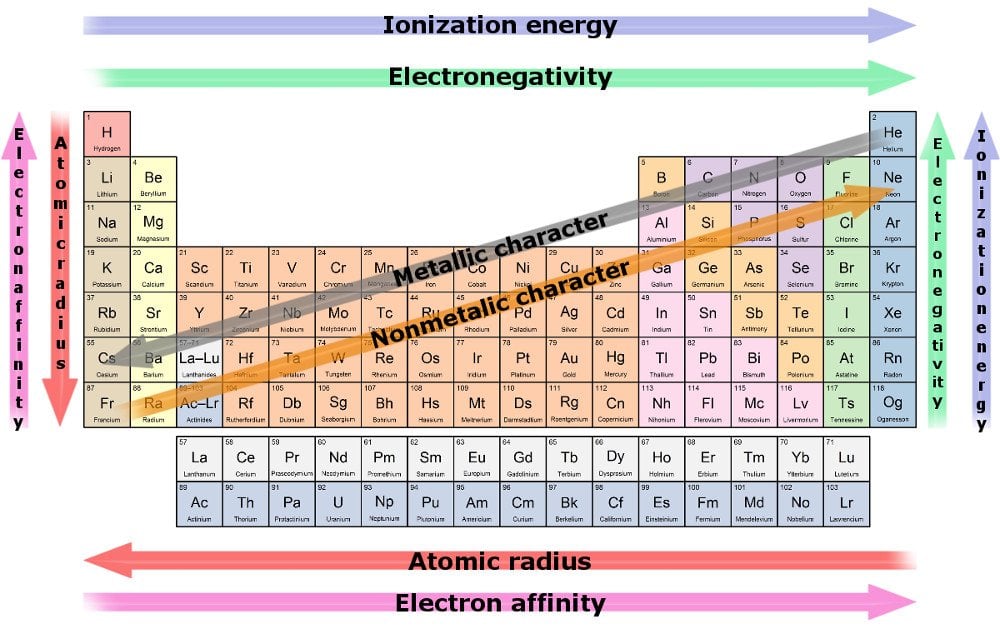
ennek a tendenciának az a következménye, hogy az atomsugár csökken, Amikor egy sor utolsó lakója felé haladunk. Ennek oka az, hogy az elektronok növekedését tükrözi a protonok növekedése a központban, míg az előbbinek ugyanabba a héjba kell tömörülnie. A húzó protonok és a növelő elektronok közötti tug-o’-háborúban az előbbi nyer, ami nagyobb nukleáris vonzerőt eredményez, minden héját közelebb húzva hozzá.
ezért a vonzás erős húzása miatt egy elem nagyobb valószínűséggel vásárol vagy szerez elektronokat, amikor egy sor mentén haladunk. Az intézkedés egy elem azon képességét, hogy húzza elektronok felé ismert Elektronegativitás. A legtöbb elektro-negatív elem az elektronok ellopása és a leggyorsabb reakció.
Trend 2
egy másik trend az elemek sugárának növekedése, amikor egy oszlopon lefelé haladunk, míg a valence elektronok száma változatlan marad, annak ellenére, hogy az atomszám folyamatosan növekszik. Ennek oka az, hogy az elektronok növekedését a héjak növekedése párhuzamosítja. A nehézfémeknek nagyobb a sugara, különösen a legmagasabb alján. Ezek szemléltetik a legszegényebb nukleáris vonzerőt, következésképpen rosszul tartják a legkülső elektronokat.

az elem elektronok elvesztésének képességének mérését elektro-pozitivitásnak nevezik, és növekszik, amikor egy oszlopon lefelé haladunk. Ismét a leginkább elektropozitív elem az, amely valószínűleg feladja elektronjait, és a leggyorsabban reagál.
most, hogy ismerjük a szabályokat, fedjük fel a nyerteseket.
A legtöbb reaktív nemfém-fluor
A fluor a halogéncsoport első eleme. Halványsárga, diatómiás, erősen korrozív, tűzveszélyes gáz, csípős szaggal. Atomszáma 9, vegyértékhéjában 7 elektron található. Sőt, a második sorban lakik, ami azt jelenti, hogy minden 9 elektronja valahogy csak 2 héjba van zsúfolva.
a 7-elektron valence héj megköveteli, hogy csak egyetlen elektront nyerjen a végső héj befejezéséhez és a stabilitás eléréséhez, ami nem nagy bravúr, ha figyelembe vesszük annak kis méretét és erőteljes nukleáris húzását. A fluort a periódusos rendszer legelektronegatívabb elemeként azonosítják, így a legerősebb oxidálószer. Ez a leginkább reaktív nem fém.

A fluor annyira reaktív, hogy olyan anyagokat égethet, amelyeket általában nem gyúlékonynak tartanak! Meg lehet égetni üveg, víz, sőt homok! Promiszkuitása lehetetlenné teszi a legtisztább formában történő tárolását vagy elszigetelését. Vad reaktivitása miatt korai elszigetelődése és kísérletezése halálos balesetekkel teli. Igen … végzetes.
A legtöbb reaktív fém – cézium
a cézium egy arany színű fém, amely robbanásszerűen reagál levegővel és vízzel. Atomszáma 55. A cézium az első oszlopban, a második az utolsó sorban található. Mint már említettük, az oszlopban olyan alacsony elem sugara elég nagy a fenti elemekhez képest.

(fotó hitel : Dnn87 / Wikimedia Commons)
a nagy sugár hatástalanná teszi a nukleáris húzását, és borzasztóan ügyetlenné teszi. Nagy mérete miatt nagyon érzékeny az ionizációra. Nagyon acquiescent, és könnyen feladja az egyetlen elektron a valence shell, hogy elérje a stabilitást, így nagyon reaktív. A cézium a leginkább reaktív fém a periódusos rendszerben, annyira, hogy ezzel a fémmel való munka gyakran robbanásokkal végződik!
Francium
a Francium az első oszlop utolsó eleme, közvetlenül a cézium alatt ülve, így az oszlop legnagyobb atomja. Logikusan arra következtethetünk, hogy a Franciumnak nagyobb reaktivitással kell rendelkeznie a Céziumhoz képest, de ez nem így van.
becslések szerint a földkéregben egyszerre legfeljebb egy uncia van. Mivel természetesen annyira ritka, a tudósoknak elő kell állítaniuk, hogy tanulmányozzák.

(fotó hitel : MarlonMarin1 / Wikimedia Commons)
azonban, még akkor is, ha valahogy elszigetelt, nem tart sokáig. Francium radioaktív jellegű, amelynek felezési ideje mindössze 22 perc, így bomlik, mielőtt kap egy esélyt, hogy reagáljon! Ráadásul oly sok proton jelenléte miatt az elektronok hihetetlenül nagy sebességgel mozognak. Ahogy Einstein rájött, olyan kicsi skálán és olyan nagy sebességgel, furcsa dolgok kezdenek bekövetkezni — az elektronok egy kicsit közelebb kerülnek a maghoz, mint amire logikusan számíthatunk, így kissé nehezebbé válnak megszabadulni.
tehát úgy tűnik, hogy a francia a leginkább reaktív elem, sajnos elméletileg.
Spoiler figyelmeztetés!
lehet, hogy észrevette, hogy a leginkább reaktív két elem csak az adott kategóriájukban nyertesek — fémek és nemfémek. Sajnálom, hogy buzzkill vagyok, de nincs végleges válasz arra, hogy ki a leginkább reaktív elem-az összes között, mert kettőre van szükség a tangóhoz.
meg lehet kérdezni, hogy melyik elem a leginkább reaktív a nátriummal? A válasz tehát fluor, nem cézium. Vagy talán szeretné tudni, hogy melyik elem a leginkább reakcióképes a nitrogénnel. Lítium! Sokkoló!
a reaktivitás kifejezést gyakran tévesen értelmezik. A kérdés kétértelmű, és némileg hiányos, ahogy ez a cikk remélhetőleg mutatja.
Leave a Reply