Kemoterápiás Extravasációk kezelése
US Pharm. 2009;34(9)(onkológiai suppl):3-11.
absztrakt: az intravénás (IV) kemoterápiás gyógyszerek extravasációs sérülést vagy szöveti nekrózist okozhatnak az alkalmazás helyén. Bár az extravasációk többsége megfelelő és alapos infúzióval megelőzhető, számos antidotumot elismertek és vizsgáltak a további szöveti sérülések megelőzése érdekében.
az infiltráció és az extravasáció az IV infúziós kezelés két jól ismert, különálló szövődménye. Az infúziós ápolók társasága és az onkológiai ápolási Társaság szerint mindkét szövődmény magában foglalja a IV oldat véletlen szivárgását a környező szövetekbe; azonban az oldat típusa különbözik. Az infiltráció egy nem vézikus vagy irritáló oldat vagy gyógyszer véletlen beadása a környező szövetekbe.1,2 Nonvesicants olyan szerek, amelyek ritkán termelnek akut reakciókat, vagy elpusztítják a szövetet, amikor beszivárognak. Az irritáló szerek fájdalmat okozhatnak az injekció beadásának helyén vagy a véna mentén, gyulladásos reakcióval vagy anélkül, általában tartós szövetkárosodás nélkül. Az irritáló szerek azonban csak akkor okozhatnak lágyszöveti fekélyeket, ha nagy mennyiségű koncentrált gyógyszeroldatot véletlenül extravasálnak gyulladásos reakciók kiváltására, tartós szövetkárosodás nélkül.3,4
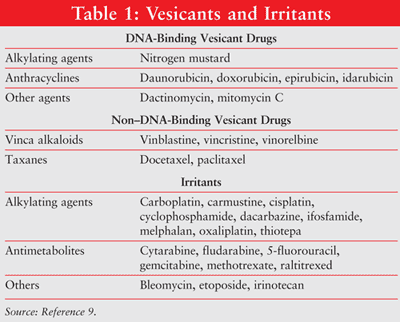
az extravasáció a vesicant anyag véletlen beinjektálására vagy szivárgására utal a perivascularis és subcutan terekbe a gyógyszeres kezelés során.1,2 az extravasáció helyi reakciókat eredményez, a helyi irritációtól a bőr súlyos szöveti nekrózisáig, a környező érrendszerig és a tartószerkezetekig.5-8 kemoterápiás szerek sorolhatók, alapján a potenciális okozhat helyi szöveti sérülés, mint vesicants, irritáló, vagy nemvesicants. (Az 1.9. táblázat számos vesicant és irritáló anyagot vázol fel) az IV-es gyógyszerek véletlen extravasációja a perifériás IV-es infúziók körülbelül 0,1-6% – ában, az implantált vénás hozzáférési port infúziók 0,3-4,7% – ában fordul elő.10-12
A szövetkárosodás patofiziológiája
a szövetkárosodás mértéke a kemoterápiás szer DNS-hez való kötődési képességétől függ. A DNS-kötő szerek közé tartoznak az antraciklinek, tumorellenes antibiotikumok, platina analógok és néhány alkiláló szer.3,4 a DNS-kötő daganatellenes szerek szövetkárosodást okoznak a szabad gyökök által okozott halálos DNS-térhálósodás vagy száltörések szaporításával, amelyek sejt apoptózishoz vezetnek.13-17 nem DNS-kötő daganatellenes szerek (pl., a vinka alkaloidok, taxánok, topoizomeráz inhibitorok) zavarják a mitózist. A nem DNS-kötő szerek könnyebben eltávolíthatók az extravasációs helyekről, és kevesebb szövetkárosodást okoznak, mint a DNS–kötő szerek.17
extravasatio kockázati tényezői
az extravasatio kockázata multifaktoriális, és nagymértékben módosítható. E kockázatok közül sok az eszközhasználat és az elhelyezés hibáiból ered. IV eszköz tényezők, amelyek befolyásolják extravasation kockázat közé tű anyag (azaz, fém), kanül mérete (nagy műanyag vs kis műanyag), és katéter típusa (azaz, központi vénás katéter ). A fém tűk nagyobb károsodást okozhatnak a behelyezéskor, és rugalmatlanok az edényben, míg a nagy méretű tűk akadályozhatják a véráramlást, lassítva az infusate hígítását.18,19 Extravasatio a CVCs akkor fordulhat elő, tűvel elmozdulás a beültetett vénás port (IVAP), mechanikus elzáródás, valamint az azt követő CVC kár, katéter migráció, vagy a fibrin ujja kialakulását, illetve trombózis. Az IVAP helytelen elhelyezése nagyobb valószínűséggel fordul elő új eszközökkel, jelentős posztoperatív duzzanattal rendelkező betegeknél, elhízott betegeknél vagy nagy mellű nőknél.20 mechanikus elzáródás oka lehet a trombusképződés, a gyógyszer kicsapódása, a retrográd katéter elmozdulása vagy a csipet-off (azaz szakaszos és pozicionális katéter elzáródás; gyanítható, hogy az infúziós elzáródás enyhíthető-e azáltal, hogy a beteg mozgatja a karját).2,21,22 az extravasáció elkerülése nagymértékben függ a IV. hely megfelelő karbantartásától és az infúzió megfelelő sebességének biztosításától. Ezek a kockázati tényezők az alkalmazott daganatellenes szerekkel, a betegekkel és a gyógyszert kezelő klinikusokkal kapcsolatosak.
prevenció
a betegek szoros ellenőrzése, valamint mind a betegek, mind a szakemberek oktatása a vesicant extravasation kockázatairól és kezeléséről úgy tűnik, hogy a megelőzés sarokköve. Míg az orvosok felelősek a pontos megrendelések megírásáért, addig az ápolók feladata az eszközök szakképzett és megfelelő elhelyezésének biztosítása, valamint a kemoterápiás infúziók vizuális és beteginterjúkon keresztüli monitorozása. A vesicant alkalmazása során a helyszínen ellenőrizni kell a duzzanatot, a vörösséget és a fájdalmat. A vezikánsokat a gyártók ajánlásainak megfelelően kell beadni (pl. megfelelő hígítás, meghatározott beadási idő). Az IV sorokat a kemoterápia alkalmazása előtt és után ki kell öblíteni. A gyógyszerész feladata az lenne, hogy segítsen olyan politikák kidolgozásában, amelyek biztosítják a kemoterápiás szerek megfelelő ellenőrzését, címkézését és adagolását. Ennek egyik módja az, hogy diszkriminatív címkézést alkalmazzunk a vesicant antineoplastics adagolásakor, hogy az ápolók megfelelő óvintézkedéseket alkalmazzanak. A gyógyszerészek szerves szerepet játszhatnak az oktatásban azáltal, hogy a különböző kemoterápiás szerek megfelelő használatáról és alkalmazásáról gyógyszerinformációkat és rutinszerű szolgáltatásokat nyújtanak az egészségügyi csoport minden tagjának. A biztonságos gyakorlatok végrehajtása érdekében multidiszciplináris együttműködési megközelítést kell alkalmazni. A kemoterápia alkalmazása betegeknél a személyzet megfelelő képzését és a betegek oktatását, valamint a szakpolitika végrehajtása révén történő adminisztratív támogatást igényel.2,23
események dokumentálása
minden extravasációs esetet alaposan dokumentálni kell és jelenteni kell. A dokumentáció több célt szolgál, többek között pontos beszámolót nyújt a történtekről, védi az érintett egészségügyi szakembereket, információkat gyűjt az extravasációkról, és kiemeli a gyakorlati hiányosságokat.23 a gyógyszerészek egy másik módja annak, hogy megelőzzék a jövőbeli eseményeket, a gyógyszerészek dokumentálják és beszámolják a gyógyszermellékhatások és a gyógyszermellékhatások megfelelő szervezeteinek. A jelentett gyógyszermellékhatások és gyógyszerhibák alapján összegyűjtött adatok tanulási eszközként használhatók arra, hogy rendszeresen megvizsgálják, milyen eszközökkel fordulnak elő ezek az események. A helyi eljárások és protokollok elengedhetetlenek az extravasáció időben történő felismeréséhez és kezeléséhez, valamint a súlyos szövetkárosodás megelőzéséhez. Együttműködési erőfeszítéseket kell tenni annak érdekében, hogy az esemény bekövetkezése után időben multidiszciplináris kísérleteket hajtsanak végre a betegek kezelésében részt vevő egészségügyi csoport minden tagjának oktatására. További erőfeszítéseket kell tenni olyan politikák kezdeményezésére, amelyek megakadályozzák a további eseményeket. Amennyiben a szakpolitikák megvalósulnak, azokat a jelenlegi gyakorlat tükrözése érdekében azonnal elérhetővé kell tenni és rendszeresen frissíteni kell. A European Oncology Nursing Society (EONS) 2007 extravasation guidelines nyújt javasolt adatok és sablonok, hogy lehet használni, hogy információkat gyűjtsön abban az esetben, ha az ügy.23
Tünetei Extravasatio
tünetei hólyagképző extravasatio tartalmazza duzzanat, bőrpír és/vagy kellemetlen érzés, hogy gyakran úgy jellemzik, mint égő vagy szúró. Ellenállás során drug administration, lassú vagy lassú infúzió, illetve hiánya vagy elvesztése a vér vissza a IV. kanül, a beültetett kikötő, vagy más központi vénás eszköz lehet mutatók hólyagképző extravasatio történik.23 az elszíneződés és a bőr elszíneződése tovább fejlődhet a hólyagok vagy nekrózis, esetleg fekély és mélyszöveti sérülés kialakulásával. Több napig is eltarthat, amíg az epitheliális károsodás teljes mértékben megvalósul.
kemoterápia által kiváltott extravasatio kezelése
a vesicant extravasatio kezelésére alkalmazott kezelési módok közé tartozik a kemoterápia azonnali abbahagyása, valamint az extravasatio helyének hűtése vagy hígítása. Az extravasációval járó morbiditás csökkentése érdekében elengedhetetlen, hogy a klinikusok jól tájékozódjanak a rendelkezésre álló kezelésekről, és gyorsan dolgozzanak a további betegkárosodás elkerülése érdekében. A Nem vényköteles extravasáció kezelése jellemzően magában foglalja a végtag emelését és a hűtést, és általában nem foglalja magában a farmakológiai terápia alkalmazását.23
A Vesicant Extravasation kezdeti kezelése
a korai beavatkozás megkönnyítését megkönnyítheti az intézményen belüli extravasációs készlet rendelkezésre bocsátása. A legtöbb extravasációs készlet tartalmaz eldobható fecskendőket és kanülöket, hideg – meleg csomagokat, gézpárnákat, tapadó vakolatot, steril és védőkesztyűt, valamint extravasáció kezelésére szolgáló gyógyszereket (pl. hialuronidáz, dimetil-szulfoxid 99%, dexrazoxán). A készlet tartalmának listáját a készletbe kell helyezni, és a gyógyszer tartalmának rendszeres ellenőrzését a frissített lejárati dátumokkal rendszeresen a gyógyszerésznek kell fenntartania.2
Egyszer hólyagképző extravasatio jelentkezik, az orvos, azonnal hagyja abba a infúzió; azonban a kanül vagy noncoring port tűt kell tartani, ahol egy kísérlet arra, hogy szívja le a hólyagképző egy 10 mL-es fecskendő kell tenni. Az extravasációs területet fel kell tüntetni és le kell fényképezni; ezután a kanül vagy a tű eltávolításra kerül, és értesíteni kell az orvost. A betegek fájdalomcsillapítók használatát igényelhetik az általuk tapasztalt fájdalom kezelésére. A kezdeti intézkedések meghozatala után nagyon fontos, hogy alaposan dokumentáljuk a mellékhatások és / vagy a gyógyszeres kezelés hibáját.23
a vinca alkaloidok esetében, ahol a vesicant diszpergálódását vagy hígítását jelzik, 20 percig, napi 4 alkalommal, 1 napig, 2 napig helyi hőt kell alkalmazni. Más hólyagképző extravasations, beleértve az antraciklinek, kezdeti kezelés felé irányul honosítása, illetve semlegesíti a extravasated ügynök hideg borogatást 20 perc naponta 4-szer, 1-2 nap, korlátozza a sejtek felvétele ezek a szerek.23
farmakológiai kezelés
DMSO: a DMSO egy közös oldószer, amely behatol a szövetekbe és fokozza a bőr permeabilitását, ami elősegítheti az extravasált gyógyszer felszívódását. Helyileg alkalmazva szabadgyök-eltávolító / antioxidáns tulajdonságokkal rendelkezik, amelyek felgyorsíthatják az extravasált gyógyszer eltávolítását. A DMSO (Rimso-50) csak az Egyesült Államokban történő kiskereskedelmi vásárláshoz érhető el 50% (vol/vol) vízben. Ezt a megoldást az FDA csak a visszatérő interstitialis cystitis kezelésére hagyta jóvá.24 a DMSO hatásosságát a kemoterápiás extravasáció kezelésére először több esettanulmányban és kis klinikai vizsgálatokban írták le.
egy esetben egy 42 éves férfi 10 mg daunorubicin extravasációját nátrium-hidrogén-karbonáttal, dexametazonnal (4 mg), jégcsomagolással és 1,5 mL helyi DMSO 70% – kal kezelték, amelyet 3-4 óránként 10 napig alkalmaztak. Ez a kezelés fájdalomcsillapítást és fekélymegelőzést biztosított.25
Olver és Schwarz három esetben jelentett extravasációs felbontást DMSO-val.26 egy esetben a DMSO 99% napi alkalmazása 14 napig a fájdalom teljes megszűnését eredményezte 2 napon belül, fekélyesedés nélkül doxorubicin extravasatióban szenvedő betegeknél. A beteg 8,4% – os nátrium-hidrogén-karbonátot és megfelelő nonfarmakológiai kezelést is kapott. (Lásd a 2. táblázatot a nem gyógyszertani lehetőségekről.) Egy másik esetben egy 49 éves férfit, aki 4-6 mg doxorubicint kapott, 5 mL 8-as doxorubicin extravasációjával kezeltek.4% nátrium-hidrogén-karbonát, jégcsomagok és DMSO 99% naponta 14 napig. Fekélyesedés nem fordult elő; azonban egy 3 x 2,5 cm-es indurált területkorlátozó könyökhosszabbítás történt.26 harmadik esetben a DMSO 99% helyi alkalmazása (6 óránként 1 hétig, majd naponta kétszer egy hétig) megakadályozta a fekélyt; a maradék pigmentáció azonban megmaradt.26
Berghammer et al szintén docetaxel extravasáció esetéről számolt be.27 az extravazátot normál (0,9% – os) sóoldattal hígítottuk, és jégcsomagolással kezeltük. A DMSO-t 45 percenként 3-szor alkalmazták, az extravasáció napján pedig orális kortikoszteroidokat és diklofenakot adtak. A tünetek 24 órán belül megszűntek, azonban az 5.napon késői tünetek (barna elszíneződés, bőr hyperplasia) jelentkeztek, majd ezt követően fokozódtak. Nem volt szükség műanyag sebészeti beavatkozásra. Bár a DMSO hipotermiával és izotóniás sóoldattal kombinálva nem volt hatékony a késleltetett tünetek megelőzésében, korlátozta a gyulladást és a szöveti nekrózist.
Ludwig et al arról számolt be, hogy a DMSO 90%-os és alfa-tokoferol 10% – os keverék alkalmazása az antraciklinek vagy mitomicin C extravasációit követő 48 órán belül 8 beteg esetében nem eredményezett bőrfekélyt vagy funkcionális vagy neurovaszkuláris károsodást.28 sajnos az alfa-tokoferol nem egy könnyen hozzáférhető gyógyszer, ezért további randomizált vizsgálatokat kell végezni annak alkalmazásának validálására.
egy 20 antraciklin extravasatióban szenvedő beteg bevonásával végzett prospektív vizsgálatban a DMSO-t 99% – uk 2 héten át naponta kétszer, 6-szor adta be.29 a DMSO-kezelést követően nem írtak le fekélyeket, bár a kezdeti duzzanat (85%), erythema (75%) és fájdalom (60%) nyilvánvaló volt. 16 beteg 3 hónapos követési periódusa után 6 betegnél (38%) nem jelentkeztek látszólagos tünetek, és 10 betegnél (63%) volt pigmentált induráció. Bertelli egy prospektív vizsgálatot is végzett, amely a DMSO antraciklin extravasációkra gyakorolt hatását értékelte.11 esetben 30 Doxorubicin, az epirubicin 46 esetben fordult elő. A betegeket 7 napon keresztül 8 óránként 99% DMSO-val kezelték. A betegek hetven százaléka (40/57) 1 héten belül teljes mértékben feloldotta az extravasációt, egy betegnek maradék lágyrész-indurációja volt, egy betegnek pedig maradék hiperpigmentációja volt.
ezekben az esetjelentésekben és kis vizsgálatokban az extravasációkat klinikailag diagnosztizálták, nem pedig biopsziával. DMSO lehet egy lehetőség kezelésére extravasált antraciklinek, mitomicin C, és aktinomicin D. javasoljuk, hogy egy vékony réteg DMSO kell alkalmazni az extravasált területen, és hagyjuk megszáradni. A nem záródó kötést 10-25 percen belül kell alkalmazni. Ezeket a lépéseket 8 óránként 7 napig meg kell ismételni.23 bár a DMSO-t a gyakorlatban a kezelés lehetőségeként alkalmazták, a prospektív vizsgálatok hiánya korlátozhatja annak használatát. Az EONS 2007 extravasációs iránymutatások további vizsgálatok elvégzését javasolják; azonban a DMSO 50-99% – a a klinikus belátása szerint alkalmazható.23 fontos megjegyezni, hogy a DMSO prospektív vizsgálatok egyike sem használt kötést annak érdekében, hogy a bőr teljes mértékben felszívja a DMSO-t.
hialuronidáz: Úgy gondolják, hogy a hialuronidáz képes lebontani az extracelluláris mátrixot, amely az epiteliális sejtek alapját képezi. A mátrix nagy mennyiségű vízmolekulát tart fenn, bomlása után képes felszabadítani a folyadékot az extracelluláris miliőbe. Extravasáció esetén lehetővé teszi a megnövekedett folyadék bejutását a helyszínre, ezáltal hígítva a bőr tényleges koncentrációját az érintkezés helyén.31,32 a hialuronidázt vinca alkaloid és taxán extravasációk kezelésére alkalmazták.33 adag hialuronidáz 150-1500 egység között, 1 mL normál sóoldatban szubkután vagy intradermálisan hígítva, az extravasációt követő 1 órán belül.
6 vinblasztin (n = 1), vinkrisztin (n = 1) és vinorelbin (n = 4) extravasatióban szenvedő beteg bevonásával végzett kis klinikai vizsgálatban 250 egység hialuronidázt fecskendeztek be az indwelling katéterbe, vagy szubkután (6 injekció) sérülés esetén. Szteroidokat vagy hideg csomagokat nem alkalmaztak. A fájdalom a hialuronidáz-kezelés után néhány napon belül megszűnt minden betegnél. Az egyik beteg enyhén fájdalmas indurációra panaszkodott 3 hónappal a vinkrisztin extravasációja után.30 ezek a jelentések ígéretes információkat tárnak fel; azonban még mindig nincs bizonyíték a hialuronidáz alkalmazására a vinca alkaloid extravasációk kezelésére. További prospektív vizsgálatokat kell végezni. Az EONS 2007 extravasation Irányelvek további vizsgálatok elvégzését javasolják; azonban a hialuronidáz opciónak tekinthető a javasolt dózisoknál a klinikus belátása szerint.23
nátrium-tioszulfát: A nátrium-tioszulfát megakadályozza az alkilezést és a szövetek pusztulását azáltal, hogy szubsztrátot biztosít a bőr alatti szövet alkilezéséhez. A nátrium-tioszulfát hatásosnak bizonyult állatkísérletekben és egy esetben mechloretamin (nitrogén-mustár) extravasáció kezelésére vonatkozó jelentésben.33,34 a javasolt adag 2 mL 0,17 M (4 mL 10% nátrium-tioszulfát és 6 mL steril injekcióhoz való víz). A bizonyítékok hiánya miatt az EONS 2007 extravasation irányelvek nem javasolják ezt antidotumként.22
dexrazoxán: A dexrazoxánt (Totect) nemrégiben hagyta jóvá az FDA az antraciklin által kiváltott extravasációk kezelésére. Dexrazoxán kettős hatásmechanizmus: 1) úgy viselkedik, mint egy vaskelát képző, megakadályozza a kialakulását vas-antraciklin komplexek, valamint vas-mediált hidroxil gyökök okozó oxidatív károsodás; illetve 2) stabilizálja a topoizomeráz II teszi megközelíthetetlen antraciklin kemoterápia. A dexrazoxán blokkolja az enzimet, így az antraciklin már nem befolyásolja, és megakadályozza a szövetek egészséges sejtjeinek károsodását.35
a dexrazoxán hatásosságát két, Európában végzett klinikai vizsgálatban igazolták.36 mindkét vizsgálat prospektív, nyílt, egykaros, multicentrikus klinikai vizsgálat volt 2001 júliusától 2005 augusztusáig, összesen 80 beteget vontak be. Az első vizsgálatba 17 dániai rákos megbetegedést, a másodikba 34 dániai, németországi, olaszországi és hollandiai rákos megbetegedést vontak be. Az antraciklin extravazációját fluoreszcens mikroszkópiával diagnosztizálták és igazolták a dexrazoxánt követő 6 órán belül vett biopsied szövetben. A 32 felmérhető betegből álló mintaméretnek a műtét előfordulási gyakoriságának legalább 70% – os csökkenését kellett mutatnia (egyoldalú binomiális teszt, a = .025, ß = .20). Az elsődleges végpont a sebészeti reszekció és a nekrózis aránya volt. A 80 beteg közül ötvennégy (1. vizsgálat: n = 18; 2. vizsgálat: n = 36) értékelhető volt (n = 13 negatív biopszia; n = 4 nem végzett biopszia; n = 8 protokoll megsértése), átlagos életkora 56 év (tartomány, 34-81 év). A vizsgált betegek hatvankilenc százaléka (n = 37) nő volt. A dexrazoxánt IV. infúzióban adták 1-2 óra alatt; 1000 mg/m2 6 órán belül; 1000 mg/m2 24 óra után; és 500 mg/m2 48 óra extravasáció után.36
a betegek hatásosságát és biztonságosságát a 7., 14., 21. és 28. napon értékelték, és a 90. 36. napon a leggyakoribb rákdiagnosztika az emlőrák (50%) volt, amelyet limfóma (39%) és más típusú rák (9%) követett. A betegeknél doxorubicin (n = 23) vagy epirubicin (n = 31) extravasációját tapasztalták. Az átlagos extravasációs terület 23,6 cm2 volt az 1. vizsgálatban és 39 cm2 volt a 2.vizsgálatban. Tizenegy betegnél 75 cm2-t meghaladó extravasációs területek voltak. A 2.vizsgálatban az 1. és 1. vizsgálatban (2,8%, 95% CI 0,1% -14,5%) nem fordult elő sebészeti beavatkozás. Az extravasáció következtében kialakult szöveti nekrózisban szenvedő betegnek nagyon nagy, 253 cm2-es doxorubicin extravasációs területe volt. A tünetek az extravasációt követő napokban növekedtek, a szöveti nekrózis a beteg extravasációját követő 9 napon belül jelentkezett, a nekrózist pedig műtéti úton kivágták. Az 1. vizsgálatban 1 (5,6%) biopszia miatti nekrózis történt, 6 (33).3%) a tervezett rákkezelés elhalasztása vagy törlése, valamint 9 (50%) kórházi kezelés az extravasáció miatt. A tanulmány 2, van 1 (2,8% – os) eset elhalás miatt extravasatio, 3 (8.3%) balesetek elhalás miatt biopszia, 10 (27.8%) események halasztás vagy törlése az ütemezett rák kezelés miatt az extravasatio, 13 (36.1%) esetben kórházi ápolás miatt az extravasatio. A 3 hónapos követés során 88,9% – nak (n = 16) nem volt negatív következménye az 1.vizsgálatban és 63,9% – nak (n = 23) a 2. vizsgálatban. A 80 beteg közül tizenöt érzékszervi zavart (n = 9), bőr atrófiát (n = 5), fájdalmat (n = 10), torzulást (n = 1) és korlátozást (n = 3) tapasztalt. A betegek többsége (71%) menetrend szerint további kemoterápiás kezelést kapott.
A leggyakoribb mellékhatások tartalmazza a csökkent fehérvérsejtszám (72.5%), csökkent hemoglobin (42.5%), csökkent vérlemezkeszám (26%), fokozott aszpartát-aminotranszferáz (36.8%), fokozott alanin-aminotranszferáz (a fiúk 23,9%), az alkalmazás helyén fellépő reakció (27.5%), valamint hányinger (18.8%).36 a klinikai vizsgálatok eredményei azt mutatták, hogy a dexrazoxán hatékony szer az akut antraciklin extravasációk kezelésére és a késleltetett tünetek megelőzésére.
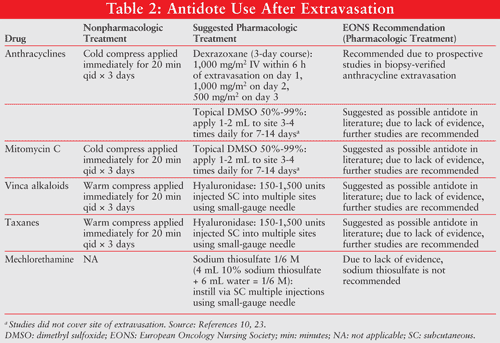
ezen kezelési ajánlások összefoglalását, beleértve az EONS 2007 iránymutatásokat, a 2.táblázat tartalmazza.
A gyógyszerész szerepe
a gyógyszerészeknek szorosan részt kell venniük a kemoterápia által kiváltott extravasációk értékelésében és kezelésében. Több szempontból is szerves szerepet játszhatnak, többek között: 1) szakpolitikák és protokollok kidolgozása; 2) beteg -, család-és multidiszciplináris oktatás; 3) extravasációk és egyéb, a kezelést követő gyógyszermellékhatások dokumentálása és bejelentése; és 4) a kezelés megfelelő adagolásának, beadásának és hatékonyságának ellenőrzése.
következtetés
az összes vizsgált vizsgálat felnőtteket érintett, mivel a gyermekgyógyászati betegeknél fokozott lett volna a izgatottság és a vonalak húzódása kockázata. Dátum, dexrazoxán az egyetlen extravasatio ügynök, hogy vizsgálták a nagy, multicentrikus, prospektív vizsgálatokban használt objektív, megbízható vizsgálati diagnosztizálni extravasatio esetekben; ez biztosítja az erős bizonyíték dexrazoxán közüzemi szolgáltató. Annak ellenére, hogy a gyakorlatban gyakran alkalmazzák, más farmakológiai kezeléseket, például a DMSO-t és a hialuronidázt nem vizsgálták széles körben, ezért hiányoznak a bizonyítékokon alapuló ajánlások. Az extravasáció kezelését a klinikus belátása szerint kell elvégezni az egészségügyi csapat minden tagjával együttműködve.
1. Infúziós Ápolók Társasága. Infúziós ápolási szabványok a gyakorlatban. J Infus Nurs. 2006;29(suppl 1): S1-S92.
2. Polovich M, White J, Kelleher L. kemoterápia és bioterápia irányelvek és ajánlások gyakorlat. 2. Szerk. Pittsburgh, PA: Oncology Nursing Society; 2005.
3. Ener RA, Meglathery SB, Styler M. szisztémás hemato-onkológiai terápiák Extravasációja. Ann Oncol. 2004;15:858-862.
4. Sauerland C, Egelking C, Wickman R, Corbi D. Vesicant extravasation I. rész: mechanizmusok, patogenezis és ápolási ellátás a kockázat csökkentése érdekében. Oncol Nurs Fórum. 2006;33:1134-1141.
5. Cassagnol M, Cohen H. Dermatologic toxicities of chemotherapeutic agents. US Pharm. 2008;33(1)(Oncology suppl):10-20.
6. Schulmeister L. Extravasation management. Semin Oncol Nurs. 2007;23:184-190.
7. Viale P. Chemotherapy and cutaneous toxicities: implications for oncology nurses. Semin Oncol Nurs. 2006;22:144-151.
8. Cox K, Stuart-Harris R, Abdini G, et al. The management of cytotoxic-drug extravasation: guide-lines drawn up by a working party for the Clinical Oncological Society of Australia. Med J Aust. 1988;148:185-189.
9. Schrijvers DL. Extravasation: a kemoterápia rettegett szövődménye. Ann Oncol. 2003;14(suppl 3): iii26-iii30.
10. Az Országos Extravasációs Információs Szolgálat. www.extravasation.org.uk/home.html.hozzáférés 2009. március 25-én.
11. Lemmers N, gélek M, Sleijfer D, et al. Szövődményei vénás portok 132 beteg disszeminált hererák kezelt polychemotherapy. J-Klin-Onkol. 1996;14:2916-2922.
12. Shetty PC, Mody MK, Kastan DJ. Az intervenciós radiológusok által elhelyezett 350 beültetett mellkaskikötő eredménye. J Vasc Interv Radiol. 1997;8:991-995.
13. Dorr RT. A vesicant kemoterápia extravasációinak antidotumai. Blood Rev. 1990;4: 41-60.
14. Langer SW, Sehested M, Jensen PB. Antraciklin extravasáció kezelése dexrazoxánnal. Clin Cancer Res.2000; 6: 3680-3686.
15. Raymond E, Faivre S, Woynarowski JM, Chaney SG. Oxaliplatin: hatásmechanizmus és daganatellenes aktivitás. Semin Oncol. 1998;2 (suppl 5): 4-12.
16. Rivory LP. Új gyógyszerek a vastagbélrák számára-hatásmechanizmusok. Aust Prescr. 2002;25:108-110. www.australianprescriber.com/magazine/25/5/108/10/. hozzáférés 2009. március 25-én.
17. Skeel RT. kézikönyve a rák kemoterápia. 5. Szerk. New York, NY: Lippincott Williams & Wilkins; 1999.
18. Boyle DM, Engelking C. Vesicant extravasation: myths and realities. Oncol Nurs Fórum. 1995;22:57-67.
19. Hadaway LC. A perifériás extravasáció megelőzése és kezelése. Ápolás. 2004;34:66-67.
20. Shulmeister L, Camp-Sorrell D. kemoterápia extravasation a beültetett kikötőkből. Oncol Nurs Fórum. 2000;27:531-538.
21. Debets JM, Wils JA, Schlangen JT. A beültetett centrális vénás hozzáférési eszközök ritka szövődménye: katétertörés és embolizáció. Támogatás Ellátás Rák. 1995;3:432-434.
22. Gorski LA. Központi vénás hozzáférési eszköz elzáródások. 2. rész: nem trombotikus okok és kezelés. Otthoni Egészségügyi Nővér. 2003;21:168-171.
23. Extravasation guidelines 2007. Európai Onkológiai Ápolási Társaság. www.cancerworld.org/CancerWorld/getStaticModFile.aspx?id=2340.hozzáférés 2009. március 25-én.
24. Rimso-50 (dimetil-szulfoxid) csomagolóbetét. Lake Forest, IL: Bioniche Pharma USA LLC; 2009.
25. Lawrence HJ, Jó éjszakát SH. Dimetil-szulfoxid korlátozó szövetkárosodás okozta extravasation doxorubicin szerek. Ann Gyakornok Orvos. 1983;98:1025.
26. Olver IN, Schwarz MA. Use of dimethyl sulfoxide in limiting tissue damage caused by extravasation of doxorubicin . Cancer Treat Rep. 1983;67:407-408.
27. Berghammer P, Pohnl R, Baur M, Dittrich C. Docetaxel extravasation. Support Care Cancer. 2001;9:131-134.
28. Ludwig CU, Stoll HR, Obrist R, Obrecht JP. Prevention of cytotoxic drug-induced skin ulcers with dimethyl sulfoxide (DMSO) and alpha-tocopherole. Eur J Cancer Clin Oncol. 1987;23:327-329.
29. Olver IN, Aisner J, Hament A, et al. A prospective study of topical dimethyl sulfoxide for treating anthracycline extravasation. J Clin Oncol.1988;6:1732-1735.
30. Bertelli G. Prevention and management of extravasation of cytotoxic drugs. Drug Saf. 1995;12:245-255.
31. Balazs EA, Laurent TC, Jeanloz RW. Nomenclature of hyaluronic acid. Biochem J. 1986;235:903.
32. Girish KS, Kemparaju K. The magic glue hyaluronan and its eraser hyaluronidase. Life Sci. 2007;80:1921-1943.
33. Dorr T. Antidotes to vesicant chemotherapy extravasations. Blood Rev. 1990;4:41-60.
34. Owen OE, Dellatorre DL, Van Scott EJ, Cohen MR. Accidental intramuscular injection of mechlorethamine. Cancer. 1980;45:2225-2226.
35. Totect (dexrazoxane for injection) package insert. Copenhagen, Denmark: TopoTarget A/S; October 2007.
36. Mouridsen HT, Langer SW, Buter J, et al. Treatment of anthracycline extravasation with Savene (dexrazoxane). Results from two prospective clinical multicenter studies. Ann Oncol. 2007;18:546-550.
Leave a Reply