6.4: ATP: adenozin-trifoszfát
készségek fejlesztése
- magyarázza el az ATP szerepét a celluláris energia pénznemében
- írja le, hogyan szabadul fel az energia az ATP
hidrolízisével. Vegye figyelembe azonban az endergonikus reakciókat, amelyek sokkal több energiát igényelnek, mivel termékeik több szabad energiával rendelkeznek, mint reagenseik. A sejten belül honnan származik az energia az ilyen reakciók táplálására? A válasz az adenozin-trifoszfátnak vagy ATP-nek nevezett energiaellátó molekulában rejlik. Az ATP egy kicsi, viszonylag egyszerű molekula (\ábra\ (\PageIndex{1}\)), de egyes kötésein belül tartalmazza a gyors energiarobbanás lehetőségét, amelyet celluláris munka elvégzésére lehet felhasználni. Ez a molekula ugyanúgy tekinthető a sejtek elsődleges energia pénznemének, mint a pénz az a pénznem, amelyet az emberek cserélnek a szükséges dolgokért. Az ATP-t az energiát igénylő celluláris reakciók többségének táplálására használják.

ahogy a neve is sugallja, az adenozin-trifoszfát három foszfátcsoporthoz kötött adenozinból áll(ábra \(\PageIndex{1}\)). Az adenozin egy nukleozid, amely a nitrogénbázis adeninből és egy öt széntartalmú cukorból, ribózból áll. A három foszfátcsoport a ribózcukor legtávolabbi pontjainak sorrendjében alfa, béta és gamma. Ezek a kémiai csoportok együttesen energiahordozót alkotnak. Ennek a molekulának azonban nem minden kötése létezik különösen nagy energiájú állapotban. A foszfátokat összekötő mindkét kötés egyformán nagy energiájú kötések (foszfoanhidrid kötések), amelyek töréskor elegendő energiát bocsátanak ki a különböző sejtreakciók és folyamatok táplálására. Ezek a nagy energiájú kötések a második és harmadik (vagy béta-és gamma -) foszfátcsoportok, valamint az első és a második foszfátcsoportok közötti kötések. Az oka, hogy ezek a kötvények tekinthető “nagy energiájú”, mert a termékek az ilyen kötvény törés—adenozin-difoszfát (ADP) egy szervetlen foszfát csoport (Pi)—lényegesen alacsonyabb, szabad energia, mint a reagensek: ATP, a víz molekula. Mivel ez a reakció egy vízmolekula használatával történik, hidrolízis reakciónak tekinthető. Más szavakkal, az ATP hidrolizálódik ADP-be a következő reakcióban:
a legtöbb kémiai reakcióhoz hasonlóan az ATP ADP-re történő hidrolízise reverzibilis. A fordított reakció regenerálja az ATP-t az ADP + Pi-ből. Valójában a sejtek az ATP regenerációjára támaszkodnak, ahogyan az emberek valamilyen jövedelem révén az elköltött pénz regenerációjára támaszkodnak. Mivel az ATP hidrolízis energiát szabadít fel, az ATP regenerációnak szabad energia bevitelét kell igényelnie. Az ATP kialakulását ebben az egyenletben fejezzük ki:
két kiemelkedő kérdés marad az ATP energiaforrásként történő felhasználásával kapcsolatban. Pontosan mennyi szabad energia szabadul fel az ATP hidrolízisével, és hogyan használják fel ezt a szabad energiát a sejtek működéséhez? Az ATP egy móljának ADP-be és PI-be történő hidrolízisére számított ∆g -7,3 kcal/mól (-30,5 kJ / mol). Mivel ez a számítás normál körülmények között igaz, várható, hogy celluláris körülmények között más érték létezik. Valójában a ∆G egy mól ATP hidrolízisére egy élő sejtben majdnem kétszerese az értéknek normál körülmények között: 14 kcal/mol (-57 kJ/mol).
az ATP rendkívül instabil molekula. Hacsak nem használják fel gyorsan a munkát, az ATP spontán disszociál az ADP + Pi-be, és a folyamat során felszabaduló szabad energia hő formájában elvész. A fenti második kérdés, vagyis az ATP hidrolízis által felszabadított energia felhasználása a sejten belüli munka elvégzésére, az energia-összekapcsolásnak nevezett stratégiától függ. A sejtek összekapcsolják az ATP hidrolízis exergonikus reakcióját endergonikus reakciókkal, lehetővé téve számukra a folytatást. Az ATP használatával történő energiacsatlakozás egyik példája egy transzmembrán ionszivattyú, amely rendkívül fontos a celluláris funkció szempontjából. Ez a nátrium-kálium szivattyú (Na+/K+ szivattyú) a nátriumot a sejtből, a káliumot pedig a sejtbe vezeti (6.4.2.ábra). A sejt ATP-jének nagy részét a szivattyú táplálására fordítják, mivel a sejtes folyamatok nagy mennyiségű nátriumot hoznak a sejtbe,a káliumot pedig a sejtből. A szivattyú folyamatosan működik, hogy stabilizálja a sejtek nátrium-és kálium-koncentrációját. Annak érdekében, hogy a szivattyú egy ciklust (három Na+ iont exportál, és két k+ iont importál), egy ATP molekulát hidrolizálni kell. Amikor az ATP hidrolizálódik, a gamma-foszfát nem egyszerűen lebeg, hanem valójában átkerül a szivattyú fehérjére. A molekulához kötődő foszfátcsoport ezen folyamatát foszforilációnak nevezzük. Az ATP hidrolízis legtöbb esetéhez hasonlóan az ATP-ből származó foszfát egy másik molekulára kerül. Foszforilált állapotban a Na + / K + szivattyú több szabad energiával rendelkezik, és konformációs változáson megy keresztül. Ez a változás lehetővé teszi a Na + felszabadítását a sejt külső oldalára. Ezután kötődik az extracelluláris k+ – hoz, amely egy másik konformációs változáson keresztül a foszfát leválik a szivattyúról. A foszfát felszabadulása kiváltja a K+ felszabadulását a sejt belsejébe. Lényegében az ATP hidrolíziséből felszabaduló energia a szivattyú táplálásához és a na+ és K+ ionok szállításához szükséges energiával párosul. Az ATP celluláris munkát végez az energiacsatlakozás ezen alapvető formájával foszforilációval.
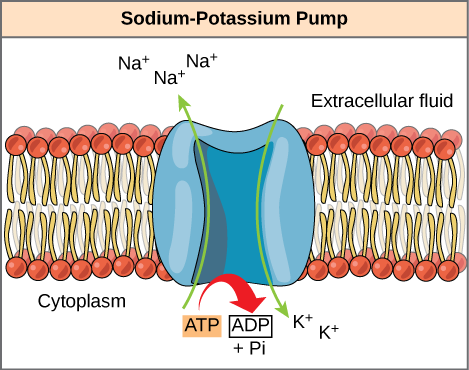
egy ATP molekula hidrolízise 7,3 kcal/MOL energiát bocsát ki (∆g = -7,3 kcal / MOL energia). Ha 2,1 kcal/MOL energiát igényel egy Na + mozgatása a membránon (∆g = + 2,1 kcal / MOL energia), hány nátriumionot lehet mozgatni egy ATP molekula hidrolízisével?
Gyakran a sejt anyagcsere-reakciók, mint például a szintézis pedig bontása tápanyagok, bizonyos molekulák kell módosítani kissé a húsosság, hogy lesz hordozók a következő lépés a reakció sorozat. Az egyik példa a sejtes légzés első lépései során, amikor a cukor glükóz molekulája lebomlik a glikolízis folyamatában. Ennek a folyamatnak az első lépésében az ATP szükséges a glükóz foszforilációjához, ami nagy energiájú, de instabil köztiterméket hoz létre. Ez a foszforilációs reakció olyan konformációs változást eredményez, amely lehetővé teszi a foszforilált glükózmolekula átalakítását a foszforilált cukor fruktózra. A fruktóz szükséges Köztes A glikolízis előrehaladásához. Itt az ATP hidrolízis exergonikus reakciója összekapcsolódik azzal az endergonikus reakcióval, amely a glükózt foszforilált közbensővé alakítja az úton. Még egyszer, a felszabaduló energia megtöri egy-foszfát bond belül ATP használták a mőszer a másik molekula, ami egy instabil köztes, illetve működteti fontos reakcióelegy.

interaktív animáció az ATP-termelő glikolízis folyamatról ezen az oldalon.
összefoglaló
az ATP az élő sejtek elsődleges energiaellátó molekulája. Az ATP nukleotidból, öt szén-dioxid-cukorból és három foszfátcsoportból áll. A foszfátokat (foszfoanhidridkötéseket) összekötő kötések nagy energiatartalommal rendelkeznek. Az ATP ADP + Pi-be történő hidrolíziséből felszabaduló energiát celluláris munka elvégzésére használják. A sejtek ATP-t használnak a munka elvégzésére azáltal, hogy összekapcsolják az ATP hidrolízis exergonikus reakcióját endergonikus reakciókkal. Az ATP foszfátcsoportját egy másik molekulának adományozza egy foszforiláció néven ismert folyamat révén. A foszforilált molekula nagyobb energiájú állapotban van, kevésbé stabil, mint a nem foszforilált formája, és ez a foszfát hozzáadásával hozzáadott energia lehetővé teszi a molekula endergonikus reakcióját.
Art Connections
egy ATP molekula hidrolízise 7,3 kcal/mol energiát bocsát ki (∆g = -7,3 kcal / MOL energia). Ha kell 2.1 kcal/mol energia egy Na + mozgatásához a membránon (∆g = + 2,1 kcal / MOL energia), hány nátriumionot lehet mozgatni egy ATP molekula hidrolízisével?
három nátriumion mozgatható egy ATP molekula hidrolízisével. A kapcsolt reakció ∆G-jének negatívnak kell lennie. Három nátriumion mozgása a membránon 6,3 kcal energiát vesz igénybe (2,1 kcal × 3 Na+ ionok = 6,3 kcal). Az ATP hidrolízise 7,3 kcal energiát biztosít, ami több mint elegendő a reakció táplálásához. Négy nátriumion mozgása a membránon keresztül azonban 8-at igényel.4 kcal energia, több mint egy ATP molekula képes biztosítani.
ellenőrző Kérdések
A felszabaduló energia az ATP hidrolízis
- elsősorban tárolt között az alfa -, béta-foszfátok
- egyenlő -57 kcal/mol
- hasznosítani, mint a hőenergia, amelyet a sejt munkát végezzen,
- nyújtó energia termeléstől függő reakciók
D
az alábbiak közül Melyik molekulák valószínű, hogy a legtöbb potenciális energia?
- szacharóz
- ATP
- glükóz
- ADP
A
Ingyenes Válasz
Gondolod, hogy az EA az ATP hidrolízis viszonylag alacsony vagy magas? Magyarázd el az érvelésedet.
a hidrolízis aktiválási energiája nagyon alacsony. Nem csak az ATP hidrolízis exergonikus folyamat, nagy −∆G-vel, hanem az ATP is egy nagyon instabil molekula, amely gyorsan lebomlik az ADP + Pi-ba, ha nem használják gyorsan. Ez nagyon alacsony EA-t sugall, mivel olyan gyorsan hidrolizál.
Szójegyzék
ATP-adenozin-trifoszfát, a sejt energia valuta phosphoanhydride kötvény kötvény, amely összeköti a foszfátok egy ATP molekula
Közreműködők, valamint Dolgának
-
Connie Rozs (Kelet-Mississippi Közösségi Főiskola), Robert Wise (University of Wisconsin, Mucsáról), Vladimir Jurukovski (Suffolk Megyei Főiskolán), Jean DeSaix (University of North Carolina a Chapel Hill), Choi Jung (Georgia Institute of Technology), Yael Avissar (Rhode Island-i Egyetemen) többek között a közreműködő szerzők. Eredeti tartalom OpenStax (CC által 4.0; ingyenesen letölthető a http://cnx.org/contents/185cbf87-c72…[email protected]).
Leave a Reply