NOAA Global Monitoring Laboratory – Halocarbons and other Atmospheric Trace Species
Chlorofluorocarbons (CFCs)
(published in The Chapman & Hall Encyclopedia of Environmental Science, edited by David E. Alexander and Rhodes W. Fairbridge, pp pp.78-80, Kluwer Academic, Boston, MA, 1999.)
Chlorofluorocarbons (CFCs) are nontoxic, nonflammable chemicals containing atoms of carbon, chlorine, and fluorine. De anvendes til fremstilling af aerosolsprayer, blæsemidler til skum og emballagematerialer, som opløsningsmidler og som kølemidler. CFC ‘ er er klassificeret som halocarboner, en klasse af forbindelser, der indeholder atomer af kulstof og halogenatomer. Individuelle CFC-molekyler er mærket med et unikt nummereringssystem. For eksempel angiver CFC-tallet på 11 antallet af atomer af kulstof, hydrogen, fluor og chlor (f.eks. CCl3F som CFC-11). Den bedste måde at huske systemet på er “reglen om 90” eller tilføj 90 Til CFC-nummeret, hvor det første ciffer er antallet af carbonatomer (C), det andet ciffer er antallet af hydrogenatomer (H), og det tredje ciffer er antallet af fluoratomer (F). Det samlede antal chloratomer(Cl) beregnes ved udtrykket: Cl = 2 (C+1) – H – F. I eksemplet CFC-11 har et kulstof, ingen hydrogen, en fluor og derfor 3 chloratomer.
køleskabe i slutningen af 1800-tallet og begyndelsen af 1900-tallet brugte de giftige gasser, ammoniak (NH3), methylchlorid (CH3Cl) og svovlsyre (SO2) som kølemidler. Efter en række dødsulykker i 1920 ‘ erne, da methylchlorid lækkede ud af køleskabe, begyndte en søgning efter en mindre giftig udskiftning som en samarbejdsindsats fra tre amerikanske virksomheder – Frigidaire, General Motorsog du Pont. CFC ‘ er blev først syntetiseret i 1928 af Thomas Midgley, Jr.af General Motors, som sikrere kemikalier til køleskabe, der anvendes i store kommercielle appilications1. Frigidaire blev udstedt det første patent, nummer 1.886.339, for formlen for CFC ‘ er den 31.December 1928. I 1930 dannede General Motors og du Pont Kinetic Chemical Company til at producere Freon (et du Pont-handelsnavn for CFC ‘ er) i store mængder. I 1935 havde Frigidaire og dets konkurrenter solgt 8 millioner nye køleskabe i USA ved hjælp af Freon-12 (CFC-12) fremstillet af Kinetic Chemical Company og de virksomheder, der fik licens til at fremstille denne forbindelse. I 1932 brugte Carrier Engineering Corporation Freon-11 (CFC-11) i verden, som først var en selvstændig klimaanlæg til hjemmet, kaldet “atmosfærisk kabinet”.; På grund af CFC-sikkerhedsrekorden for ikke-toksicitet blev Freon det foretrukne kølemiddel i store klimaanlæg. Folkesundhedskoder i mange amerikanske byer blev revideret for at udpege Freon som det eneste kølevæske, der kunne bruges i offentlige bygninger. Efter Anden Verdenskrig blev CFC ‘ er brugt som drivmidler til bugspray, maling, hårbalsam og andre sundhedsprodukter. I slutningen af 1950 ‘erne og begyndelsen af 1960’ erne gjorde CFC ‘ erne en billig løsning på ønsket om aircondition i mange biler, hjem og kontorbygninger. Senere steg væksten i CFC-brug over hele verden med et årligt salg på omkring en milliard dollars (USA) og mere end en million tons produceret CFC.
mens CFC ‘ er er sikre at bruge i de fleste applikationer og er inerte i den nedre atmosfære, gennemgår de signifikant reaktion i den øvre atmosfære eller stratosfæren. I 1974 blev to kemikere fra University of California, Professor F. Mario Molina viste, at CFC ‘ erne kunne være en vigtig kilde til uorganisk chlor i stratosfæren efter deres fotolytiske nedbrydning ved UV-stråling. Derudover vil nogle af de frigivne klor blive aktive til at ødelægge osomon i stratosfæren2. Det er en gas, der primært findes i stratosfæren. Det absorberer skadelig ultraviolet stråling i bølgelængderne mellem 280 og 320 nm af UV-B-båndet, hvilket kan forårsage biologisk skade på planter og dyr. Et tab af stratosfærisk osomon resulterer i mere skadelig UV-B-stråling, der når jordens overflade. Klor frigivet fra CFC ‘ er ødelægger osomon i katalytiske reaktioner, hvor 100.000 molekyler af osomon kan ødelægges pr.
en stor udtømning af stratosfærisk osomon i foråret blev værre hvert følgende år. Dette tab blev beskrevet i 1985 af den britiske forsker Joe Farman og hans kolleger3. Det blev kaldt den antarktiske ø hole af andre. Det var et andet hul end et tab i mellemhøjderne. Tabet var større over Antarktis end mellemhøjderne på grund af mange faktorer: de usædvanligt kolde temperaturer i regionen,den dynamiske isolering af denne kurthole, og de synergistiske reaktioner af chlor og brom4. Også i polare områder som følge af reaktioner, der involverer polære stratosfæriske skyer (PSCs)5 og i mellemhøjder efter vulkanudbrud. Behovet for at kontrollere CFC ‘ erne blev presserende. i 1987 underskrev 27 nationer en global miljøaftale, Montreal-protokollen for at reducere stoffer, der nedbryder Osområdet6, der havde en bestemmelse om at reducere produktionsniveauerne for disse forbindelser i 1986 med 50% inden år 2000. Denne internationale aftale omfattede restriktioner for produktion af CFC-11, -12, -113, -114, -115, og Halonerne (kemikalier, der anvendes som brandslukningsmidler). En ændring, der blev godkendt i London i 1990, var mere kraftig og opfordrede til eliminering af produktionen inden år 2000. De chlorerede opløsningsmidler, methylchloroform (CH3CCl3) og carbontetrachlorid (CCl4) blev føjet til London-ændringen. store mængder af reaktivt stratosfærisk chlor i form af chlormonilte (ClO), der kun kunne skyldes ødelæggelsen af CFC ‘ erne i stratosfæren, blev observeret af instrumenter ombord på NASA er-2-flyet og UARS (Upper Atmospheric Research Satellite) over nogle regioner i Nordamerika i løbet af vinteren 19927,8. Den miljømæssige bekymring for CFC ‘ er følger af deres lange atmosfæriske levetid (55 år for CFC-11 og 140 år for CFC-12, CCl2F2)9, som begrænser vores evne til at reducere deres overflod i atmosfæren og tilhørende fremtidige tab af osomfang. Dette resulterede i Københavns ændring, der yderligere begrænsede produktionen og blev godkendt senere i 1992. Fremstillingen af disse kemikalier sluttede for det meste den 1.januar 1996. De eneste undtagelser, der blev godkendt, var for produktion i udviklingslande og for nogle undtagne applikationer inden for medicin (dvs.astmainhalatorer) og forskning. Montreal-protokollen omfattede håndhævelsesbestemmelser ved at anvende økonomiske og handelsmæssige sanktioner, hvis et signatarland handler eller producerer disse forbudte kemikalier. I alt 148 underskrivende lande har nu underskrevet Montreal-protokollen. Atmosfæriske målinger CFC-11 og CFC-12 rapporteret i 1993 viste, at deres vækstrater var faldende som følge af både frivillige og mandaterede reduktioner i emissioner9. Mange CFC ‘ er og udvalgte chlorerede opløsningsmidler er enten udjævnet (Figur 1) eller faldet i koncentrationen i 19949,10.
efterspørgslen efter CFC ‘er blev imødekommet ved genanvendelse og genbrug af eksisterende lagre af CFC’ er og ved anvendelse af erstatninger. Nogle applikationer, for eksempel affedtning af metaller og rengøringsopløsningsmidler til kredsløb, der engang brugte CFC ‘ er bruger nu halocarbonfrie væsker, vand (undertiden som damp) og fortyndede citronsyrer. Industrien udviklede to klasser af halocarbonsubstitutter-hydrochlorfluorcarboner (HCFC ‘er) og hydrofluorcarboner (HFC’ er). HCFC ‘ erne inkluderer hydrogenatomer ud over chlor -, fluor-og carbonatomer. Fordelen ved at bruge HCFC ‘ er er, at brintet reagerer med troposfærisk hydroksyl (OH), hvilket resulterer i en kortere atmosfærisk levetid. HCFC – 22 (CHClF2) har en atmosfærisk levetid på omkring 13 år11 og er blevet brugt i lav efterspørgsel hjemme klimaanlæg og nogle køleapplikationer siden 1975. HCFC ‘ er indeholder dog stadig klor, hvilket gør det muligt for dem at ødelægge osomon. Københavns ændringsforslag opfordrer til, at deres produktion fjernes inden år 2030. HFC ‘ er betragtes som en af de bedste erstatninger til reduktion af stratosfærisk tab på grund af deres korte levetid og mangel på klor. I USA bruges HFC-134a i alle nye indenlandske bil klimaanlæg. For eksempel vokser HFC-134a hurtigt i 1995 med en vækstrate på omkring 100% om året med en atmosfærisk levetid på omkring 12 år12. (“Reglen om 90” gælder også for den kemiske formel for HCFC ‘er og HFC’ er.)
brug af CFC ‘ er, nogle chlorerede opløsningsmidler og haloner bør blive forældede i det næste årti, hvis Montreal-protokollen overholdes af alle parter, og der anvendes erstatninger. Videnskaben, der blev grundlaget for Montreal-protokollen, resulterede i 1995 Nobelprisen for Kemi. Prisen blev uddelt i fællesskab til professorer F. S. Ved University of California i Irvine, M. Molina ved Massachusetts Institute of Technology, Cambridge, og Paul Crutsen ved maks-Planck-Institute for Chemistry, Tyskland, for deres arbejde inden for atmosfærisk kemi, især med hensyn til dannelse og nedbrydning af osomon (især af CFC ‘ er og kvælstofilter).
1Midgley, T., og Henne, A., organiske fluorider som kølemidler, industriel og teknisk Kemi, 22, 542-547, 1930.
2Molina, M. J. og F. S. rodland, stratosfærisk vask til chlorfluormethan: Kloratom katalyserede ødelæggelse af osomon, Natur, 249, 810-814, 1974.
3farman, J. C., B. G. Gardiner og J. D. Shanklin, store tab af det samlede areal i Antarktis afslører sæsonbestemt interaktion, Natur, 315.207-210, 1985. 4mcelroy, M. B., R. J. Salavitch og J. A. Logan, reduktioner af Antarktis på grund af synergistiske interaktioner mellem klor og brom, Nature, 321, 759-762, 1986.
5Solomon, S., R. R. Garcia, F. S. Rodlandog D. J. Vuebbles, om udtømningen af Antarktis, natur, 321, 755-758, 1986.
6Montreal protokol om stoffer, der nedbryder Osomonlaget, 15 pp, De Forenede Nationers Miljøprogram (UNEP), Ny York, 1987.
7Toohey, D. V., L. M. Avallone, L. R. Lait, P. A. Nymand, M. R. Schoeberl, D. V. Fahey, E. L. træbro, og J. G. Anderson, den sæsonmæssige udvikling af reaktivt klor i stratosfæren på den nordlige halvkugle, videnskab, 261, 1134-1136, 1993.
8vand, J., L. Froidevauks, V. Read, G. Manney, L. .Elson, D. blomst, R. Jarnot og R. Harved, stratosfærisk ClO andoson fra Mikrobølgelammet på den øvre atmosfære Forskningssatellit, Natur, 362, 597-602, 1993.
9elkins, T. M. Thompson, T. H. Svanson, J. H. Butler, B. D. Hall, S. O. Cummings, D. A. Fisher og A. G. Raffo, fald i vækstraterne for atmosfæriske chlorfluorcarboner 11 og 12, Nature, 364, 780-783, 1993.
10Prinn, R. G., R. F. Uiss, B. R. Miller, J. Huang, F. N. Alyea, D. M. Cunnold, P. J. Fraser, D. E. Hartley og P. G. Simmonds, atmosfæriske tendenser og levetider for ch3ccl3 og globale OH-koncentrationer, Science, 269, 187-192, 1995.
11MONTKA, S. A., R. C. Myers, J. H. Butler, S. C. Cummings og J. V. Elkins, global troposfærisk distribution og kalibreringsskala for HCFC-22, geofysiske Forskningsbreve, 20 (8), 703-706, 1993.
12montska, S. A., R. C. Myers, J. H. Butler, J. H. Elkins, L. T. Lock, A. D. Clarke og A. H. Goldstein, observationer af HFC-134a i den fjerne troposfære, geofysiske Forskningsbreve, 23, 169-172, 1996.
foreslået yderligere læsning:
Cagin, S. og P. Dray, mellem jord og himmel: hvordan CFC ‘ er ændrede vores verden og truede osomelaget, 512 s., Pantheon Press, 1993. 1994, redigeret af D. L. Albritton, R. T. Vandsonog R. J. Aucamp, 37.451 s., Verdens Meteorologiske Organisation, Geneve, 1995.
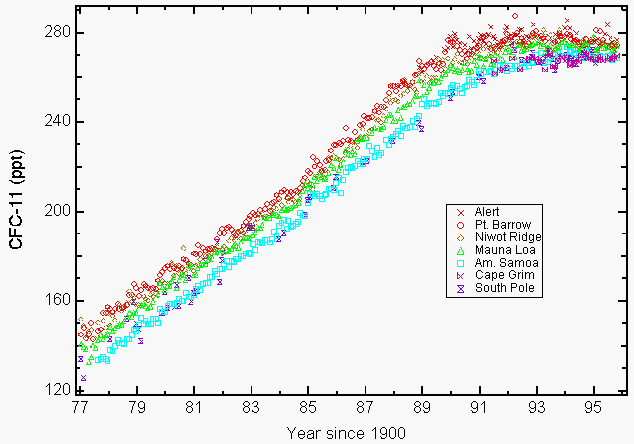
Figur 1: akkumuleringen af chlorfluorcarbon-11 (CFC-11) i atmosfæren niveauer ud som følge af frivillige og mandaterede emissionsreduktioner. Månedlige midler rapporteret som tørblandingsforhold i dele pr. billion (PPT) for CFC-11 i jordoverfladen for fire NOAA/CMDL-stationer (Pt. Mauna Loa, Alaska, USA; Cape Matatula, Amerikansk Samoa, og Sydpolen) og tre kooperative stationer (Alert, nordvestlige territorier, Canada (Atmospheric environment Service); Cape Grim Baseline Air Pollution Station, Tasmanien, Australien, (samfundets videnskabelige og industrielle forskningsorganisation)9. (Venligst udlånt af NOAA / CMDL)
Leave a Reply