Lukket system
i klassisk mekanikredit
I ikke-relativistisk klassisk mekanik er et lukket system et fysisk system, der ikke udveksler noget stof med dets omgivelser og ikke er underlagt nogen nettokraft, hvis kilde er ekstern for systemet. Et lukket system i klassisk mekanik ville svare til et isoleret system i termodynamik. Lukkede systemer bruges ofte til at begrænse de faktorer, der kan påvirke resultaterne af specifikt problem eller eksperiment.
i termodynamikrediger
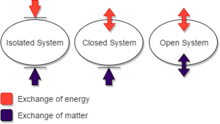
i termodynamik kan et lukket system udveksle energi (som varme eller arbejde), men ikke noget, med dets surroundings.An isoleret system kan ikke udveksle varme, arbejde eller stof med omgivelserne, mens et åbent system kan udveksle energi og stof. (Denne ordning med definition af udtryk anvendes ikke ensartet, selvom det er praktisk til nogle formål. Især bruger nogle forfattere ‘lukket system’, hvor ‘isoleret system’ bruges her.)
for et simpelt system med kun en type partikel (atom eller molekyle) udgør et lukket system et konstant antal partikler. For systemer, der gennemgår en kemisk reaktion, kan der imidlertid være ALLE slags molekyler, der genereres og ødelægges af reaktionsprocessen. I dette tilfælde udtrykkes det faktum, at systemet er lukket, ved at angive, at det samlede antal af hvert elementært atom er bevaret, uanset hvilken slags molekyle det kan være en del af. Matematisk:
j = 1 m A I J N J = B i {\displaystyle \sum _{j=1}^{m}a_{IJ}N_{j}=b_{i}}

hvor N j {\displaystyle n_{j}}

er antallet af J-type molekyler, a i J {\displaystyle a_{IJ}}

er antallet af atomer af element i {\displaystyle i}

i molekyle j {\displaystyle j}

og B i {\displaystyle b_{i}}

er samlet antal atomer af element i {\displaystyle i}

i systemet, som forbliver konstant, da systemet er lukket. Der vil være en sådan ligning for hvert andet element i systemet.
i termodynamik er et lukket system vigtigt for at løse komplicerede termodynamiske problemer. Det tillader eliminering af nogle eksterne faktorer, der kan ændre resultaterne af eksperimentet eller problemet og dermed forenkle det. Et lukket system kan også bruges i situationer, hvor termodynamisk ligevægt er nødvendig for at forenkle situationen.
I kvantefysikkredit
denne ligning, kaldet Schr-Krosdingers ligning, beskriver opførslen af et isoleret eller lukket kvantesystem, det vil sige pr.definition et system, der ikke udveksler information (dvs. energi og/eller stof) med et andet system. Så hvis et isoleret system er i en eller anden ren tilstand |liter(t) liter H på tidspunktet t, hvor H betegner systemets Hilbert-rum, er tidsudviklingen af denne tilstand (mellem to på hinanden følgende målinger).
I list t list ( r , t) = h ^ list ( r , t ) {\displaystyle I\hbar {\frac {\partial }{\partial t}}\psi \Left(\mathbf {r} ,t\right)={\hat {h}}\Psi \Left(\mathbf {r} ,t\right)\,\!}

Leave a Reply