VSEPR 2
Il contenuto che segue è la sostanza della General Chemistry Lecture 34. In questa conferenza continuiamo la discussione di VSEPR con quegli atomi che possono superare l’ottetto.
Quando un elemento è dentro o oltre il 3 ° periodo nella tavola periodica, ha la capacità di superare la regola dell’ottetto, il che significa che può creare più di 4 legami con altri atomi. In VSEPR ci sono due strutture che dobbiamo sapere che rientrano in questa categoria: AX5 e AX6.
AX5
Come con i precedenti modelli estesa ottetto modelli avvio con i titoli di stato in tutti i punti intorno all’atomo centrale:
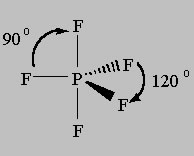
L’EPG e MG per questo modello è chiamato Trigonale Bipyramidal perché la linea di disegno dal assiale (up-down) atomi equatoriale (circa la metà) atomi mostra due 3 lati piramidi:
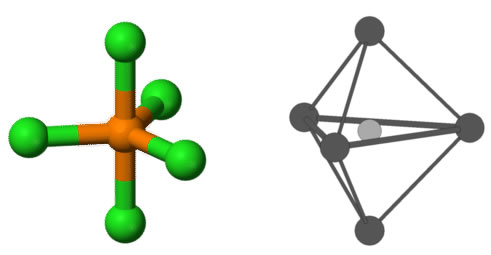
Da qui se vogliamo avviare la rimozione di vincoli e di sostituirli con lone pairs, l’EPG rimane costante con 5 regioni di densità elettronica, ma la geometria molecolare modifiche. Sono stati fatti studi per determinare dove sarebbe stato rimosso il primo atomo e si è determinato che la struttura sarebbe stata più energeticamente favorevole perdendo un atomo equatoriale prima, seconda e poi terza.
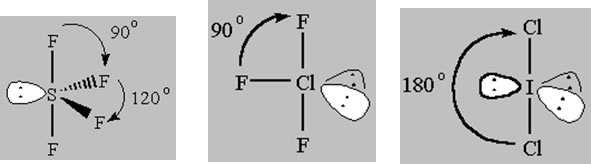
Vedere MG (AX4E), MG a forma di T (AX3E2)e poi lineare (AX2E3)
AX6
Per l’ultimo dei modelli VSEPR vedremo ci sono 6 atomi periferici collegati all’atomo centrale.
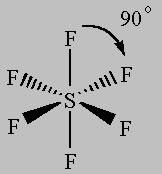
Il disegno delle posizioni degli atomi in questa disposizione è simile al sistema di coordinate cartesiane:
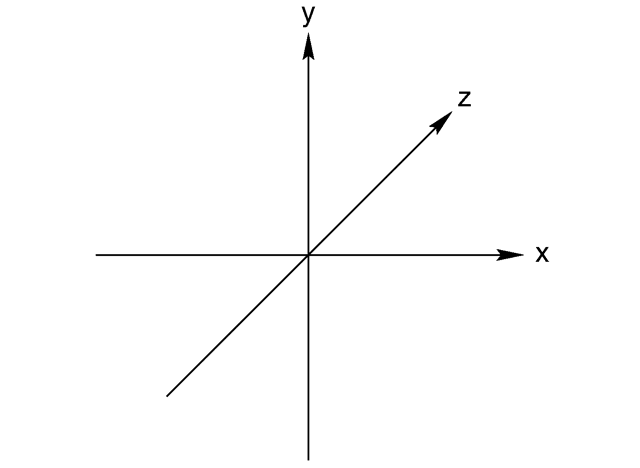
Con gli atomi periferici ad ogni estremità dell’asse.
Come per i modelli precedenti, EPG e MG hanno lo stesso nome quando tutti e 6 gli atomi sono legati all’atomo centrale. In questo caso la struttura è chiamata Ottaedrica (8 lati).
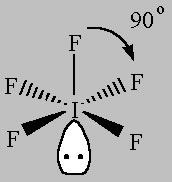
Quando rimuovi gli atomi e lasci le coppie solitarie, appaiono le seguenti strutture:
 |
 |
|
Square Pyramidal (AX5E)
|
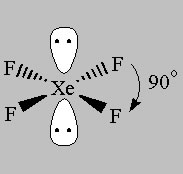
Square Planar (AX4E2)
|
Leave a Reply