Pro e contro del test prenatale
Lo scopo dello screening e della diagnosi prenatale è quello di identificare anomalie cromosomiche, condizioni genetiche e anomalie strutturali nel feto prima della nascita.
Le opzioni di screening e diagnostica coinvolgono una serie di test non invasivi e invasivi in diverse fasi della gravidanza, e hanno avanzato a passi da gigante negli ultimi 40 anni, in parallelo con significativi cambiamenti sociali e demografici nel corso di quel tempo.
In Australia nel 2013, l’età media delle donne che ha partorito è stata 30.1 anni, contro il 29,5 nel 2003, mentre la percentuale di madri di età compresa tra 35 e oltre è aumentata dal 19% nel 2003 al 22% nel 2013, e l’età media delle madri prima volta, inoltre, è aumentato, dal 27,8 anni, nel 2003, a 28.6 in 2013.1
Quarant’anni fa, l’età materna è stato l’unico strumento di screening disponibili per identificare le gravidanze a rischio per anomalie cromosomiche. Da allora, la disponibilità di test prenatali non invasivi sempre più economici e accurati ha fatto sì che le donne di tutte le età possano ora avere opzioni di test prenatali migliorate.
Di fronte alle molte opzioni per i test prenatali, alcune coppie potrebbero sentirsi sopraffatte, mentre i medici potrebbero trovare difficile tenere il passo con tutti i dettagli dei nuovi test. Ma la consulenza è fondamentale per garantire che le coppie siano pienamente consapevoli del processo di test da prospettive fisiche, emotive, pratiche e finanziarie.
La prima e più importante domanda da porre è: la coppia dovrebbe prendere in considerazione i test prenatali? Alcune coppie non discutono mai il problema fino a quando non rimangono incinte e molte non hanno mai considerato la possibilità di avere un bambino con un problema cromosomico, come la sindrome di Down, o un difetto alla nascita, come il labbro leporino.
D’altra parte, in questi giorni una migliore alfabetizzazione sanitaria significa che molte coppie sono informate e proattive, e alcune vogliono che ogni test sia disponibile per garantire che i loro bambini siano sani.
La prossima domanda riguarda quali test/i avere e se questi dovrebbero essere test di screening o diagnostici. Per definizione, un test di screening esamina una popolazione per identificare quegli individui a maggior rischio di avere una certa condizione, mentre un test diagnostico determina se un individuo ha una particolare condizione. Nel contesto dei test prenatali, i test di screening includono ecografie, screening biochimico e test prenatali non invasivi (NIPT), mentre i test diagnostici sono il campionamento dei villi coriali (CVS) e l’amniocentesi.
Infine, quando si parla alle coppie di test, ci sono le questioni pratiche di costo e accesso, che saranno influenzate in larga misura dallo stato socioeconomico del paziente. Molti servizi di ultrasuoni di alta qualità e altri test non sono rebatable Medicare e quindi insostenibile per alcuni pazienti.
Naturalmente, solo perché un test è disponibile non significa che dovrebbe essere eseguito, e le coppie che intraprendono i test prenatali devono farlo con gli occhi spalancati per evitare di finire su un giro sulle montagne russe da incubo quando vengono indirizzati per “tutti i test”.
A tal fine, la consulenza pre-test è vitale in modo che le coppie comprendano le possibilità materne legate all’età di un bambino con un grave problema cromosomico e possano quindi soppesarle con i rischi e i benefici dei vari test offerti.
Le coppie devono capire esattamente cosa i test possono e non possono rilevare e, soprattutto, esattamente perché stanno facendo il test. Domande difficili devono essere risolte in questa fase: considererebbero la cessazione di una gravidanza se a un feto fosse stata diagnosticata la sindrome di Down? Sarebbe la diagnosi informare la gestione e la pianificazione per la consegna se un feto con sindrome di Down è stato anche trovato per avere un grave difetto cardiaco che richiede chirurgia cardiaca neonatale?
Questo articolo considera due scenari di casi comuni e la gamma di opzioni di test prenatali disponibili per entrambi.
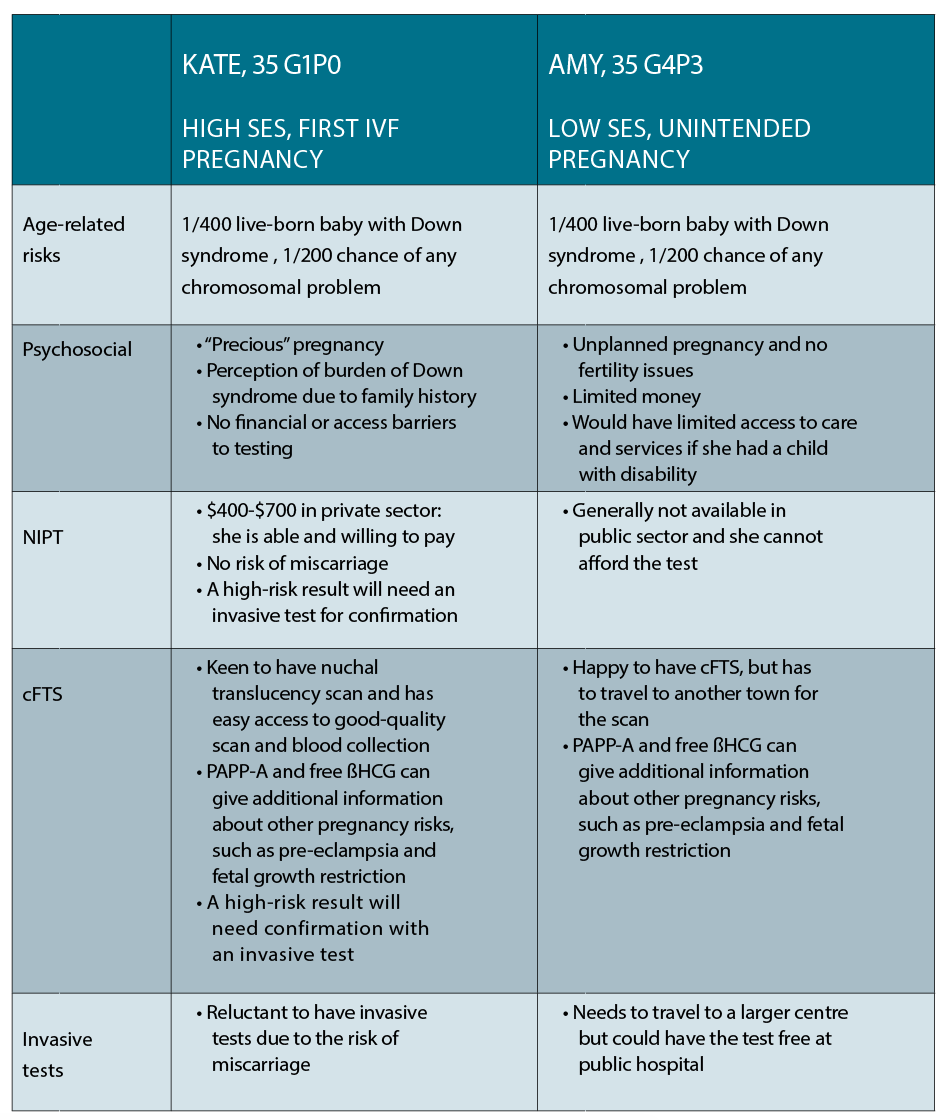
Caso 1
Kate è un avvocato aziendale di 35 anni che vive nel centro della città, che ha concepito la sua prima gravidanza al suo quarto ciclo di fecondazione in vitro. Ora è incinta di 10 settimane e vuole conoscere le opzioni a sua disposizione per la diagnosi prenatale. Ha un cugino con sindrome di Down ed è molto preoccupato per il proprio rischio di avere un bambino con la stessa condizione.
Case 2
Amy ha anche 35 anni e vive in una piccola città nel NSW. Lei e il suo partner hanno tre figli piccoli e stanno lottando finanziariamente, e lei è 10 settimane in una gravidanza non intenzionale. Vuole conoscere le sue opzioni per i test prenatali come uno dei suoi amici ha recentemente dato alla luce un bambino con sindrome di Down.

le Coppie hanno bisogno di capire esattamente ciò che il test può rilevare
suola in NON-INVASIVE TEST
L’inizio del primo trimestre, o dating, l’ecografia viene eseguita tra i sette e i 12 settimane, ed è utile per confermare la presenza di una valida gravidanza e determinare se c’è una gravidanza multipla. Permette anche accurata incontri di gestazione, aiuta ad escludere una gravidanza ectopica e localizzare la placenta. Non viene eseguito per rilevare difetti alla nascita.
Una scansione di traslucenza nucale viene eseguita tra 11 settimane e tre giorni e 13 settimane e sei giorni (lunghezza della groppa della corona fetale di 45-84mm), idealmente come parte dello “screening combinato del primo trimestre”. La traslucenza nucale è uno spazio pieno di liquido nella parte posteriore del collo fetale che può essere misurato mediante ultrasuoni. È ben noto che più ampia è la traslucenza nucale, maggiore è il rischio di anomalie fetali, inclusi problemi cromosomici come la sindrome di Down, nonché difetti cardiaci strutturali e alcuni disturbi genetici singoli.
Ad oggi, la raccomandazione è stata che la scansione della traslucenza nucale dovrebbe essere eseguita in combinazione con uno screening biochimico materno come uno schermo combinato del primo trimestre (CFTS), che misura PAPP-A e ßHCG libero per migliorare i tassi di rilevamento della sindrome di Down.
Da solo, la scansione della traslucenza nucale ha un tasso di rilevamento di circa il 65% al 70% per la sindrome di Down, e con l’aggiunta di marcatori sierici come PAPP-A e beta-HCG libero, entrambi riportati come multipli della mediana (MoMs), questo aumenta a circa il 90% con un tasso di falsi positivi del 5%.
Nella maggior parte dei casi, questi test saranno rassicuranti e offriranno tranquillità alle coppie senza mettere a rischio la gravidanza,
che può verificarsi con test invasivi come CVS o amniocentesi.
Con la disponibilità di test prenatali non invasivi, è sorto il dibattito sul valore dello screening combinato del primo trimestre per la sindrome di Down, anche se molti sostengono che la scansione di 12 settimane ha ancora un ruolo da svolgere nell’identificare anomalie strutturali e altri problemi che potrebbero influire negativamente sull’esito della gravidanza.2
Morfologia fetale L’ecografia viene eseguita a 18-20 settimane e può rilevare fino al 50% delle principali anomalie strutturali. Non è raccomandato come test di screening primario per la sindrome di Down. La sensibilità della scansione nel rilevare le malformazioni è influenzata da una serie di fattori, tra cui la natura della malformazione, l’abilità e l’esperienza dell’operatore, la qualità della macchina ad ultrasuoni, l’habitus del corpo materno e la posizione della placenta.
TEST PRENATALE NON INVASIVO
Un campione genetico fetale rilevabile nel sangue materno, che può essere testato per una diagnosi prenatale accurata, è stato a lungo il santo graal dei test prenatali. I miglioramenti nella tecnologia del DNA hanno infine portato alla capacità di isolare e misurare il DNA fetale circolante nel sangue materno.3
Circa il 10-15% del DNA nel sangue materno è di origine fetale e proviene da cellule fetali intatte e da DNA fetale circolante senza cellule (ccffDNA), derivato prevalentemente dalla degradazione delle cellule placentari. Il ccffDNA viene eliminato entro poche ore dalla consegna dalla circolazione materna e il DNA fetale rilevato durante una gravidanza, quindi, rappresenta il DNA del feto corrente.
NIPT comporta la misurazione dei frammenti cromosomici senza cellule e l’utilizzo delle differenze quantitative per distinguere le gravidanze di aneuploidia da quelle che non sono interessate. Ad esempio, i feti con sindrome di Down avranno un aumento misurabile e statisticamente significativo del numero di frammenti del cromosoma 21.
Tuttavia, come il campionamento dei villi coriali, il ccffDNA riflette il DNA placentare piuttosto che fetale, che deve essere preso in considerazione durante la consulenza e la discussione di potenziali opzioni di test invasivi. Ciò può restituire risultati citogeneticamente ambigui causati da fattori come il mosaicismo placentare.
Numerose aziende biotecnologiche hanno lanciato diverse piattaforme NIPT con nomi eufemistici come Harmony e Panorama, consentendo test prenatali non invasivi su larga scala per l’aneuploidia fetale, come la trisomia 13, 18 e 21 e anomalie comuni dei cromosomi sessuali, come la sindrome di Turner.
I principali vantaggi del NIPT sono che non è invasivo, disponibile da nove settimane di gestazione, e ha un’elevata sensibilità e specificità, sebbene per definizione sia uno screening piuttosto che un test diagnostico. Tuttavia, circa il 25% delle anomalie cromosomiche non sarà rilevato dal NIPT, e quindi test invasivi dovrebbero essere offerti alle donne ad aumentato rischio di un’anomalia cromosomica, ad esempio nel caso di una maggiore misurazione della traslucenza nucale o CFT, o quelle con un’anomalia strutturale rilevata su ultrasuoni.4
C’è anche un inconveniente pratico nell’impostazione australiana in quanto NIPT non è finanziato pubblicamente, portando a disuguaglianza di accesso. Non è ancora stabilito come il NIPT dovrebbe essere incorporato nella pratica di screening prenatale di routine, o quale sia il modo più economico per farlo.
Molti esperti attualmente sostengono il contingente modello di screening, secondo il quale tutte le donne hanno cFTS, e quelli ad alto rischio di sindrome di Down (>1/50) sono offerti test invasivi; quelli a rischio intermedio tra 1/50 e 1/300 a disposizione una scelta di NIPT o procedure invasive; e quelli a basso rischio (<1/300) sono rassicurati e non ha offerto ulteriori test.5
TEST INVASIVI O DIAGNOSTICI
Negli ultimi anni, il numero di procedure invasive di test prenatali è diminuito in modo significativo, principalmente a causa della disponibilità di test non invasivi migliorati.6 Le principali indicazioni per l’esecuzione di test invasivi sono ora per la diagnosi prenatale di disturbi monogenici (mendeliani), piuttosto che per la rilevazione di aneuploidia.
Il campionamento dei villi coriali è un test invasivo eseguito a 11-13 settimane di gravidanza, tramite un approccio trans-vaginale o trans-addominale, a seconda delle preferenze dell’operatore e della posizione della placenta. Il tasso di aborto spontaneo correlato alla procedura è basso (<1%), ma rimane comunque una barriera per alcune donne, specialmente in quelle con una storia di infertilità o perdita di gravidanza.
C’è un 1% di possibilità di ottenere un risultato inconcludente con CVS. Ciò è solitamente dovuto al mosaicismo placentare confinato, un fenomeno ben riconosciuto che può essere associato a un basso PAPP-A e a esiti avversi della gravidanza, inclusa la restrizione della crescita fetale e la perdita precoce della gravidanza, anche se il feto ha un cariotipo normale. Quando i risultati del CVS sono ambigui, vengono eseguiti ulteriori test-generalmente l’amniocentesi-per chiarire se l’anomalia cromosomica è veramente presente nel feto o è limitata alla placenta.
L’amniocentesi viene eseguita dopo 15 settimane ed è anche associata a un piccolo (<0.5%) rischio di aborto spontaneo. L’amniocentesi è considerata il gold standard, in quanto le cellule fetali ottenute dal liquido amniotico derivano da diversi tessuti fetali tra cui il tratto urinario e la pelle, e sono quindi più veramente rappresentative del cariotipo fetale rispetto a quelle ottenute dalla placenta. Lo svantaggio principale dell’amniocentesi rispetto al CVS è la tempistica successiva, e quindi la gestazione più avanzata, nel momento in cui vengono ricevuti i risultati.
Attualmente, la maggior parte dei laboratori diagnostici si è allontanata dall’analisi citogenetica (cariotipo) come test standard e ha adottato tecniche molecolari, tra cui la reazione a catena della polimerasi fluorescente quantitativa (QF-PCR). La QF-PCR è più economica e meno laboriosa rispetto all’analisi standard del cariotipo e i risultati sono ottenuti più rapidamente (entro 24-48 ore rispetto a 10-14 giorni) poiché la tecnica non richiede la coltura di cellule fetali.
Mentre la QF-PCR è in grado di diagnosticare le comuni aneuploidie che coinvolgono i cromosomi 13, 18, 21 e i cromosomi sessuali, non può rilevare altre rare anomalie cromosomiche. Inoltre, non può determinare se una trisomia è dovuta alla non disgiunzione (cioè aneuploidia comune e legata all’età) o alla traslocazione, che è più rara ma preoccupante, in quanto può essere ereditata e associata ad un aumento del rischio di recidiva nelle future gravidanze.
Il microarray cromosomico, noto anche come cariotipo molecolare, è ben consolidato come una delle principali indagini utilizzate per valutare neonati e bambini con anomalie strutturali e disabilità intellettiva. Analizza i cromosomi ad una risoluzione molto più alta (generalmente <2,5 kb o 250.000 coppie di basi) rispetto alla risoluzione da 5 MB a 10 MB di un cariotipo standard, o studio citogenetico, per rilevare piccole duplicazioni e delezioni cromosomiche.
Sempre più spesso, microarray viene utilizzato in ambito prenatale, dove può produrre risultati difficili da interpretare, indicati come “varianti di significato incerto”. Per questo motivo, il microarray cromosomico deve essere offerto solo con un’adeguata consulenza pre-e post-test e solo in situazioni in cui è clinicamente indicato. Nelle gravidanze ad alto rischio in cui è stata rilevata un’anomalia strutturale o un aumento della misurazione della traslucenza nucale, microarray ha dimostrato di migliorare la resa diagnostica di circa il 6%.7
La diagnosi genetica preimpianto è ora disponibile per i pazienti ad aumentato rischio di aneuploidia o di un singolo disturbo genetico. Essi sono ora in grado di sottoporsi a fecondazione in vitro e hanno embrioni biopsied e testati tramite diagnosi genetica preimpianto il quinto giorno, prima del trasferimento degli embrioni in utero.
La PGD viene sempre più utilizzata dalle coppie che desiderano evitare una gravidanza affetta da una particolare condizione genetica o anomalia cromosomica. Sebbene non sia accurato al 100%, la PGD può ridurre significativamente il rischio di avere una gravidanza affetta e quindi la necessità di considerare l’interruzione della gravidanza.
Esistono due tipi principali di diagnosi genetica preimpianto:
Test per l’aneuploidia: questo viene utilizzato per le coppie a rischio di aneuploidia a causa dell’età materna avanzata, della traslocazione parentale bilanciata, dell’aborto ricorrente e del fallimento dell’impianto;
Test per un singolo disturbo genetico: questo è usato in coppie a rischio di avere un bambino con un singolo disturbo genetico, tra cui condizioni autosomiche recessive, X-linked o autosomiche dominanti. In queste situazioni, la specifica diagnosi molecolare o del DNA deve essere identificata, prima che la PGD possa essere offerta.
È vitale che le coppie che considerano la FIV e la PGD siano indirizzate per una consulenza appropriata in quanto devono essere pienamente consapevoli del punto fisico, emotivo e finanziario rilevante per queste procedure.
Dr Kennedy è direttore MotherSafe RHW e docente congiunto Scuola di salute delle donne e dei bambini a UNSW
1. AIHW Australia’s mothers and babies 2013 in breve
2. McLennan A, Palma-Dias R, da Silva Costa F, et al. Test prenatali non invasivi nella pratica clinica di routine – un audit di NIPT e screening combinato del primo trimestre in una popolazione australiana non selezionata. ANZJOG 2016; 56: 22-28.
3. Lo YMD, Corbetta N, Chamberlain PF, Rai V, Sargent IL, Redman CWG, Wainscoat JS. 1997. Presenza di DNA fetale nel plasma materno e nel siero. Lancetta 350, 485-4874:
4. Petersen OB1, Vogel I, Ekelund C, Hyett J, Tabor A. Potenziali conseguenze diagnostiche dell’applicazione di test prenatali non invasivi: studio basato sulla popolazione da un paese con screening del primo trimestre esistente. Ultrasuoni Obstet Gynecol. 2014 Mar; 43 (3):265-71.
5. Hui L, Hyett J Test prenatali non invasivi per la trisomia 21; sfide per l’implementazione in Australia. ANZJOG 2013; 53 (5): 416-424.
6. Hui L, Muggli EE, Halliday JL. Tendenze basate sulla popolazione nello screening prenatale e nella diagnosi per l’aneuploidia: un’analisi retrospettiva di 38 anni di dati a livello statale. BJOG 2016; 123(1):90-7
7. Wapner RJ et al Chromosomal microarray versus karyotyping for prenatal diagnosis N Engl J Med 2012; 367:2175-2184

Leave a Reply