Composti covalenti
Ora hai una breve idea del perché i diversi elementi si comportano in modo diverso. Ma sai che una parte importante di esso è a causa della” natura ” dei legami nei composti. Proprio come te e i tuoi migliori amici hanno una serie di differenze dovute alle qualità “interne”, così è il caso dei composti ionici e covalenti. In questo capitolo, impareremo di più sul concetto di composti covalenti, esamineremo le loro proprietà e altro ancora.
Suggested Videos
What is a Covalent Compound?
Covalent compounds are the ones having strong intra-molecular bonds. Questo perché gli atomi all’interno delle molecole covalenti sono tenuti molto strettamente insieme. Ogni molecola è infatti abbastanza separata e la forza di attrazione tra le singole molecole in un composto covalente tende ad essere debole.
Abbiamo bisogno di pochissima energia nel separare le molecole. Ciò è dovuto alle forze attrattive tra le molecole con l’assenza di carica elettrica complessiva. I composti covalenti sono solitamente molecole gassose a temperatura e pressione ambiente. Potrebbero anche essere liquidi con bassi punti di ebollizione relativamente bassi.
Queste caratteristiche potrebbero essere attribuite alle loro deboli forze intermolecolari che tengono insieme questi atomi. Tuttavia, abbiamo anche molti composti covalenti solidi. Hanno bassi punti di fusione. Tuttavia, è interessante notare che un piccolo numero di questi ha una struttura completamente diversa. Formano enormi strutture in cui un numero enorme di atomi sono tenuti insieme. Ciò è possibile a causa della presenza di elettroni condivisi.
Queste strutture molecolari giganti sono fondamentalmente reticoli costituiti da molecole che sono tenuti insieme da legami covalenti struttura. Questi legami covalenti sono molto forti. Inoltre tendono ad essere molto duri con alti punti di fusione che sono diversi dalla maggior parte dei composti covalenti. L’esempio di questo tipo di composti covalenti comprende diamante e grafite di rete atomo di carbonio. Essi comprendono anche silice di silicio e atomi di ossigeno rete.
Scarica il Legame Chimico Cheat Sheet PDF facendo clic sul pulsante per il Download al di sotto


Sfoglia più Temi Legame Chimico E Struttura Molecolare
- Bond Parametri
- Fondamenti di Legame Chimico
- Ibridazione
- il Legame Idrogeno
- Ionica o Electrovalent Composti
- Orbitale Molecolare Teoria
- la Polarità dei Legami
- Strutture di Risonanza
- Legame di Valenza Teoria
- Teoria VSEPR
Proprietà generali dei composti covalenti
- I composti covalenti di solito hanno bassi punti di fusione. Un’eccezione a questo includono molecole di silice e diamanti che hanno un alto punto di fusione.
- Questi composti hanno bassi punti di ebollizione. Questo può essere attribuito alla loro debole forza di attrazione tra i vari atomi legati. Le forze di Van Der Waals legano questi atomi.
- Questi composti sono solitamente gas e liquidi con bassi punti di ebollizione e fusione.
- I composti covalenti solidi hanno strutture morbide come la grafite. Ciò è dovuto alla presenza di una nuvola di elettroni tra ogni strato di atomi di carbonio.
- Questi composti sono non conduttori di carica elettrica. L’assenza di ioni carichi è la ragione principale dietro questo. Un’eccezione a questo è la grafite, dove vediamo una nuvola di elettroni. Questi rendono la grafite un buon conduttore.
- Sono anche cattivi conduttori di calore. Le loro molecole mancano di elettroni liberi e ciò ostacola il flusso di energia termica.
- I composti covalenti non possiedono caratteristiche polari come proprietà generale. Pertanto, questi composti sono insolubili in acqua. Le molecole d’acqua non sono assolutamente neutre e hanno una leggera carica negativa sull’atomo di ossigeno e leggere cariche positive sugli atomi di idrogeno e poiché i composti covalenti sono costituiti da molecole neutre o molecole con leggere cariche e quindi non sono attratti fortemente dalle molecole d’acqua.
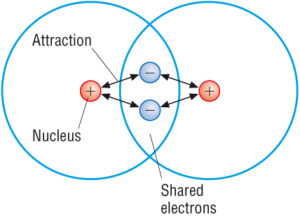
(Fonte: Google)
Proprietà fisiche e chimiche
- I composti covalenti liquidi evaporano. Ciò significa che le molecole di liquidi e solidi perde dalla loro superficie nell’aria.
- Questi composti hanno molto meno affinità tra le loro molecole.
- Vari composti covalenti hanno le loro molecole di forma caratteristica. I loro legami sono diretti ad angoli prestabiliti.
- Alcuni composti, in particolare i medicinali, sono solubili in acqua. Il resto è solubile in olio.
- La maggior parte dei composti covalenti non sono polari o hanno pochissima tendenza a dividersi completamente per formare ioni e quindi non condurre mai elettricità.
- A temperatura e pressione normali, troveremo questi composti come liquidi o gas. Ma ci sono anche solidi e hanno pesi molecolari più elevati.
- I cristalli di composti covalenti sono di due tipi: Uno che ha una debole forza di van der Waal che li tiene insieme come nello iodio. Questi sono facilmente fusibili e volatili L’altro con una grande rete di atomi che creano le macromolecole.
- Questi composti sono solubili in solventi organici come etere e benzene.
- I legami covalenti sono direzionali in natura. Pertanto, mostrano il fenomeno dell’isomerismo.
- Composti covalenti majorly hanno un tasso molto lento di reazioni, a differenza dei vari composti ionici.
Esempi risolti per te
Domanda: Perché i composti covalenti non sono solubili in acqua?
Risposta: Le molecole d’acqua non sono assolutamente neutre. Queste molecole hanno una leggera carica negativa sull’atomo di ossigeno e leggere cariche positive sugli atomi di idrogeno. D’altra parte, sappiamo che i composti covalenti sono costituiti da molecole neutre o molecole con leggere cariche. È per questo motivo che questi composti non sono fortemente attratti dalle molecole d’acqua.
Leave a Reply