CIMAvax-EGF: UN nuovo vaccino terapeutico per il cancro polmonare avanzato
RELAZIONE
CIMAvax-EGF: UN nuovo vaccino terapeutico per il cancro polmonare avanzato
Gisela González1, Agustin Lage1, Tania Crombet1, Gryssel Rodríguez1, Beatriz García1, Ariadna Cuevas1, Lisel Viña1, Norkis Arteaga1, Elia Neninger2
1Center di Immunologia Molecolare, CIMAve. 216 corner 15, Atabey, Playa, POBox 16 040, L’Avana, Cuba
2Hermanos Ameijeiras HospitalSan Lázaro # 701 e / Belascoín y Marqués González, Centro Habana, L’Avana City, Cuba.
ABSTRACT
Sono mostrati i risultati che consentono all’Agenzia di regolamentazione cubana (CECMED) di concedere la registrazione sanitaria al vaccino oncologico CIMAvax-EGF per il cancro polmonare avanzato non a piccole cellule (NSCLC). Questa è stata la prima registrazione di un vaccino terapeutico a Cuba e anche la prima registrazione di un vaccino contro il cancro del polmone nel mondo. Quindi, un vaccino terapeutico unico viene offerto ai pazienti affetti da cancro del polmone, che aumenterà la sopravvivenza e la loro qualità di vita. A tal fine, dovevano essere affrontate importanti sfide precliniche, cliniche, normative, produttive e negoziali. I risultati ottenuti in questi campi hanno portato a 18 articoli scientifici pubblicati su riviste ad alto impatto e 4 oggetti di invenzione, generando diversi brevetti a Cuba e in altri paesi. In ambito preclinico, sono stati dimostrati immunogenicità, sicurezza ed effetti antitumorali in diverse specie animali. L’esperienza clinica è iniziata nel 1995. Fino ad ora, cinque studi clinici di fase I-II si sono conclusi a Cuba, due di fase II si sono conclusi anche, uno a Cuba e un altro in Canada e nel Regno Unito, e uno studio di fase II-III con un programma ottimizzato, nonché uno studio di fase III sono attualmente in corso a Cuba. In campo normativo, è stata progettata ed eseguita una strategia di registrazione rapida. Ha richiesto nuove concezioni normative per sviluppare questo prodotto unico. È stato realizzato un processo produttivo scalabile, riproducibile e controllato, insieme a un sistema di qualità che ha garantito la piena conformità GMP. I fondi per lo sviluppo del prodotto provenivano dall’implementazione di una nuova strategia negoziale: la negoziazione di beni immateriali.
Keywords: Cancer vaccine, NSCLC, Fast-Track Registration, CIMAvax-EGF, Phase II-III Clinical Trial
INTRODUZIONE
La relazione tra il sistema formato dal recettore del fattore di crescita epidermico (EGFR) e i suoi ligandi con lo sviluppo del cancro è ben nota. Nei tumori di origine epidermoide, c’è una sovraespressione dell’EGFR che si riferisce a cattive prognosi e ricadute precoci dopo l’intervento chirurgico. Ecco perché questo sistema è diventato un obiettivo importante per le terapie antitumorali.
I meccanismi di proliferazione cellulare sono iniziati con il legame dell’EGF all’EGFR. Il nostro approccio terapeutico consiste in un vaccino con una formulazione EGF che lo rende immunogenico e induce una risposta immunitaria umorale. La produzione di anticorpi specifici anti-EGF che si legano all’EGF autologo, impedisce che si leghi all’EGFR innescando così i meccanismi di proliferazione cellulare derivati da tale interazione (1-4).
Qui riportiamo i risultati della registrazione a Cuba di questo vaccino (CIMAvax-EGF). Questo faceva parte di una strategia globale che comprendeva nuovi contributi clinici, normativi e tecnologici e aziendali, ed è supportato da 18 articoli scientifici internazionali e proprietà intellettuale in tutto il mondo. Descriviamo anche le innovazioni in diversi campi che hanno permesso la registrazione di CIMAvax-EGF a Cuba e in Perù.
RISULTATI E DISCUSSIONE
La vaccinazione con EGF è sicura, immunogenica e aumenta la sopravvivenza con una buona qualità di vita nei pazienti con carcinoma polmonare in stadio avanzato
L’esperienza clinica con CIMAvax-EGF nella terapia del carcinoma polmonare non a piccole cellule (NSCLC) in stadio avanzato è iniziata nel 1995. Fino ad ora, cinque studi clinici di fase I-II sono stati conclusi a Cuba; 2 studi clinici randomizzati di fase II sono stati conclusi, uno a Cuba e un altro in Canada e nel Regno Unito, e c’è uno studio di fase III in corso a Cuba. Più di 800 pazienti oncologici avanzati sono stati trattati con CIMAvax-EGF, dimostrando così di essere sicuro, immunogenico e in grado di aumentare la sopravvivenza con una buona qualità di vita.
L’obiettivo principale degli studi di fase I-II era quello di decidere la migliore formulazione vaccinale (proteina portante e adiuvante), la dose e il programma terapeutico. Questi risultati hanno dimostrato i vantaggi della proteina P64k come proteina portante e della Montanide ISA51 come adiuvante. E ‘stata dimostrata anche l’ aumentata immunogenicità del ridimensionamento della dose (5-7).
L’analisi dei dati aggregati di tutti gli studi di fase I-II ha mostrato un aumento significativo della sopravvivenza in pazienti con migliori risposte anticorpali o buoni risponditori anticorpali (GAR) e in pazienti con diminuzioni più pronunciate delle concentrazioni di sieri EGF () derivanti dalla vaccinazione. È stato inoltre dimostrato un aumento significativo della sopravvivenza di tutti i pazienti vaccinati rispetto a un controllo storico concomitante (7).
Uno studio clinico di fase II è stato condotto su 80 pazienti, che sono stati randomizzati a ricevere CIMAvax-EGF e la migliore terapia di supporto (BSC) (40 pazienti) o BSC da soli (40 pazienti), dopo aver concluso la chemioterapia di prima linea. I risultati precedenti sono stati corroborati in questo studio. Circa il 50% dei pazienti vaccinati erano GAR e sono sopravvissuti significativamente più dei pazienti che non hanno raggiunto la classificazione GAR (che sono stati classificati come poveri risponditori anticorpali, PAR). Allo stesso modo, i pazienti con la maggiore diminuzione sono sopravvissuti significativamente più del paziente che non ha mostrato questa diminuzione (Tabella 1). È stata osservata una significativa correlazione inversa tra i titoli anticorpali anti-EGF e, che si è verificata nei pazienti vaccinati ma non nei controlli, dimostrando così che è stata causata dalla vaccinazione (Figura 1).
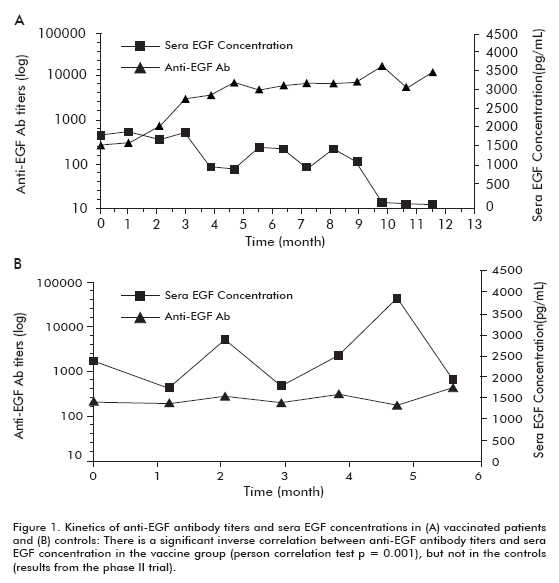
In tutti i pazienti vaccinati (18,53 ± 11,47; media ± mediana), rispetto ai controlli non vaccinati (7,55 ± 5.33), che era significativo nel gruppo di pazienti di 60 anni o più giovani (Log rank test; p < 0,05) (Figura 2) (8).
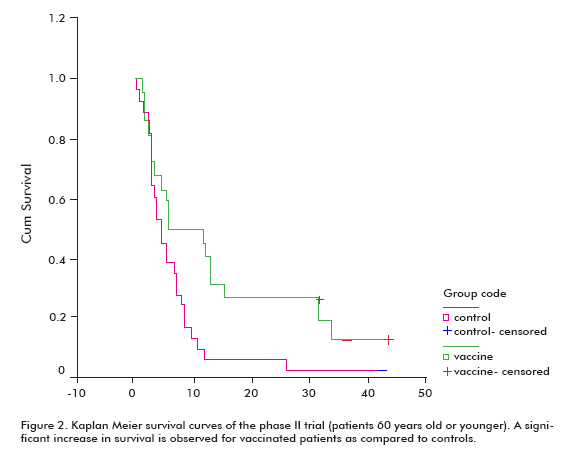
Come evidenziato in un test di competizione in vitro, i sieri di pazienti vaccinati hanno inibito il legame dell’EGF con l’EGFR. Questa inibizione di legame era proporzionale ai titoli anticorpali e alla sopravvivenza. Inoltre, i sieri di pazienti vaccinati hanno inibito la fosforilazione dell’EGFR in proporzione ai suoi titoli anticorpali anti-EGF.
È stato studiato il riconoscimento preferenziale del sito di legame EGF/EGFR (loop B della molecola EGF). I pazienti i cui sieri riconoscono preferenzialmente l’anello B sono sopravvissuti significativamente più dei pazienti che non hanno riconosciuto questo epitopo (9).
Si è recentemente concluso a Cuba uno studio di ottimizzazione dose / schedule (fase I-II). Nella sua progettazione, sono stati considerati tutti gli elementi che aumentano l’immunogenicità negli studi precedenti, che includevano: Montanide ISA51 come adiuvante, aumento delle dosi, quattro siti di iniezione e somministrazione di due dosi di vaccino prima della chemioterapia di prima linea, seguita dalla vaccinazione. I risultati di questo studio hanno dimostrato un significativo aumento di immunogenicità, con un 95% di GAR raggiungendo dieci volte i precedenti titoli anticorpali massimi. Tutti i pazienti vaccinati sono sopravvissuti significativamente più dei controlli dello studio di fase II (10).
È stata riscontrata anche una maggiore capacità dei sieri dei pazienti di inibire il legame EGF/EGFR e la fosforilazione di EGFR. Al settimo mese, dopo aver concluso la chemioterapia, la risposta anticorpale si è spostata verso l’anello B della molecola EGF, il che potrebbe indicare un miglioramento della qualità della risposta immunitaria. I risultati di questo studio hanno dimostrato che esiste un margine di miglioramento nella risposta a CIMAvax-EGF che può essere raggiunto manipolando la dose e lo schema terapeutico (10).
I risultati di questi studi sono stati convalidati in uno studio di fase III attualmente in corso a Cuba.
Progettazione e implementazione di una strategia normativa per la registrazione del vaccino per renderlo disponibile a tutti i pazienti con tumore polmonare avanzato non a piccole cellule
CIMAvax-EGF è un vaccino terapeutico per il cancro del polmone unico al mondo. Una strategia globale è stata progettata e implementata; è stata guidata da requisiti normativi, per la registrazione veloce a Cuba. Una stretta relazione tra lo sponsor (CIM) e l’Agenzia di regolamentazione cubana (CECMED) aveva lo scopo di stabilire i requisiti per ottenere un prodotto e la sua rapida applicazione a beneficio di pazienti oncologici avanzati senza altre alternative terapeutiche. Questa strategia comprendeva la progettazione di un sistema di qualità, i controlli di qualità e le specifiche, nonché i requisiti GMP per coprire le diverse fasi dello sviluppo del prodotto. Questa strategia globale può essere utilizzata nello sviluppo di altri prodotti simili.
L’esperienza normativa accumulata e la documentazione hanno portato all’approvazione di studi clinici in diversi paesi. Il fascicolo contenente tutte le informazioni ha permesso di registrare CIMAvax-FEG a Cuba e in Perù. Possiamo quindi affermare che abbiamo una strategia definita per la registrazione delle droghe in diversi paesi.
Il processo di produzione GMP che genera un prodotto scalabile, coerente e conforme alle specifiche
La prima sfida per progettare un processo di produzione per CIMAvax-EGF è stata quella di avere un preparato EGF immunogenico. È stato ottenuto dalla coniugazione chimica dell’EGF ricombinante umano alla proteina di membrana ricombinante, P64k (da Neisseria meningitidis). Il coniugato viene iniettato insieme ad un adiuvante appropriato (attualmente, Montanide ISA 51 di Seppic, Francia).
È stato inizialmente progettato un processo su scala di laboratorio. Un processo sanitario e riproducibile scalabile (e scalabile) è stato successivamente progettato e implementato, in conformità con le linee guida GMP. Sono stati inoltre progettati e implementati saggi analitici in vitro e in vivo per valutare la qualità delle materie prime e dei prodotti intermedi e finali.
Tutte le modifiche sono state valutate e supportate dall’attuale strategia normativa. I risultati dello studio di equivalenza, per confrontare entrambi i prodotti, hanno ricevuto l’approvazione da parte di CECMED della domanda di processo in scala e l’approvazione del prodotto ottenuto in questo processo per il suo uso clinico. Lo scaling-up e l’ottimizzazione del processo produttivo hanno lasciato il posto a una pubblicazione (11) e a un nuovo oggetto di invenzione, con brevetti successivamente presentati in diversi paesi.
Negoziazione di beni immateriali ci ha concesso fondi per lo sviluppo di progetti e anche l’esperienza di apprendimento nel nostro lavoro congiunto con le autorità di regolamentazione di diversi paesi
Questo progetto è stato negoziato con controparti straniere sulla base del nuovo concetto di “negoziazione di beni immateriali”, supportato principalmente attraverso la proprietà intellettuale del nostro prodotto che era Questa strategia di negoziazione consisteva nel concedere in licenza il progetto per il suo sviluppo congiunto con altri paesi, il che significa che le controparti straniere coprivano le spese delle azioni normative e degli studi clinici nei loro territori. Come risultato di questi negoziati, Cuba ha ricevuto pagamenti per le pietre miliari. Questa modalità di negoziazione ci ha permesso anche di avere uno scambio costante con specialisti qui e all’estero, aumentando così la nostra esperienza. I nostri risultati positivi con questa modalità di negoziazione potrebbero essere applicati ad altri prodotti in corso nel nostro paese.
RILEVANZA DELLO STUDIO
CIMAvax-EGF è il primo vaccino terapeutico per il trattamento del cancro registrato a Cuba e il primo registrato al mondo per la terapia del cancro del polmone. Il cancro ai polmoni è un problema di salute irrisolto con più di 1,3 milioni di casi diagnosticati ogni anno e lo stesso numero di morti in tutto il mondo. A Cuba, è la principale causa di morte per cancro in entrambi i sessi con un’incidenza di oltre 4000 morti all’anno. La terapia di scelta per i pazienti diagnosticati in fase avanzata è quella della chemioterapia di prima linea, che può essere somministrata in concomitanza con la radioterapia. Si tratta di un trattamento palliativo, non curativo, con una risposta completa alla chemioterapia molto rara e risposte oggettive (complete o parziali) che si verificano solo nel 25% dei pazienti.
CIMAvax-EGF offre un trattamento alternativo per questi pazienti che hanno già ricevuto chemioterapia di prima linea. I gravi eventi avversi dei trattamenti chemioterapici e / o radioterapici sono ben noti e peggiorano gravemente la qualità della vita. Invece, la vaccinazione con CIMAvax-EGF genera solo eventi avversi lievi o moderati, piuttosto che gravi, che possono essere risolti con le cure di supporto convenzionali, migliorando al contempo la sopravvivenza dei pazienti con cancro polmonare avanzato e offrendo una buona qualità di vita.
Fino ad ora, più di 800 cubani sono stati trattati con CIMAvax-EGF in più di 20 ospedali in tutto il paese. La registrazione di CIMAvax-EGF consente di estenderlo a tutti i pazienti del paese a cui è stato diagnosticato un cancro polmonare avanzato; rendendo così Cuba il primo paese al mondo con un programma nazionale che utilizza questa alternativa terapeutica.
Per quanto riguarda i benefici economici, attraverso i negoziati di questo progetto abbiamo ottenuto 6.346 milioni di dollari. La strategia negoziale del progetto è per il suo sviluppo congiunto con altri paesi, il che significa che la controparte straniera copre le spese degli studi clinici nel proprio paese, rendendolo accessibile. Queste prove richiedono investimenti di milioni di USD, e questo è possibile solo se è supportato da controparti straniere. Allo stesso tempo, questa strategia offre più dati clinici a Cuba, senza le spese di realizzazione delle prove qui. Fino ad ora, gli studi clinici sono stati eseguiti in Canada, Regno Unito e Malesia. Nel prossimo futuro inizieranno gli studi clinici in Cina e in Europa.
Inoltre, come parte di questa strategia di licenza, le controparti straniere sono responsabili della registrazione del prodotto nelle regioni in cui hanno diritti commerciali. Durante i processi di registrazione e marketing, Cuba riceverà pagamenti per le pietre miliari e in seguito, come royalties di vendita.
Il mercato mondiale dei vaccini contro il cancro è considerato nell’ordine di miliardi di dollari. Il fatto che Cuba abbia un prodotto unico per il trattamento avanzato del cancro del polmone può fornirci un potenziale di esportazione che può finanziare l’uso di questo prodotto nel nostro sistema sanitario nazionale.
CONCLUSIONI
La vaccinazione con CIMAvax-EGF è sicura, immunogenica e porta ad un aumento della sopravvivenza con una buona qualità della vita nei pazienti con tumori polmonari in fase avanzata. La progettazione e l’implementazione di una strategia normativa per la registrazione di questo vaccino lo ha reso disponibile
per tutti i casi di pazienti con cancro polmonare avanzato non a piccole cellule a Cuba. Questa esperienza positiva potrebbe essere applicabile ad altri prodotti simili in corso di realizzazione. È stato sviluppato un processo di produzione scalabile, coerente e riproducibile e conforme alle linee guida GMP, per generare un prodotto conforme alle specifiche. L’esperienza nella negoziazione di beni immateriali è stata molto positiva e ci ha concesso fondi per lo sviluppo di progetti, supportando al contempo l’esperienza di apprendimento derivata dal lavoro congiunto con le autorità di regolamentazione di diversi paesi.
RINGRAZIAMENTI
Gli autori vogliono ringraziare i seguenti specialisti del Centro di Immunologia Molecolare per il loro contributo a questo lavoro: Rolando Pérez, Loany Calvo, Suhamy Attenzione, Belinda Sánchez, Irene Beausoleil, Ernesto Chico, Airama Alvisa, Ileana Cartroman, Sergio Degustazione, Ana Veloso, Reinaldo Corvo, Yanelda Lopez, Yosniel Hernández, Antonio Vallin, Alejandro Portillo, Liuva Legno, Guido Ferrer, Diana Borges, Niuvis Pérez, Tamara García, Idaine Bacino, Mayra Santaelena, Joaquin Solozabal, Aida Rodriguez, Maria Elena Garcia, Addis Torres, Eric Chong, Carmen Roll, Mauritius Catala, Soraida Acosta, Barbara Wilkinson, Olga Torres, Normando Iznaga tutti del Centro di Immunologia Molecolare, e anche a Daniele González, Lourdes B Costa, Galina M Moya, Rolando Páez, Gerardo Guillén, Vivian Pujol, Dinorah Torres del Centro di Ingegneria Genetica e Biotecnologia.
1. González G, Montero E, León K, Cohen IR, Lage A. Autoimmunizzazione al fattore di crescita epidermico, un componente dell’omuncolo imunologico. Autoimmun Rev 2002;1:89-95.
2. Lage A, Crombet T, González G. Targeting epidermal growth factor receptor signalling: primi risultati e tendenze future in oncologia. Ann Med 2003;5(35):327-36.
3. González G e Lage A. Vaccini contro il cancro per l’immunodeprivazione ormonale: L’approccio al vaccino EGF: argomenti principali nella ricerca sul cancro, Capitolo 11, Ed Nova Publishers, 2007.
4. González G e Lage A. Vaccini contro il cancro per l’ormone / fattore di crescita deprivazione immunitaria: un approccio fattibile per il trattamento del cancro. Curr Cancer Drug Targets 2007;7: 229-41.
5. González G, Crombet T, Torres F, Catala M, Alfonso L, Osorio M, et al. Vaccino contro il cancro basato sul fattore di crescita epidermico per la terapia del cancro polmonare non a piccole cellule. Ann Oncol 2003;14:461-6.
6. Crombet T, Neninger E, Catalá M, García B, Leonard I, Martínez L, et al. Trattamento di pazienti con NSCLC con un vaccino antitumorale a base di EGF. Relazione di uno studio di fase I. Cancro Biol Ther 2006;5 (2): 136-41.
7. González G, Crombet T, Neninger E, Viada C, Lage A. Vaccinazione terapeutica con fattore di crescita epidermico (EGF) nel carcinoma polmonare avanzato: analisi di dati aggregati provenienti da tre studi clinici. Hum Vaccines 2007;3(1): 8-13.
8. Neninger E, De la Torre A, Osorio M, Catald M, Bravo I, Mendoza M, et al. Studio controllato randomizzato di fase II di un vaccino contro il fattore di crescita epidermico nel carcinoma polmonare non a piccole cellule avanzato. J Clin Oncol 2008;26: 1452-8.
9. García B, Neninger E, De la Torre A, Leonard I, Martínez R, Viada C, et al. L’efficace inibizione del legame del recettore del fattore di crescita epidermico/fattore di crescita epidermico da parte degli anticorpi anti-epidermici del fattore di crescita è correlata a una migliore sopravvivenza nei pazienti con cancro polmonare non a piccole cellule avanzati trattati con il vaccino del fattore di crescita epidermico. Clin Cancer Res 2008; 14 (3): 840-6.
10. Neninger E, Verdecia BG, Crombet T, Viada C, Pereda S, Leonard I, et al. Combinazione di un vaccino antitumorale a base di EGF con chemioterapia nel carcinoma polmonare non a piccole cellule avanzato. J Immunother 2009; 32: 92-9.
11. A, A, A, A, A, A, A, A, A, A, A, et al. Sviluppo del processo di produzione per un vaccino antitumorale basato sul fattore di crescita epidermico. Bio-pharm Int, Vaccini Suppl, ottobre 2008.
Leave a Reply