Chimica inorganica
La chimica inorganica descrittiva si concentra sulla classificazione dei composti in base alle loro proprietà. In parte la classificazione si concentra sulla posizione nella tavola periodica dell’elemento più pesante (l’elemento con il più alto peso atomico) nel composto, in parte raggruppando i composti per le loro somiglianze strutturali.
Classificazioni della chimica inorganica:
Coordinamento compoundsEdit
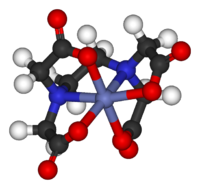
Classica composti di coordinazione funzione di metalli legata al “solitario coppie di elettroni che risiedono sul gruppo principale atomi di ligandi come H2O, NH3, Cl−, e CN−. Nei moderni composti di coordinazione quasi tutti i composti organici e inorganici possono essere usati come ligandi. Il “metallo” di solito è un metallo dei gruppi 3-13, così come i trans-lantanidi e i trans-attinidi, ma da una certa prospettiva, tutti i composti chimici possono essere descritti come complessi di coordinazione.
La stereochimica dei complessi di coordinazione può essere piuttosto ricca, come accennato dalla separazione di Werner di due enantiomeri di 6+, una prima dimostrazione che la chiralità non è inerente ai composti organici. Un tema di attualità all’interno di questa specializzazione è la chimica di coordinazione supramolecolare.
- Esempi: −, 3+, TiCl4(THF)2.
gruppo Principale compoundsEdit

Queste specie dotate di elementi dei gruppi I, II, III, IV, V,VI, VII, 0 (escluso idrogeno) della tavola periodica. A causa della loro reattività spesso simile, gli elementi del gruppo 3 (Sc, Y e La) e del gruppo 12 (Zn, Cd e Hg) sono generalmente inclusi, e talvolta anche i lantanidi e gli attinidi.
I composti del gruppo principale sono noti fin dagli inizi della chimica, ad esempio lo zolfo elementare e il fosforo bianco distillabile. Gli esperimenti sull’ossigeno, O2, di Lavoisier e Priestley non solo hanno identificato un importante gas biatomico, ma hanno aperto la strada alla descrizione di composti e reazioni secondo rapporti stechiometrici. La scoperta di una sintesi pratica di ammoniaca utilizzando catalizzatori di ferro da Carl Bosch e Fritz Haber nei primi anni del 1900 ha profondamente influenzato l’umanità, dimostrando il significato della sintesi chimica inorganica.I composti tipici del gruppo principale sono SiO2, SnCl4 e N2O. Molti composti del gruppo principale possono anche essere classificati come “organometallici”, in quanto contengono gruppi organici, ad esempio, B(CH3)3). I composti del gruppo principale si trovano anche in natura, ad esempio il fosfato nel DNA, e quindi possono essere classificati come bioinorganici. Al contrario, i composti organici privi di (molti) ligandi di idrogeno possono essere classificati come “inorganici”, come i fullereni, i buckytubes e gli ossidi di carbonio binari.
- Esempi: tetrasulfur tetranitride S4N4, diborano B2H6, siliconi, buckminsterfullerene C60.
Composti di metalli di transizionemodifica
I composti contenenti metalli del gruppo 4-11 sono considerati composti di metalli di transizione. I composti con un metallo del gruppo 3 o 12 sono talvolta incorporati in questo gruppo, ma anche spesso classificati come composti del gruppo principale.
I composti di metalli di transizione mostrano una ricca chimica di coordinazione, che varia dal tetraedrico per il titanio (ad esempio, TiCl4) al quadrato planare per alcuni complessi di nichel all’ottaedrico per i complessi di coordinazione del cobalto. Una gamma di metalli di transizione può essere trovata in composti biologicamente importanti, come il ferro nell’emoglobina.
- Esempi: ferropentacarbonile, tetracloruro di titanio, cisplatino
Organometallici compoundsEdit

di Solito, composti organometallici sono considerati per contenere la M-C-H gruppo. Il metallo (M) in queste specie può essere un elemento di gruppo principale o un metallo di transizione. Operativamente, la definizione di un composto organometallico è più rilassata per includere anche complessi altamente lipofili come carbonili metallici e persino alcossidi metallici.
I composti organometallici sono principalmente considerati una categoria speciale perché i ligandi organici sono spesso sensibili all’idrolisi o all’ossidazione, rendendo necessario che la chimica organometallica impieghi metodi preparativi più specializzati di quelli tradizionali nei complessi di tipo Werner. La metodologia sintetica, in particolare la capacità di manipolare complessi in solventi a basso potere di coordinamento, ha permesso l’esplorazione di leganti molto debolmente coordinanti come idrocarburi, H2 e N2. Poiché i ligandi sono petrolchimici in un certo senso, l’area della chimica organometallica ha notevolmente beneficiato della sua rilevanza per l’industria.
- Esempi: Cyclopentadienyliron dicarbonyl dimer (C5H5)Fe(CO)2CH3, ferrocene Fe(C5H5)2, molybdenum hexacarbonyl Mo(CO)6, triethylborane Et3B, Tris(dibenzylideneacetone)dipalladium(0) Pd2(dba)3)
Cluster compoundsEdit
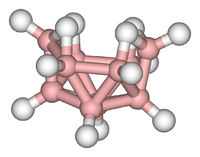

I cluster possono essere trovati in tutte le classi di composti chimici. Secondo la definizione comunemente accettata, un cluster consiste in minima parte di un insieme triangolare di atomi che sono direttamente legati l’uno all’altro. Ma i complessi dimetallici legati al metallo-metallo sono molto rilevanti per l’area. I cluster si verificano nei sistemi inorganici “puri”, nella chimica organometallica, nella chimica dei gruppi principali e nella chimica bioinorganica. La distinzione tra cluster molto grandi e solidi sfusi è sempre più sfocata. Questa interfaccia è la base chimica della nanoscienza o della nanotecnologia e deriva specificamente dallo studio degli effetti di dimensione quantistica nei cluster di selenidi di cadmio. Pertanto, i grandi cluster possono essere descritti come una matrice di atomi legati di carattere intermedio tra una molecola e un solido.
- Esempi: Fe3(CO)12, B10H14, 2−, 4Fe-4S
Bioinorganica compoundsEdit

Per definizione, questi composti si trovano in natura, ma il sottocampo comprende specie antropogeniche, come inquinanti (ad esempio, metilmercurio) e farmaci (ad esempio, Cisplatino). Il campo, che incorpora molti aspetti della biochimica, include molti tipi di composti, ad esempio i fosfati nel DNA e anche complessi metallici contenenti ligandi che vanno dalle macromolecole biologiche, comunemente peptidi, a specie mal definite come l’acido umico e l’acqua (ad esempio, coordinati ai complessi di gadolinio impiegati per la risonanza magnetica). Tradizionalmente la chimica bioinorganica si concentra sul trasferimento di elettroni ed energia nelle proteine rilevanti per la respirazione. La chimica inorganica medicinale comprende lo studio di elementi sia non essenziali che essenziali con applicazioni alla diagnosi e alle terapie.
- Esempi: emoglobina, metilmercurio, carbossipeptidasi
Composti allo stato solidomodifica
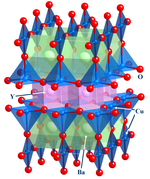
Questo importante settore si concentra sulla struttura, bonding, e le proprietà fisiche dei materiali. In pratica, la chimica inorganica allo stato solido utilizza tecniche come la cristallografia per ottenere una comprensione delle proprietà che derivano dalle interazioni collettive tra le subunità del solido. Inclusi nella chimica dello stato solido sono i metalli e le loro leghe o derivati intermetallici. I campi correlati sono la fisica della materia condensata, la mineralogia e la scienza dei materiali.
- Esempi: chip di silicio, zeoliti, YBa2Cu3O7
Leave a Reply