3.4: Rutherford’s Experiment-The Nuclear Model of the Atom
Atomi e oro
Nel 1911, Rutherford e colleghi Hans Geiger e Ernest Marsden iniziarono una serie di esperimenti innovativi che avrebbero cambiato completamente il modello accettato dell’atomo. Hanno bombardato fogli molto sottili di lamina d’oro con particelle alfa in rapido movimento.


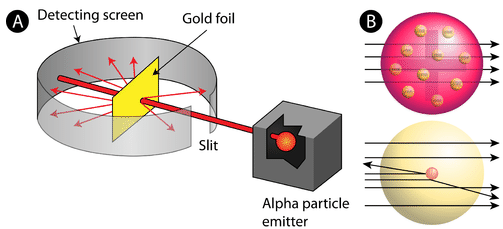
Figura \(\PageIndex{2}\) (A) La configurazione sperimentale per l’esperimento della lamina d’oro di Rutherford: un elemento radioattivo che emetteva particelle alfa era diretto verso un sottile foglio di lamina d’oro circondato da uno schermo che consentiva il rilevamento delle particelle deviate. (B) Secondo il modello plum pudding (in alto) tutte le particelle alfa dovrebbero essere passate attraverso la lamina d’oro con poca o nessuna deflessione. Rutherford ha scoperto che una piccola percentuale di particelle alfa sono state deviate a grandi angoli, che potrebbe essere spiegato da un atomo con un piccolo, denso, nucleo positivamente carica al suo centro (in basso).
Secondo il modello atomico accettato, in cui la massa e la carica di un atomo sono distribuite uniformemente in tutto l’atomo, gli scienziati si aspettavano che tutte le particelle alfa passassero attraverso la lamina d’oro con solo una leggera deflessione o nessuna. Sorprendentemente, come mostrato nella figura \ (\PageIndex{2}\) (mentre la maggior parte delle particelle alfa erano effettivamente non riflesse, una percentuale molto piccola (circa 1 su 8000 particelle) rimbalzava sulla lamina d’oro ad angoli molto grandi. Alcuni sono stati anche reindirizzati indietro verso la fonte. Nessuna conoscenza precedente li aveva preparati per questa scoperta. In una famosa citazione, Rutherford esclamò che era ” come se avessi sparato un guscio da 15 pollici a un pezzo di tessuto ed è tornato e ti ha colpito.”
Rutherford aveva bisogno di trovare un modello completamente nuovo dell’atomo per spiegare i suoi risultati. Poiché la stragrande maggioranza delle particelle alfa era passata attraverso l’oro, ragionò che la maggior parte dell’atomo era spazio vuoto. Al contrario, le particelle che erano altamente deviate devono aver sperimentato una forza tremendamente potente all’interno dell’atomo. Concluse che tutta la carica positiva e la maggior parte della massa dell’atomo dovevano essere concentrate in uno spazio molto piccolo all’interno dell’atomo, che chiamò nucleo. Il nucleo è il piccolo, denso, nucleo centrale dell’atomo ed è composto da protoni e neutroni.
Il modello atomico di Rutherford divenne noto come modello nucleare. Nell’atomo nucleare, i protoni e i neutroni, che comprendono quasi tutta la massa dell’atomo, si trovano nel nucleo al centro dell’atomo. Gli elettroni sono distribuiti attorno al nucleo e occupano la maggior parte del volume dell’atomo. Vale la pena sottolineare quanto piccolo sia il nucleo rispetto al resto dell’atomo. Se potessimo far saltare in aria un atomo delle dimensioni di un grande stadio di calcio professionale, il nucleo sarebbe delle dimensioni di un marmo.
Il modello di Rutherford si rivelò un passo importante verso una piena comprensione dell’atomo. Tuttavia, non affrontava completamente la natura degli elettroni e il modo in cui occupavano il vasto spazio attorno al nucleo. Per questa e altre intuizioni, Rutherford ha ricevuto il premio Nobel per la chimica nel 1908. Sfortunatamente, Rutherford avrebbe preferito ricevere il premio Nobel per la Fisica perché considerava la fisica superiore alla chimica. Secondo lui, ” Tutta la scienza è fisica o collezionismo di francobolli.”
Leave a Reply