Håndtering af kemoterapi Ekstravasationer
US Pharm. 2009; 34 (9) (onkologi suppl): 3-11. abstrakt: intravenøs (IV) kemoterapeutisk medicin har potentialet til at forårsage ekstravasationsskade eller vævsnekrose på indgivelsesstedet. Selvom et flertal af ekstravasationer kan forhindres ved korrekt og grundig infusionsadministration, er flere modgift blevet anerkendt og undersøgt for at forhindre yderligere vævsskade.
Infiltration og ekstravasation er to velkendte, tydelige komplikationer ved IV-infusionsterapi. Ifølge Infusion Nurses Society og Oncology Nursing Society involverer begge komplikationer utilsigtet lækage af en IV-opløsning i det omgivende væv; imidlertid adskiller typen af opløsning sig. Infiltration er utilsigtet administration af en ikke-vesikant eller irriterende opløsning eller medicin i det omgivende væv.1,2 Nonvesicants er midler, der sjældent producerer akutte reaktioner eller ødelægger vævet, når de infiltrerer. Irriterende stoffer kan fremkalde smerter på injektionsstedet eller langs venen, med eller uden en inflammatorisk reaktion, normalt uden vedvarende vævsskade. Irriterende stoffer kan dog kun forårsage sår i blødt væv, hvis en stor mængde koncentreret lægemiddelopløsning utilsigtet ekstravaseres for at inducere inflammatoriske reaktioner uden vedvarende vævsskade.3,4
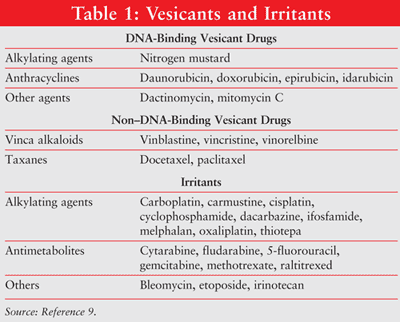
ekstravasation henviser til utilsigtet instillation eller lækage af vesikantmateriale i de perivaskulære og subkutane rum under administration af medicin.1,2 ekstravasation resulterer i lokale reaktioner lige fra lokal irritation til svær vævsnekrose i huden, omgivende vaskulatur og understøttende strukturer.5-8 kemoterapeutiske midler kan klassificeres, baseret på deres potentiale til at forårsage lokal vævsskade, som vesikanter, irritanter eller nonvesicants. (Flere vesikanter og irritanter er beskrevet i tabel 1.9) den utilsigtede ekstravasation af IV-lægemidler forekommer i cirka 0,1% til 6% af perifere IV-infusioner og 0,3% til 4,7% af implanterede venøse adgangsportinfusioner.10-12
Patofysiologi af vævsskade
omfanget af vævsskade afhænger af det kemoterapeutiske middels bindingskapacitet til DNA. DNA-bindemidler omfatter antracykliner, antitumorantibiotika, platinanaloger og nogle alkyleringsmidler.3,4 DNA-bindende antineoplastik forårsager vævsskade ved formering af dødelig DNA-tværbinding eller strengbrud forårsaget af frie radikaler, hvilket fører til celleapoptose.13-17 ikke-DNA-bindende antineoplastik (f. eks., vinca alkaloider, taksaner, topoisomerasehæmmere) interfererer med mitose. Ikke-DNA-bindemidler fjernes lettere fra ekstravasationssteder og forårsager mindre vævsskade end DNA–bindemidler.17
risikofaktorer for ekstravasation
risici for ekstravasation er multifaktorielle og kan stort set ændres. Mange af disse risici stammer fra fejl i enhedens brug og placering. IV – enhedsfaktorer, der påvirker ekstravasationsrisiko, inkluderer nålemateriale (dvs.metal), kanylestørrelse (stor plast vs. lille plast) og katetertype (dvs. centralt venekateter). Metal nåle kan forårsage mere skade på indsættelse og er ufleksibel i beholderen, mens store gauge nåle kan hindre blodgennemstrømningen, bremse fortynding af infusate.18,19 ekstravasation fra CVC ‘ er kan forekomme med nåleforskydning fra en implanteret venøs adgangsport (IVAP), mekanisk okklusion og efterfølgende CVC-skade, katetermigration eller dannelse af fibrinhylster og trombose. Forkert placering af IVAP forekommer mere sandsynligt hos patienter med nye enheder, dem med betydelig postoperativ hævelse og overvægtige patienter eller store brystkvinder.20 mekaniske okklusioner kan skyldes dannelse af thrombus, medikamentfældning, retrograd kateterforskydning eller klemning (dvs.en intermitterende og positionel kateterokklusion; det skal mistænkes, hvis infusionsokklusion kan lindres ved at lade patienten bevæge deres armpositionering).2,21,22 undgåelse af ekstravasation afhænger i høj grad af korrekt vedligeholdelse af IV-stedet og sikring af, at den korrekte infusionshastighed implementeres. Disse risikofaktorer er relateret til de anvendte antineoplastik, patienterne og klinikeren, der administrerer lægemidlet.
forebyggelse
tæt overvågning af patienter og uddannelse af både patienter og praktiserende læger om risici og håndtering af vesikant ekstravasation synes at være hjørnestenene i forebyggelse. Mens læger bærer ansvaret for at skrive nøjagtige ordrer, sygeplejersker er ansvarlige for at sikre dygtig og korrekt placering af udstyr og overvågning af kemoterapiinfusioner visuelt og gennem patientsamtaler. Under administration af vesicant skal stedet overvåges for hævelse, rødme og smerte. Vesikanter skal administreres i overensstemmelse med fabrikantens anbefalinger (f.eks. korrekt fortynding, specificeret administrationstid). IV-linjer skal skylles før og efter administration af kemoterapi. Apotekets rolle ville være at hjælpe med at udvikle politikker, der sikrer korrekt verifikation, mærkning og udlevering af kemoterapeutiske midler. En måde, dette kan udføres på, er at bruge diskriminerende mærkning ved udlevering af vesicant antineoplastik, så sygeplejersker bruger de passende forholdsregler. Apotekere kan spille en integreret rolle i uddannelsen ved at give lægemiddelinformation og rutinemæssige tjenester til alle medlemmer af sundhedsvæsenet om korrekt brug og administration af de forskellige kemoterapeutiske midler. Der skal anvendes en tværfaglig samarbejdsmetode for at sikre, at sikker praksis implementeres. Administration af kemoterapi hos patienter kræver korrekt uddannelse af personale og uddannelse af patienter og administrativ støtte gennem implementering af politik.2,23
dokumentation af hændelser
hver hændelse med ekstravasation skal dokumenteres og rapporteres grundigt. Dokumentation tjener flere formål, herunder at give en nøjagtig redegørelse for, hvad der skete, beskytte de involverede sundhedspersonale, indsamle oplysninger om ekstravasationer og fremhæve underskud i praksis.23 dokumentation og rapportering til de relevante enheder af bivirkninger og medicineringsfejl er en anden måde, hvorpå apotekere kan hjælpe med at forhindre fremtidige begivenheder. Data indsamlet fra de rapporterede bivirkninger og medicineringsfejl kunne bruges som læringsværktøjer til systemisk at undersøge, hvordan disse hændelser opstår. Lokale procedurer og protokoller er afgørende for rettidig anerkendelse og håndtering af ekstravasation og forebyggelse af alvorlig vævsskade. Der bør gøres en fælles indsats for at sikre rettidige tværfaglige forsøg på at uddanne alle medlemmer af sundhedsvæsenet, der er involveret i ledelsen af disse patienter, når begivenheden har fundet sted. Der bør gøres en ekstra indsats for at iværksætte politikker, der kan forhindre yderligere begivenheder. Hvis politikker er på plads, bør de gøres let tilgængelige og opdateres regelmæssigt for at afspejle den nuværende praksis. European Oncology Nursing Society (EONS) 2007 ekstravasation retningslinjer giver foreslåede data og skabeloner, der kan bruges til at indsamle oplysninger i tilfælde af en sag.23
tegn og symptomer på ekstravasation
tegn og symptomer på vesikant ekstravasation inkluderer hævelse, rødme og / eller ubehag, der ofte beskrives som brændende eller stikkende. Modstand under lægemiddeladministration, en langsom eller træg infusion og mangel eller tab af blodretur fra IV-kanylen, implanteret port eller anden central venøs adgangsanordning kan være indikatorer for, at der forekommer en vesikant ekstravasation.23 misfarvningen og indurationerne i huden kan udvikle sig yderligere med udviklingen af blærer eller nekrose og muligvis sårdannelse og dyb vævsskade. Det kan tage flere dage, før det fulde omfang af epitelskaden realiseres.
behandling af kemoterapi-induceret ekstravasation
behandlingsmetoder anvendt til håndtering af vesikant ekstravasation inkluderer øjeblikkelig seponering af kemoterapi og afkøling eller fortynding af stedet for ekstravasation. For at reducere sygeligheden forbundet med ekstravasation er det vigtigt, at klinikere er velinformerede om de tilgængelige behandlinger og arbejder hurtigt for at undgå yderligere patientskade. Håndtering af nonvesikant ekstravasation inkluderer typisk hævning af lemmer og afkøling og inkluderer normalt ikke anvendelse af farmakologisk terapi.23
Initial styring af Vesicant ekstravasation
let tilvejebringelse af tidlig intervention kan lettes ved at stille et ekstravasationssæt til rådighed i institutionen. De fleste ekstravasationssæt indeholder engangssprøjter og kanyler, kolde-varme pakninger, gasbindepuder, klæbende gips, sterile og beskyttelseshandsker og medicin til behandling af ekstravasation (f.eks. En liste over kittets indhold skal placeres i kittet, og regelmæssig verifikation af lægemiddelindholdet med opdaterede udløbsdatoer bør opretholdes regelmæssigt af en farmaceut.2
når vesikant ekstravasation opstår, skal klinikeren straks stoppe infusionen; kanylen eller den ikke-korende portnål skal dog holdes på plads, og der skal forsøges at aspirere vesikanten med en 10 mL sprøjte. Ekstravasationsområdet skal markeres og fotograferes; derefter skal kanylen eller nålen fjernes, og lægen skal underrettes. Patienter kan kræve brug af analgetika for at hjælpe med at håndtere den smerte, de kan opleve. Når de første foranstaltninger er truffet, er det meget vigtigt at dokumentere den bivirkning og/eller medicineringsfejl, der er opstået, grundigt.23
for vinca-alkaloider, hvor spredning eller fortynding af vesikanten er indikeret, påføres lokal varme i 20 minutter 4 gange dagligt i 1 i 2 dage. For andre vesikante ekstravasationer, herunder antracykliner, er initial behandling rettet mod lokalisering og neutralisering af det ekstravaserede middel med kolde kompresser i 20 minutter 4 gange dagligt i 1 til 2 dage, hvilket begrænser den cellulære optagelse af disse midler.23
farmakologisk behandling
DMSO: DMSO er et almindeligt opløsningsmiddel, der trænger ind i væv og forbedrer hudpermeabilitet, hvilket kan lette absorptionen af et ekstravaseret lægemiddel. Når det anvendes topisk, har det friradikale rensnings – / antioksidantegenskaber, der kan fremskynde fjernelsen af det ekstravaserede lægemiddel. DMSO (Rimso-50) er kun tilgængelig til detailkøb i USA i en 50% (vol/vol) opløsning i vand. Denne løsning er FDA godkendt kun til behandling af tilbagevendende interstitiel cystitis.24 effekten af DMSO til behandling af kemoterapi-ekstravasation blev først beskrevet i flere sagsrapporter og små kliniske studier.
i et tilfælde blev en ekstravasation på 10 mg daunorubicin hos en 42-årig mand behandlet med natriumbicarbonat, deksamethason (4 mg), ispakninger og 1,5 mL topisk DMSO 70%, som blev påført hver 3.til 4. time i 10 dage. Dette regime gav smertelindring og forebyggelse af mavesår.25
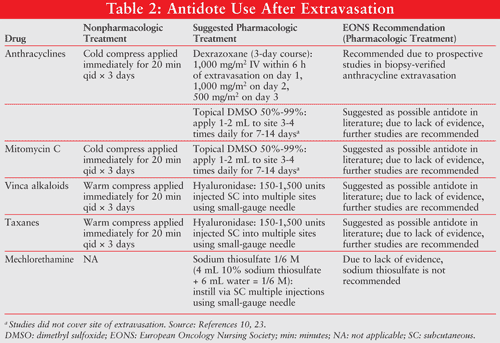
Olver rapporterede tre tilfælde af ekstravasationsopløsning med DMSO-brug.26 i et tilfælde resulterede den daglige anvendelse af DMSO 99% i 14 dage i fuldstændig opløsning af smerte inden for 2 dage uden sårdannelse hos en patient med doksorubicin ekstravasation. Patienten modtog også natriumbicarbonat 8,4% og den passende ikke-farmakologiske behandling. (Se tabel 2 for ikke-farmakologiske muligheder.) I et andet tilfælde blev en 49-årig mand, der fik 4 til 6 mg doksorubicin, behandlet for ekstravasation af doksorubicin med 5 mL 8.4% natriumbicarbonat, ispakker og DMSO 99% anvendes dagligt i 14 dage. Ulceration forekom ikke; imidlertid forekom en 3 gange 2,5 cm indurated område, der begrænser albueforlængelse.26 i et tredje tilfælde forhindrede en topisk påføring af DMSO 99% (hver 6.time i 1 uge og derefter to gange dagligt i en anden uge) ulceration; imidlertid forblev resterende pigmentering.26
Berghammer et al.rapporterede også et tilfælde af ekstravasation af docetaksel.27 ekstravasatet blev fortyndet med normal (0,9%) saltopløsning og behandlet med ispakninger. DMSO blev påført 3 gange hvert 45.minut, og orale kortikosteroider og diclofenac blev givet på dagen for ekstravasation. Alle symptomer forsvandt inden for 24 timer; forsinkede symptomer (brun misfarvning, hudhyperplasi) optrådte dog på dag 5 og steg derefter. Ingen plastisk kirurgisk indgreb var nødvendig. Selvom DMSO i kombination med hypotermi og isotonisk saltopløsning ikke var effektiv til at forhindre de forsinkede symptomer, begrænsede den betændelsen og vævsnekrose. rapporterede, at brugen af en DMSO 90% og alfa-tocopherol 10% blanding inden for 48 timer efter ekstravasationer af antracykliner eller mitomycin C hos 8 patienter resulterede i ingen hudsår eller funktionel eller neurovaskulær svækkelse.28 desværre er alfa-tocopherol ikke et let tilgængeligt lægemiddel, og yderligere randomiserede forsøg bør udføres for at validere dets anvendelse.
i en prospektiv undersøgelse af 20 patienter med antracyclin-ekstravasationer blev DMSO 99% administreret to gange, 6 gange dagligt i 2 uger.29 Der blev ikke beskrevet sår efter DMSO-behandling, skønt indledende hævelse (85%), erytem (75%) og smerter (60%) var tydelige. Efter en 3 måneders opfølgningsperiode hos 16 patienter havde 6 (38%) patienter ingen tilsyneladende symptomer, og 10 (63%) havde pigmenterede indurationer. Bertelli gennemførte også en prospektiv undersøgelse, der evaluerede virkningerne af DMSO på antracyklin-ekstravasationer.30 Doksorubicin tegnede sig for 11 tilfælde, og epirubicin tegnede sig for 46 tilfælde. Patienterne blev behandlet med DMSO 99% hver 8.time i 7 dage. Halvfjerds procent af patienterne (40/57) havde fuldstændig opløsning af ekstravasation inden for 1 uge, en patient havde resterende bløddelsinduration, og en patient havde resterende hyperpigmentering.
i disse tilfælde rapporter og små undersøgelser blev ekstravasationer diagnosticeret klinisk og ikke ved biopsi. DMSO kan være en mulighed for behandling af ekstravaserede antracykliner, mitomycin C og actinomycin D. Det anbefales, at et tyndt lag DMSO påføres det ekstravaserede område og får lov til at tørre. En ikke-okklusiv dressing skal påføres inden for 10 til 25 minutter. Disse trin skal gentages hver 8. time i 7 dage.23 selvom DMSO er blevet anvendt i praksis som en mulighed for behandling, kan mangel på potentielle forsøg begrænse brugen. Eons 2007-ekstravasationsretningslinjerne anbefaler, at der udføres yderligere undersøgelser; DMSO 50% Til 99% kan dog overvejes til brug efter klinikerens skøn.23 Det er vigtigt at bemærke, at ingen af DMSO-prospektive undersøgelser brugte en bandage for at give huden mulighed for fuldt ud at absorbere DMSO.
Hyaluronidase: Det menes, at hyaluronidase er i stand til at nedbryde den ekstracellulære matrice, der ligger til grund for epitelceller. Matricen holder fast i store mængder vandmolekyler, og ved dets nedbrydning er det i stand til at frigive væsken i det ekstracellulære miljø. I tilfælde af en ekstravasation muliggør det øget væske til stedet og fortynder således den faktiske koncentration af huden på kontaktstedet.31,32 Hyaluronidase er blevet anvendt til behandling af vinca alkaloid og taksan ekstravasationer.33 doser hyaluronidase i området fra 150 til 1.500 enheder fortyndet i 1 mL normal saltvand subkutant eller intradermalt inden for 1 time efter ekstravasation er blevet anvendt.
i en lille klinisk undersøgelse af 6 patienter med vinblastin (n = 1), vincristin (n = 1) og vinorelbin (n = 4) ekstravasation blev 250 enheder hyaluronidase injiceret i det indbyggede kateter eller subkutant (6 injektioner) i tilfælde af skade. Ingen steroider eller kolde pakninger blev anvendt. Smerter forsvandt inden for få dage efter behandling med hyaluronidase hos alle patienter. En patient klagede over mildt smertefuld induration 3 måneder efter ekstravasation af vincristin.30 disse rapporter afslører lovende oplysninger; der er dog stadig en generel mangel på beviser for brugen af hyaluronidase til behandling af vinca alkaloid ekstravasationer. Flere prospektive forsøg skal gennemføres. EONS 2007-ekstravasationsretningslinjerne anbefaler, at der udføres yderligere undersøgelser; hyaluronidase kan dog betragtes som en mulighed ved foreslåede doser efter klinikerens skøn.23
natriumthiosulfat: Natriumthiosulfat forhindrer alkylering og vævsdestruktion ved at tilvejebringe et substrat til alkylering i det subkutane væv. Natriumthiosulfat har vist sig at være effektivt i dyreforsøg og i en sagsrapport til behandling af ekstravasation af mechlorethamin (nitrogen sennep).33,34 den foreslåede dosis er 2 mL 0,17 M (en opløsning af 4 mL 10% natriumthiosulfat og 6 mL sterilt vand til injektion). På grund af manglende beviser anbefaler eons 2007-ekstravasationsretningslinjerne ikke dette som en modgift.22
: Totect blev for nylig godkendt af FDA til behandling af antracyklin-inducerede ekstravasationer. 1) Det fungerer som en jernchelator, der forhindrer dannelse af jern-antracyklinkomplekser og jernmedierede hydroksilradikaler, der forårsager oksidativ skade; og 2) det stabiliserer topoisomerase II og gør det utilgængeligt for antracyklinkemoterapi. Det er ikke længere påvirket af antracyclin og forhindrer skade på de sunde celler i væv.35
effekt blev påvist i to kliniske forsøg udført i Europa.36 begge forsøg var prospektive, åbne, enkeltarmede, multicenter kliniske forsøg udført fra juli 2001 til August 2005 med i alt 80 patienter inkluderet. Den første undersøgelse omfattede patienter fra 17 kræftsteder i Danmark, og den anden omfattede patienter fra 34 kræftsteder i Danmark, Tyskland, Italien og Holland. Antracyklin ekstravasation blev diagnosticeret og bekræftet via fluorescensmikroskopi af biopsieret væv taget inden for 6 timer. En stikprøvestørrelse på 32 vurderbare patienter var påkrævet for at vise en 70% eller større reduktion i forekomsten af kirurgi (ensidig binomial test, a = .025, kr = .20). Det primære endepunkt var hastigheden af kirurgisk resektion og nekrose. Fireoghalvtreds af de 80 patienter (undersøgelse 1: n = 18; undersøgelse 2: n = 36) var evaluerbare (n = 13 negative biopsier; n = 4 ingen biopsier udført; n = 8 protokolovertrædelser) med en gennemsnitlig alder på 56 år (interval, 34-81 år). Niogtres procent (n = 37) af de evaluerede patienter var kvinder. IV-infusion i løbet af 1 til 2 timer; 1.000 mg/m2 inden for 6 timer; 1.000 mg/m2 efter 24 timer; og 500 mg / m2 efter 48 timers ekstravasation.36
patienterne blev vurderet for effekt og sikkerhed på dag 7, 14, 21 og 28 og for effekt på dag 90, 36 den mest almindelige kræftdiagnose var brystkræft (50%) efterfulgt af lymfom (39%) og andre typer kræft (9%). Patienter oplevede ekstravasationer af doksorubicin (n = 23) eller epirubicin (n = 31). Det gennemsnitlige ekstravasationsområde var 23,6 cm2 i Studie 1 og 39 cm2 i Studie 2. Elleve patienter havde områder med ekstravasation på over 75 cm2. Der var ingen tilfælde af operation i Studie 1 og 1 (2,8%, 95% CI 0,1% -14,5%) i Studie 2. Patienten, der udviklede vævsnekrose på grund af ekstravasation, havde et meget stort område af doksorubicin-ekstravasation på 253 cm2. Symptomerne steg i dagene efter ekstravasationen, vævsnekrose begyndte at forekomme 9 dage efter patientens ekstravasation, og nekrose blev kirurgisk udskåret. I undersøgelse 1 var der 1 (5,6%) hændelse af nekrose på grund af biopsi, 6 (33.3%) hændelser med udsættelse eller annullering af planlagt kræftbehandling og 9 (50%) indlæggelser på grund af ekstravasation. I undersøgelse 2 var der 1 (2,8%) hændelse med nekrose på grund af ekstravasation, 3 (8,3%) hændelser med nekrose på grund af biopsi, 10 (27,8%) hændelser med udsættelse eller annullering af planlagt kræftbehandling på grund af ekstravasationen og 13 (36,1%) hændelser med indlæggelse på grund af ekstravasationen. Ved 3 måneders opfølgning havde 88,9% (n = 16) ingen negative følger i Studie 1 og 63,9% (n = 23) i Studie 2. Femten af de 80 patienter oplevede sensoriske forstyrrelser (n = 9), hudatrofi (n = 5), smerte (n = 10), vansiring (n = 1) og begrænsning (n = 3). De fleste af patienterne (71%) var i stand til at modtage yderligere kemoterapibehandling efter planen.
de mest almindelige bivirkninger omfattede et nedsat antal hvide blodlegemer (72, 5%), nedsat hæmoglobin (42, 5%), nedsat antal blodplader (26%), øget aspartataminotransferase (36, 8%), øget alaninaminotransferase (23, 9%), reaktion på injektionsstedet (27, 5%) og kvalme (18, 8%).36 resultater fra de kliniske forsøg viste, at det er et effektivt middel til behandling af akutte antracyklin-ekstravasationer og forebyggelse af forsinkede symptomer.
en oversigt over disse behandlingsanbefalinger, herunder eons 2007-retningslinjerne, findes i tabel 2.
farmaceutens rolle
apotekere bør være tæt involveret i vurderingen og styringen af alle kemoterapiinducerede ekstravasationer. De kan spille en integreret rolle på flere måder, herunder: 1) Udvikling af politikker og protokoller; 2) patient -, familie-og tværfaglig uddannelse; 3) dokumentation og rapportering af ekstravasationer og andre bivirkninger efter Terapi; og 4) overvågning af korrekt dosering, administration og effektivitet af behandlingen.
konklusion
alle de undersøgte undersøgelser involverede voksne, da pædiatriske patienter ville have haft en øget risiko for agitation og træk i linjerne. Til dato er det eneste ekstravasationsmiddel, der er blevet undersøgt i store, multicenter, prospektive forsøg, der brugte objektiv, pålidelig test til at diagnosticere ekstravasationssager; dette giver stærke beviser for, at det er nyttigt. På trods af deres almindelige anvendelser i praksis er andre farmakologiske behandlinger, såsom DMSO og hyaluronidase, ikke blevet undersøgt grundigt; derfor mangler anbefalinger baseret på evidens. Styring af ekstravasation bør udføres efter klinikerens skøn i samarbejde med alle medlemmer af sundhedsvæsenet.
1. Infusion Sygeplejersker Samfund. Infusion sygepleje standarder for praksis. J Infus Nurs. 2006; 29 (suppl 1): S1-S92.
2 . Polovich M, Hvid J, Kelleher L. kemoterapi og bioterapi retningslinjer og anbefalinger til praksis. 2. udgave. Pittsburgh, PA: Oncology Nursing Society; 2005.
3. Ener RA, Meglathery SB, Styler M. ekstravasation af systemiske hæmato-onkologiske terapier. Ann Oncol. 2004;15:858-862.
4. Sauerland C, Egelking C, Vægmand R, Corbi D. Vesicant ekstravasation del i: mekanismer, patogenese og sygepleje for at reducere risikoen. Oncol Nurs Forum. 2006;33:1134-1141.
5. Cassagnol M, Cohen H. Dermatologic toxicities of chemotherapeutic agents. US Pharm. 2008;33(1)(Oncology suppl):10-20.
6. Schulmeister L. Extravasation management. Semin Oncol Nurs. 2007;23:184-190.
7. Viale P. Chemotherapy and cutaneous toxicities: implications for oncology nurses. Semin Oncol Nurs. 2006;22:144-151.
8. Cox K, Stuart-Harris R, Abdini G, et al. The management of cytotoxic-drug extravasation: guide-lines drawn up by a working party for the Clinical Oncological Society of Australia. Med J Aust. 1988;148:185-189.
9. Schrijvers DL. Extravasation: en frygtet komplikation af kemoterapi. Ann Oncol. 2003; 14 (suppl 3): iii26-iii30.
10. Den Nationale Ekstravasation Information Service. www.extravasation.org.uk/home.html. adgang til 25. marts 2009.
11. Lemmers N, Gels M, Sleijfer D, et al. Komplikationer af venøse adgangsporte hos 132 patienter med dissemineret testikelkræft behandlet med polykemoterapi. J Clin Oncol. 1996;14:2916-2922.
12. Shetty PC, Mody MK, Kastan DJ. Resultat af 350 implanterede brystporte placeret af interventionelle radiologer. J Vasc Interv Radiol. 1997;8:991-995.
13. Dorr RT. Modgift mod vesikant kemoterapi ekstravasationer. Blod Rev. 1990; 4: 41-60.
14. Langer SV, Sehested M, Jensen PB. Behandling af antracyclin ekstravasation. Clin Kræft Res. 2000; 6: 3680-3686.
15. Raymond E, Faivre S, Jm, Chaney SG. Antineoplastisk aktivitet: virkningsmekanisme og antineoplastisk aktivitet. Semin Oncol. 1998; 2 (suppl 5): 4-12.
16. Rivory LP. Nye lægemidler til kolorektal cancer-virkningsmekanismer. Aust Prescr. 2002;25:108-110. www.australianprescriber.com/magazine/25/5/108/10/. adgang til 25. marts 2009.
17. Skeel RT. Håndbog for kræft kemoterapi. 5. udgave. Ny York, NY: Lippincott Vilhelms & Vilkins; 1999.
18. Boyle DM, Engelking C. Vesicant ekstravasation: myter og realiteter. Oncol Nurs Forum. 1995;22:57-67.
19. LC. Forebyggelse og styring af perifer ekstravasation. Sygepleje. 2004;34:66-67.
20. Shulmeister L, Camp-Sorrell D. kemoterapi ekstravasation fra implanterede havne. Oncol Nurs Forum. 2000;27:531-538.
21. Debets JM, vil JA, Schlangen JT. En sjælden komplikation af implanterede centralvenøse adgangsanordninger: kateterfraktur og embolisering. Støtte Pleje Kræft. 1995;3:432-434.
22. Gorski LA. Central venøs adgangsanordning okklusioner. Del 2: ikke-trombotiske årsager og behandling. Hjem Healthc Sygeplejerske. 2003;21:168-171.
23. Retningslinjer for ekstravasation 2007. European Oncology Nursing Society. www.cancerworld.org/CancerWorld/getStaticModFile.aspx?id=2340. adgang til 25. marts 2009.
24. Rimso-50 indlægsseddel. Lake Forest, IL: Bioniche Pharma USA LLC; 2009.
25. – Godnat. Dimethylsulfoksid-begrænsende vævsskade forårsaget af ekstravasation af doksorubicinmidler. Ann Praktikant Med. 1983;98:1025.
26. Olver ind, Mor. Use of dimethyl sulfoxide in limiting tissue damage caused by extravasation of doxorubicin . Cancer Treat Rep. 1983;67:407-408.
27. Berghammer P, Pohnl R, Baur M, Dittrich C. Docetaxel extravasation. Support Care Cancer. 2001;9:131-134.
28. Ludwig CU, Stoll HR, Obrist R, Obrecht JP. Prevention of cytotoxic drug-induced skin ulcers with dimethyl sulfoxide (DMSO) and alpha-tocopherole. Eur J Cancer Clin Oncol. 1987;23:327-329.
29. Olver IN, Aisner J, Hament A, et al. A prospective study of topical dimethyl sulfoxide for treating anthracycline extravasation. J Clin Oncol.1988;6:1732-1735.
30. Bertelli G. Prevention and management of extravasation of cytotoxic drugs. Drug Saf. 1995;12:245-255.
31. Balazs EA, Laurent TC, Jeanloz RW. Nomenclature of hyaluronic acid. Biochem J. 1986;235:903.
32. Girish KS, Kemparaju K. The magic glue hyaluronan and its eraser hyaluronidase. Life Sci. 2007;80:1921-1943.
33. Dorr T. Antidotes to vesicant chemotherapy extravasations. Blood Rev. 1990;4:41-60.
34. Owen OE, Dellatorre DL, Van Scott EJ, Cohen MR. Accidental intramuscular injection of mechlorethamine. Cancer. 1980;45:2225-2226.
35. Totect (dexrazoxane for injection) package insert. Copenhagen, Denmark: TopoTarget A/S; October 2007.
36. Mouridsen HT, Langer SW, Buter J, et al. Treatment of anthracycline extravasation with Savene (dexrazoxane). Results from two prospective clinical multicenter studies. Ann Oncol. 2007;18:546-550.
Leave a Reply