enantiomerer og diastereomerer
enantiomerer og diastereomerer er de eneste to stereokemiske forhold, som du kan have mellem to molekyler. Stereoisomerer er to molekyler, der opfylder følgende to krav:
- begge molekyler skal have den samme molekylformel, og
- begge molekyler skal have den samme atomforbindelse.
så hvad er forskellen da? Molekylerne er stereoisomerer, hvis de har en anden 3d-form, og de kan ikke overlejres i rummet.
hvad betyder ikke-overlejret?
ikke-overlejrede molekyler kan ikke få dem til at se nøjagtigt ens ud, uanset hvor mange rotationsoperationer du gør med dem. “Rotationerne” inkluderer også den frie rotation omkring de enkelte obligationer.
tænk på dine hænder. Hvis du justerer dem sammen, så alle fingre står op, vil palmerne se i modsatte retninger. Hvis du får dine palmer til at se i samme retning, vil dine tommelfingre se i anden retning osv. Uanset hvor meget du roterer dine hænder, vil du aldrig være i stand til at få dem til at se nøjagtigt ens ud—dine hænder er ikke-overlejrede spejlbilleder. Samme princip gælder for molekyler.
hvorfor har vi brug for to forhold? Hvorfor skal vi have enantiomerer og diastereomerer og kan ikke bare gøre med en—stereoisomerer? Der er faktisk en anden type forhold, som to molekyler kan have. Lad os grave lidt dybere.
Hvad er enantiomerer?
enantiomerer er to molekyler, der ikke er overlejrede spejlbilleder. Ligesom dine hænder kan molekyler have et spejlbillede, der ikke kan overlejres med det originale molekyle. Se på disse to molekyler:
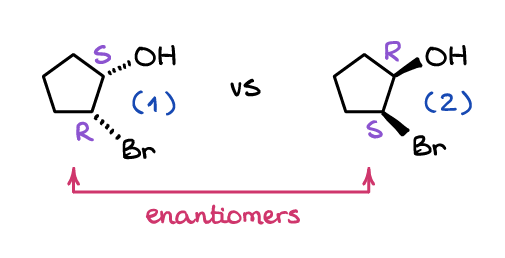
uanset hvor meget du roterer en i rummet, vil du aldrig være i stand til at få det til at se det samme ud som det andet. Mens molekyle (1) og molekyle (2) har begge grupper (OH og Br) cis til hinanden, ser de i forskellige retninger fra cyklusplanet.
Bemærk, Der er mange måder, hvordan du kan lave et spejlbillede til et molekyle. Her er de tre mulige eksempler:
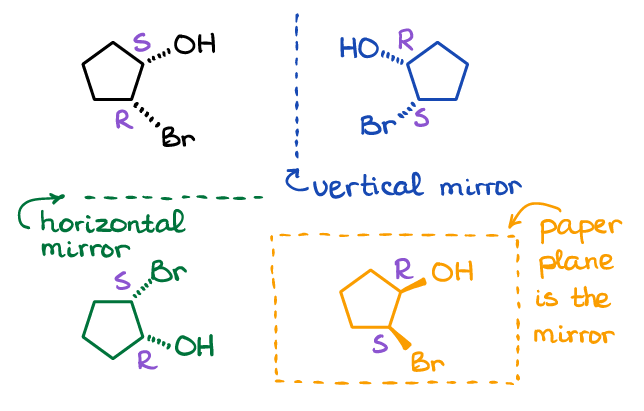
spejlplanet kan være lodret, vandret eller endda papiret, hvor du tegner molekylet, kan være selve spejlplanet. Jeg foreslår, at du laver et par af molekylerne fra billedet ovenfor ved hjælp af dit molekylære model kit (vælg en refleksion), og sørg for, at de ikke er overlejrede ved fysisk at rotere dem i rummet.
en anden vigtig skelnen mellem enantiomererne er, at alle stereocentre også spejles mellem molekylerne. Betydning, Alle s stereocentre er R ‘er i det andet molekyle, og alle R’ er i det ene molekyle er S ‘ er i det andet. For eksempel er molekylet (1) ovenfra (1s, 2R)-2-bromocyclopentanol, mens dets enantiomer, molekyle (2), er (1R, 2s)-2-bromocyclopentanol.
Hvad er diastereomerer?
når det kommer til diastereomerer, er det vel ikke enantiomerer. Jeg mener, seriøst, den “almindelige” definition af en diastereomerer er stereoisomerer, der ikke er enantiomerer. Den officielle definition er dog, at diastereomerer er ikke-overlejrede molekyler, der ikke er spejlbilleder af hinanden. Lad os for eksempel se på følgende to molekyler:
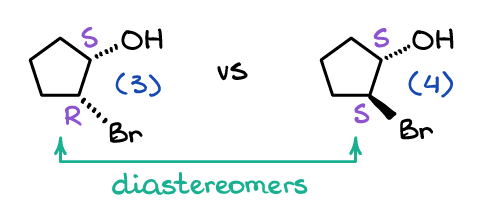
molekyler (3) og (4) er naturligvis ikke spejlbilleder, så de kan ikke være enantiomerer. De er heller ikke overlejrede i rummet, uanset hvor meget du roterer dem i rummet, så de er heller ikke det samme molekyle. Definition diastereomerer, da de ikke er overlejrede, ikke spejlbilleder af hinanden.
Bemærk, at i modsætning til enantiomerer har diastereomerer kun nogle af stereocentrene ændret sig fra det ene molekyle til det andet. For eksempel er molekyle (3) (1s, 2R)-2-bromocyclopentanol, mens dets diastereomer er (1s, 2s)-2-bromocyclopentanol.
skal du have chirale carbonatomer for at have enantiomerer og diastereomerer?
Nej, det gør du ikke! Bemærk, hvordan definitionen af enantiomerer siger, at molekylerne er ikke-overlejrede spejlbilleder, mens diastereomerer er ikke-overlejrede ikke-spejlbilleder? Definitionerne siger intet om de chirale centre eller atomer. Således fungerer ethvert par molekyler, der passer til definitionen! For eksempel er allener kumulerede alkener, der ikke er plane:
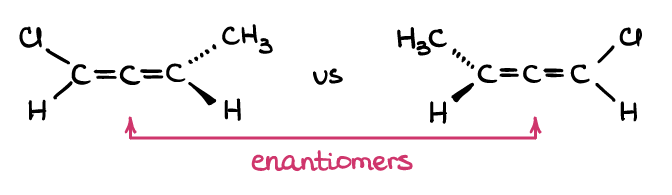
Hvis du bygger et par allener med dit molekylære model kit (Ja, få dit molekylære model kit og faktisk bygge dem!), vil du se, at de ikke kan overlejres i rummet. Men disse to molekyler har ingen chirale carbonatomer… og alligevel passer de til definitionen af enantiomerer, derfor er de et par enantiomerer! Så som du kan se, er de chirale atomer i sig selv ikke det vigtige her, det er snarere 3D-strukturen i selve molekylet.
Du kan også have diastereomerer i molekyler, der ikke har nogen chirale atomer. Se på følgende eksempler:
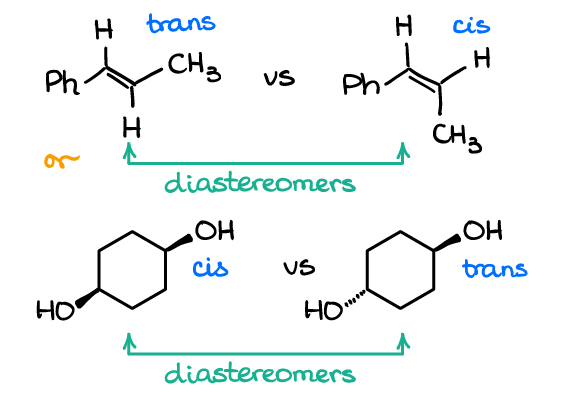
det øverste par er et eksempel på cis/trans (eller E/å, hvis du vil bruge de strenge uipac-navne) isomerer i alkener. Det andet par repræsenterer også som cis / trans par af isomerer. Ingen af molekylerne har dog chirale atomer. Og da hvert par repræsenterer et par ikke-overlejrede molekyler, der ikke er spejlbilleder, er de diastereomerer.
Dette er typiske eksempler på test, og mange instruktører elsker at kaste disse spørgsmål på dig. Mange studerende har en tendens til at have en slags tunnelsyn, når det kommer til stereokemiske forhold, der kun fokuserer på molekyler med chirale atomer. Dette er en defekt heuristisk! Så sørg for altid at analysere hele molekylet og bruge definitionen af forholdet, snarere end kun at fokusere på de chirale atomer.
Leave a Reply