3.4: Rutherfords eksperiment – atomets nukleare Model
atomer og guld
i 1911 indledte Rutherford og kolleger Hans Geiger og Ernest Marsden en række banebrydende eksperimenter, der fuldstændigt ville ændre den accepterede model af atomet. De bombarderede meget tynde plader af guldfolie med hurtigt bevægende alfapartikler.


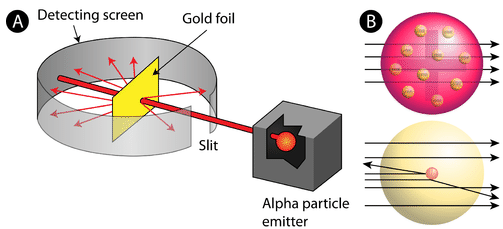
figur \(\Sideindeks{2}\) (A) den eksperimentelle opsætning til Rutherfords guldfolieeksperiment: et radioaktivt element, der udsendte alfapartikler, blev rettet mod et tyndt ark guldfolie, der var omgivet af en skærm, der muliggør påvisning af de afbøjede partikler. (B) ifølge blommepudding-modellen (øverst) skulle alle alfapartiklerne have passeret gennem guldfolien med ringe eller ingen afbøjning. Rutherford fandt ud af, at en lille procentdel af alfapartikler blev afbøjet i store vinkler, hvilket kunne forklares af et atom med en meget lille, tæt, positivt ladet kerne i midten (bunden).
ifølge den accepterede atommodel, hvor et atoms masse og ladning er ensartet fordelt over hele atomet, forventede forskerne, at alle alfapartiklerne ville passere gennem guldfolien med kun en lille afbøjning eller slet ingen. Overraskende, som vist i figur \(\Sideindeks{2}\) (mens de fleste af alfapartiklerne faktisk var ubesvarede, sprang en meget lille procentdel (ca.1 ud af 8000 partikler) af guldfolien i meget store vinkler. Nogle blev endda omdirigeret tilbage mod kilden. Ingen forudgående viden havde forberedt dem til denne opdagelse. I et berømt citat udbrød Rutherford, at det var “som om du havde fyret en 15-tommers skal på et stykke væv, og det kom tilbage og ramte dig.”
Rutherford var nødt til at komme med en helt ny model af atomet for at forklare hans resultater. Fordi langt størstedelen af alfapartiklerne var passeret gennem guldet, begrundede han, at det meste af atomet var tomt rum. I modsætning hertil må partiklerne, der blev stærkt afbøjet, have oplevet en enorm kraftig kraft i atomet. Han konkluderede, at al den positive ladning og størstedelen af atomets masse skal koncentreres i et meget lille rum i atomets indre, som han kaldte kernen. Kernen er den lille, tætte, centrale kerne af atomet og består af protoner og neutroner.Rutherfords atommodel blev kendt som atommodellen. I atomet er protonerne og neutronerne, som omfatter næsten hele atomets masse, placeret i kernen i atomets centrum. Elektronerne er fordelt rundt om kernen og optager det meste af atomets volumen. Det er værd at understrege, hvor lille kernen er sammenlignet med resten af atomet. Hvis vi kunne sprænge et atom på størrelse med et stort professionelt fodboldstadion, ville kernen være på størrelse med en marmor.Rutherfords model viste sig at være et vigtigt skridt i retning af en fuld forståelse af atomet. Det adresserede imidlertid ikke fuldstændigt elektronernes natur og den måde, hvorpå de besatte det store rum omkring kernen. For denne og andre indsigter blev Rutherford tildelt Nobelprisen i kemi i 1908. Desværre ville Rutherford have foretrukket at modtage Nobelprisen i fysik, fordi han betragtede fysik bedre end kemi. Efter hans mening er “al videnskab enten fysik eller frimærkeindsamling.”
Leave a Reply