2.4 B: dehydrering syntese
dehydrering syntese
de fleste makromolekyler er lavet af enkelt underenheder eller byggesten, kaldet monomerer. Monomerer kombineres med hinanden via kovalente bindinger til dannelse af større molekyler kendt som polymerer. Dermed frigiver monomerer vandmolekyler som biprodukter. Denne type reaktion er kendt som dehydreringssyntese, hvilket betyder “at sammensætte, mens du mister vand. “Det anses også for at være en kondensationsreaktion, da to molekyler kondenseres til et større molekyle med tabet af et mindre molekyle (vandet.i en dehydreringssyntesereaktion mellem to ikke-ioniserede monomerer, såsom monosaccharidsukker, kombineres brintet af en monomer med hydroksyl-gruppen af en anden monomer og frigiver et vandmolekyle i processen. Det er en af de mest almindelige typer af hydrogen, der bruges til at danne en kovalent binding. Således bliver de monomerer, der er sammenføjet, dehydreret for at muliggøre syntese af et større molekyle.
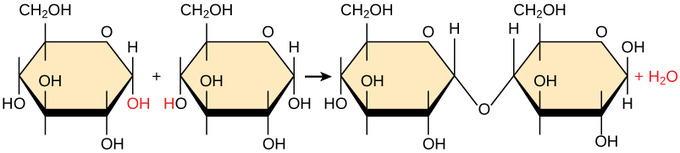
når monomererne ioniseres, som det er tilfældet med aminosyrer i et vandigt miljø som cytoplasma, kombineres to hydrogener fra den positivt ladede ende af en monomer med et ilt fra den negativt ladede ende af en anden monomer, der igen danner vand, som frigives som et sideprodukt og igen forbinder de to monomerer med en kovalent binding.

som yderligere monomerer forbinder via flere dehydreringssyntesereaktioner, begynder kæden af gentagne monomerer at danne en polymer. Forskellige typer monomerer kan kombineres i mange konfigurationer, hvilket giver anledning til en forskelligartet gruppe af makromolekyler. Tre af de fire store klasser af biologiske makromolekyler (komplekse kulhydrater, nukleinsyrer og proteiner) er sammensat af monomerer, der går sammen via dehydreringssyntesereaktioner. Komplekse kulhydrater dannes ud fra monosaccharider, nukleinsyrer dannes ud fra mononukleotider, og proteiner dannes ud fra aminosyrer.
der er stor mangfoldighed i den måde, hvorpå monomerer kan kombineres til dannelse af polymerer. For eksempel er glucosemonomerer bestanddelene af stivelse, glykogen og cellulose. Disse tre er polysaccharider, klassificeret som kulhydrater, der er dannet som et resultat af flere dehydreringssyntesereaktioner mellem glukosemonomerer. Imidlertid resulterer den måde, hvorpå glukosemonomerer samles, specifikt placeringer af de kovalente bindinger mellem forbundne monomerer og orienteringen (stereokemi) af de kovalente bindinger, i disse tre forskellige polysaccharider med forskellige egenskaber og funktioner. I nukleinsyrer og proteiner varierer placeringen og stereokemien af de kovalente forbindelser, der forbinder monomererne, ikke fra molekyle til molekyle, men i stedet de flere slags monomerer (fem forskellige monomerer i nukleinsyrer, A, G, C, T og U mononukleotider; 21 forskellige aminosyrer monomerer i proteiner) kombineres i en lang række sekvenser. Hvert protein eller nukleinsyre med en anden sekvens er et andet molekyle med forskellige egenskaber.
Leave a Reply