Peptidbinding
Signifikant delokalisering av det ensomme par elektroner på nitrogenatomet gir gruppen en delvis dobbeltbinding karakter. Den delvise dobbeltbindingen gjør amidgruppen plan, som forekommer i enten cis-eller transisomerer. I den utfoldede tilstanden av proteiner er peptidgruppene fri til å isomerisere og vedta begge isomerer; i foldet tilstand blir imidlertid bare en enkelt isomer vedtatt i hver posisjon (med sjeldne unntak). Transformen foretrekkes overveldende i de fleste peptidbindinger (omtrent 1000:1-forhold i trans: cis-populasjoner). Imidlertid har X-pro peptidgrupper en tendens til å ha et omtrent 30:1-forhold, antagelig fordi symmetrien mellom c α {\displaystyle \mathrm {C^{\alpha }} }

og C δ {\displaystyle \mathrm {C^{\delta }} }

atomer av prolin gjør cis og trans isomerer nesten like i energi (se figur nedenfor).
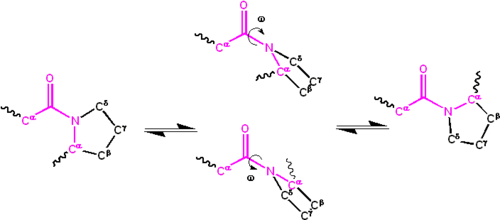


; ω = 0 ∘ {\displaystyle \omega =0^{\circ }}

for cis-isomeren (synperiplanar konformasjon) og ω = 180 ∘ {\displaystyle \omega =180^{\circ}}

for transisomeren (antiperiplanar konformasjon). Amidgrupper kan isomerisere Om C ‘ – n-bindingen mellom cis – og transformene, om enn sakte ( τ ∼ {\displaystyle \ tau \sim}

20 sekunder ved romtemperatur). Overgangen sier ω = ± 90 ∘ {\displaystyle \ omega = \ pm 90^{\circ }}

krever at den delvise dobbeltbindingen brytes, slik at aktiveringsenergien er omtrent 80 kilojoule/mol (20 kcal / mol). Aktiveringsenergien kan imidlertid senkes (og isomeriseringen katalyseres) ved endringer som favoriserer den enkeltbundne formen, for eksempel å plassere peptidgruppen i et hydrofobt miljø eller donere en hydrogenbinding til nitrogenatomet i En x-Pro-peptidgruppe. Begge disse mekanismene for å senke aktiveringsenergien er observert i peptidylprolyl-isomeraser (Ppiaser), som er naturlig forekommende enzymer som katalyserer cis-transisomeriseringen Av x-Pro-peptidbindinger. conformational protein folding er vanligvis mye raskere (vanligvis 10-100 ms) enn cis-trans isomerisering (10-100 s). En nonnativ isomer av noen peptidgrupper kan forstyrre den konformative foldingen betydelig, enten bremse den eller forhindre at den selv forekommer til den innfødte isomeren er nådd. Imidlertid har ikke alle peptidgrupper samme effekt på folding; nonnative isomerer av andre peptidgrupper kan ikke påvirke folding i det hele tatt.
Leave a Reply