CIMAvax-EGF: en ny terapeutisk vaksine mot avansert lungekreft
RAPPORT
CIMAvax-EGF: en ny terapeutisk vaksine mot avansert lungekreft
Gisela Gonzá 1, Agustin Lage1, Tania Crombet1, Gryssel Rodríguez1, Beatriz Garcauka1, Ariadna Cuevas1, Lisel Viñ 1, Norkis Arteaga1, Elia neninger2
1senter for molekylær immunologi, cimave. 216 hjørne 15, Atabey, Playa, POBox 16 040, Havana, Cuba
2Hermanos Ameijeiras HospitalSan L@zaro # 701 E / Belascoí Gonz@lez, Centro Habana, Havana City, Cuba.
ABSTRACT
resultatene som tillater Cubanske Regulatory Agency (CECMED) å gi Sanitær Registrering Til CIMAvax-EGF kreftvaksine for avansert ikke-småcellet lungekreft (NSCLC) er vist. Dette var Den første registreringen av en terapeutisk vaksine i Cuba og også den første registreringen av en lungekreft vaksine i verden. Derfor tilbys en unik terapeutisk vaksine til lungekreftpasienter, noe som vil øke overlevelse og livskvalitet. Til dette formål skulle betydelige prekliniske, kliniske, regulatoriske, produktive og forhandlingsutfordringer bli møtt. Resultatene som ble oppnådd i disse feltene førte til 18 vitenskapelige artikler publisert i high impact tidsskrifter og 4 oppfinnelsesobjekter, og genererte flere patenter I Cuba og andre land. I preklinisk setting ble immunogenisitet, sikkerhet og antitumorale effekter vist hos forskjellige dyrearter. Den kliniske erfaringen begynte i 1995. Hittil har fem fase I-II kliniske studier konkludert På Cuba, to fase II har også konkludert, en I Cuba og en annen I Canada og STORBRITANNIA, og en fase II-III studie med en optimalisert tidsplan, samt en fase III studie pågår for Tiden på Cuba. I det regulatoriske feltet ble en fast-track registreringsstrategi designet og utført. Det kreves nye regulatoriske oppfatninger for å utvikle dette unike produktet. En skalerbar, reproduserbar og kontrollert produktiv prosess ble utført, sammen med et kvalitetssystem som sikret full gmp-overholdelse. Midler til produktutvikling kom fra implementering av en ny forhandlingsstrategi: forhandling av immaterielle eiendeler.
Nøkkelord: Kreftvaksine, NSCLC, Fast-Track Registrering, CIMAvax-EGF, Fase II-III Klinisk Studie
INNLEDNING
forholdet mellom systemet dannet Av Epidermal Vekstfaktorreseptoren (EGFR) og dets ligander med kreftutvikling er velkjent. I epidermoid opprinnelsestumorer er DET ET overuttrykk AV EGFR som relaterer seg til dårlige prognoser og tidlige tilbakefall etter operasjon. Det er derfor dette systemet har blitt et viktig mål for anti-tumor terapi.
celleproliferasjonsmekanismer initieres med bindingen AV EGF TIL EGFR. Vår terapeutiske tilnærming består av en vaksine MED EN EGF-formulering som gjør den immunogen og induserer en humoral immunrespons. Produksjonen av spesifikke ANTI-EGF-antistoffer som binder seg til den autologe EGF, forhindrer det i å binde SEG TIL EGFR og derved utløse celleproliferasjonsmekanismer avledet fra denne interaksjonen (1-4).
her rapporterer vi resultatene av registreringen i Cuba av denne vaksinen (CIMAvax-EGF). Dette var en del av en global strategi bestående av nye kliniske, regulatoriske, teknologiske og forretningsmessige bidrag, og støttes av 18 internasjonale vitenskapelige artikler og immaterielle rettigheter over hele verden. Vi beskriver også innovasjoner på ulike felt som gjorde det mulig å registrere CIMAVAX-EGF i Cuba og Peru.
Resultater og DISKUSJON
Vaksinasjon med EGF er trygg, immunogen Og øker overlevelsen med god livskvalitet hos pasienter i fremskredne stadier lungekreft
den kliniske erfaringen Med CIMAvax-EGF i behandlingen av ikke-småcellet lungekreft (NSCLC) på fremskredne stadier begynte i 1995. Hittil har fem fase I-II kliniske studier blitt avsluttet I Cuba; 2 randomiserte fase II kliniske studier ble avsluttet, en I Cuba og en annen I Canada og STORBRITANNIA, og det er en fase III-studie pågår i Cuba. Mer enn 800 avanserte kreftpasienter har blitt behandlet Med CIMAVAX–EGF, og viser dermed at Det er trygt, immunogent og i stand til å øke overlevelse med god livskvalitet. hovedmålet med fase I-II-studiene var å bestemme den beste vaksineformuleringen( bærerprotein og adjuvans), dosen og det terapeutiske skjemaet. Disse resultatene viste fordelene Med p64k-proteinet som bærerprotein og Montanide ISA51 som adjuvans. Den økte immunogenisiteten ved oppskalering av dosen ble også vist (5-7). analysen av samlede data fra alle fase I-II-studiene viste en signifikant økning i overlevelse hos pasienter med bedre antistoffrespons eller gode antistoffresponser( GAR), og hos pasienter med mer uttalt reduksjon I sera EGF-konsentrasjoner () som følge av vaksinasjon. Det ble også vist en signifikant økning i overlevelse hos alle vaksinerte pasienter sammenlignet med samtidig historisk kontroll (7). En fase II klinisk studie ble utført på 80 pasienter, som ble randomisert til Å få CIMAvax-EGF og best supportive care (bsc) (40 pasienter) eller BSC alene (40 pasienter), etter avsluttet førstelinjekemoterapi. De tidligere funnene ble bekreftet i denne studien. Omtrent 50% av de vaksinerte pasientene var GAR og overlevde betydelig mer enn pasienter som ikke nådde GAR-klassifiseringen(som ble klassifisert som dårlige antistoffresponere, PAR). Tilsvarende overlevde pasienter med størst reduksjon i betydelig mer enn pasienter som ikke viste denne reduksjonen (Tabell 1). En signifikant invers korrelasjon ble observert mellom ANTI-EGF antistofftitere og, som forekom hos vaksinerte pasienter, men ikke i kontrollene, og viste dermed at det var forårsaket av vaksinasjon (Figur 1).
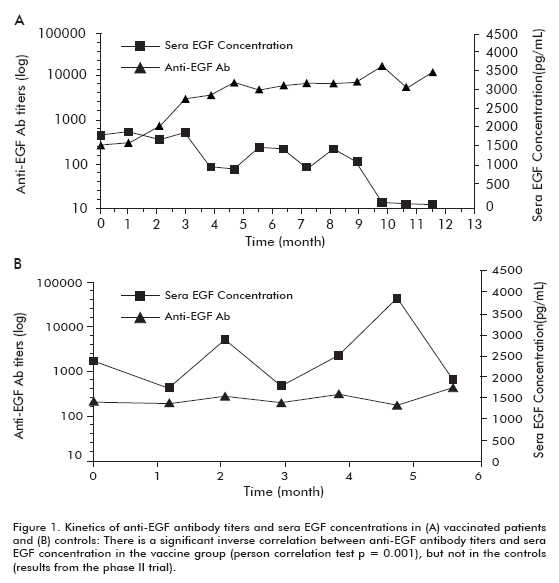
Det var en økt trend i overlevelse hos alle vaksinerte pasienter (18,53 ± 11,47; gjennomsnittlig ± median), sammenlignet med de ikke-vaksinerte kontrollene (7,55 ± 5.33), som var signifikant i gruppen pasienter som var 60 år eller yngre (Log rank test; p < 0,05) (Figur 2) (8).
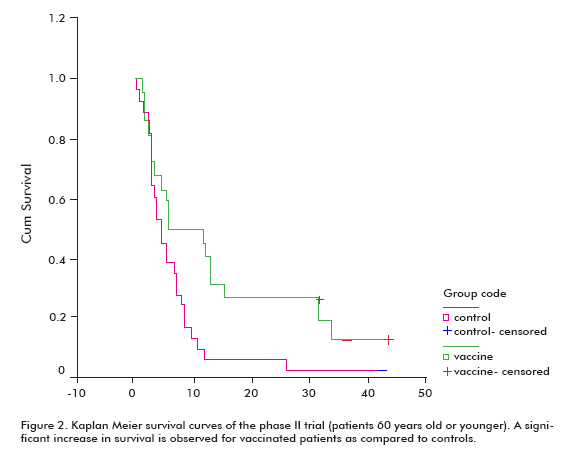
som vist i en in vitro konkurranseanalyse hemmet sera fra vaksinerte pasienter bindingen AV EGF til EGFR. Denne bindingshemming var proporsjonal med antistofftiter og overlevelse. I tillegg hemmet sera fra vaksinerte pasienter egfr-fosforylering i forhold til DETS ANTI-EGF-antistofftitere.
preferansegjenkjenningen AV egf / EGFR-bindingsstedet (loop B AV EGF-molekylet) ble studert. Pasienter hvis sera fortrinnsvis gjenkjenner loop B overlevde betydelig mer enn pasienter som ikke gjenkjente denne epitopen (9).
en dose / tidsplan optimalisering studie ble nylig avsluttet I Cuba (fase i-II). I sin utforming ble alle elementer som økte immunogeniteten i tidligere studier vurdert, som inkluderte: Montanide ISA51 som adjuvans, økte doser, fire injeksjonssteder og administrasjon av to vaksinedoser før førstelinje kjemoterapi, etterfulgt av vaksinasjon. Resultater fra denne studien viste en signifikant økning i immunogenisitet, med en 95% AV GAR nå ti ganger de tidligere maksimale antistofftitere. Alle vaksinerte pasienter overlevde betydelig mer enn kontroller fra fase II-studien (10).
en økt kapasitet av sera av pasienter til å hemme EGF/EGFR binding OG EGFR fosforylering ble også funnet. På måned syv, etter avsluttet kjemoterapi, antistoffresponsen forskjøvet mot loop B AV EGF molekylet, noe som kan indikere en forbedring i kvaliteten på immunresponsen. Resultater fra denne studien viste at det er en forbedringsmargin i responsen På CIMAvax-EGF som kan nås ved å manipulere dosen og terapeutisk tidsplan (10).
resultatene av disse forsøkene blir validert i en fase III-studie som pågår i Cuba.
Design Og implementering av en reguleringsstrategi for vaksineregistrering for å gjøre den tilgjengelig for alle avanserte ikke-småcellet lungekreft pasienter
CIMAvax-EGF Er en terapeutisk vaksine for lungekreft som er unik i verden. En global strategi ble designet og implementert; den ble styrt av regulatoriske krav, for rask registrering i Cuba. Et nært forhold mellom sponsoren (CIM) og DET Cubanske Reguleringsbyrået (CECMED) hadde til hensikt å etablere kravene til å skaffe et produkt og dets raske anvendelse til fordel for avanserte kreftpasienter uten noe annet terapeutisk alternativ. Denne strategien inkluderte utformingen av et kvalitetssystem, kvalitetskontroller og spesifikasjoner, SAMT gmp-krav for å dekke de ulike trinnene i produktutvikling. Denne globale strategien kan brukes i utviklingen av andre lignende produkter. Den akkumulerte regulatoriske erfaringen og dokumentasjonen førte til godkjenning av kliniske studier i forskjellige land. Dossieret som inneholder all informasjon gjorde Det mulig å registrere CIMAvax-EGF i Cuba og Peru. Vi kan derfor si at vi har en definert strategi for narkotikaregistrering i ulike land.
GMP-produksjonsprosessen som genererer et produkt som er skalerbart, konsistent og i samsvar med spesifikasjonene
den første utfordringen med å designe en produksjonsprosess for CIMAvax-EGF var å ha et immunogent EGF-preparat. Det ble oppnådd ved kjemisk konjugering av det humane rekombinante EGF til det rekombinante membranproteinet, P64k (Fra Neisseria meningitidis). Konjugatet injiseres sammen med en passende adjuvans (For Tiden, Montanide ISA 51 Fra Seppic, Frankrike).
en prosess på laboratorieskala ble opprinnelig utformet. En oppskalerbar (og skalerbar) sanitær og reproduserbar prosess ble senere designet og implementert, i samsvar MED gmp retningslinjer. In vitro og in vivo analytiske analyser ble også designet og implementert for å evaluere kvaliteten på råvarene, og mellomprodukter og sluttprodukter.
alle endringer ble vurdert og støttet av Gjeldende Reguleringsstrategi. Resultater fra ekvivalensstudien, for å sammenligne begge produktene, mottok GODKJENNING FRA CECMED av scaled process application, og godkjenning av produktet oppnådd i denne prosessen for klinisk bruk. Oppskalering og optimalisering av produksjonsprosessen ga vei til en publikasjon (11) og et nytt oppfinnelsesobjekt, med patenter som senere ble presentert i forskjellige land.
Forhandling av immaterielle eiendeler gitt oss midler til prosjektutvikling og også erfaring i vårt felles arbeid med myndigheter fra ulike land
Dette Prosjektet ble forhandlet med utenlandske kolleger på grunnlag av romanen begrepet «forhandling av immaterielle eiendeler», støttes hovedsakelig gjennom åndsverk av vårt produkt som var under utvikling. Denne forhandlingsstrategien besto av lisensiering av prosjektet for felles utvikling med andre land, noe som betyr at utenlandske kolleger dekket utgiftene til regulatoriske tiltak og kliniske studier på deres territorier. Som et resultat av disse forhandlingene Mottok Cuba betalinger for milepæler. Denne modaliteten for forhandling tillot oss også å ha en konstant utveksling med spesialister her og i utlandet, og dermed øke vår erfaring. Våre positive resultater med denne forhandlingsmodaliteten kan brukes på andre produkter som pågår i vårt land.
RELEVANS AV STUDIEN
CIMAvax-EGF er den første terapeutiske vaksinen for kreftbehandling registrert på Cuba, og den første registrerte i verden for lungekreft terapi. Lungekreft er et uløst helseproblem med mer enn 1,3 millioner tilfeller diagnostisert hvert år og samme antall dødsfall over hele verden. På Cuba er Det den viktigste dødsårsaken på grunn av kreft hos begge kjønn med en forekomst på mer enn 4000 avdøde per år. Terapi av valget for pasienter diagnostisert på avanserte stadier er at av første linje kjemoterapi, som kan gis samtidig med strålebehandling. Dette er en palliativ, ikke-kurativ behandling, med fullstendig respons på kjemoterapi som svært sjelden, og objektiv respons (fullstendig eller delvis) forekommer hos bare 25% av pasientene.
CIMAvax-EGF tilbyr en alternativ behandling for disse pasientene som allerede har fått førstelinje kjemoterapi. De alvorlige bivirkningene av kjemoterapi og / eller strålebehandling er velkjente, og forverrer livskvaliteten alvorlig. I stedet genererer vaksinasjon Med CIMAVAX-EGF bare milde eller moderate, snarere enn alvorlige, bivirkninger som kan løses med konvensjonell støttebehandling, samtidig som overlevelsen av avanserte lungekreftpasienter forbedres og gir god livskvalitet.
Inntil nå har mer enn 800 Cubanere blitt behandlet Med CIMAvax-EGF på mer enn 20 sykehus over hele landet. Registreringen Av CIMAVAX-EGF gjør at den kan utvides til alle pasientene i landet som ble diagnostisert med avansert lungekreft; Dermed Blir Cuba det første landet i verden med et nasjonalt program som bruker dette terapeutiske alternativet.
når det gjelder økonomiske fordeler, gjennom forhandlinger om Dette Prosjektet har vi fått 6.346 millioner USD. Forhandlingsstrategien for prosjektet er for felles utvikling med andre land, noe som betyr at den utenlandske motparten dekker utgiftene til de kliniske forsøkene i sitt eget land, noe som gjør det rimelig. Disse forsøkene krever investeringer på millioner AV USD, og dette er bare mulig hvis det støttes av utenlandske kolleger. Samtidig gir denne strategien flere kliniske data til Cuba, uten utgifter til å utføre forsøkene her. Hittil har kliniske studier blitt utført I Canada, STORBRITANNIA og Malaysia. I nær fremtid vil kliniske studier begynne I Kina og Europa. som en del av denne lisensstrategien har også utenlandske motparter ansvaret for produktregistrering i regionene der de har kommersielle rettigheter. Under registrerings-og markedsføringsprosessene vil Cuba motta betalinger for milepæler og senere, som salgs royalties.
verdensmarkedet for kreftvaksiner anses å være i størrelsesorden milliarder USD. Det Faktum At Cuba har et unikt produkt for avansert lungekreftbehandling, kan gi oss et eksportpotensial som kan finansiere bruken av dette produktet i Vårt Nasjonale Helsevesen. Vaksinasjon Med CIMAvax-EGF er trygg, immunogen og fører til økt overlevelse med god livskvalitet hos pasienter med lungesvulster i avanserte stadier. Utformingen og implementeringen av en reguleringsstrategi for registrering av denne vaksinen gjorde den tilgjengelig
for alle tilfeller av avanserte ikke-småcellet lungekreftpasienter i Cuba. Denne positive erfaringen kan gjelde for andre lignende produkter som pågår. En produksjonsprosess ble utviklet, som var skalerbar, konsistent og reproduserbar og overholdt gmp-retningslinjene, for å generere et produkt som overholder spesifikasjonene. Erfaringen med forhandling av immaterielle eiendeler har vært svært positiv, og har gitt oss midler til prosjektutvikling, samtidig som den støtter læringsopplevelsen fra felles arbeid med reguleringsmyndighetene i ulike land.
BEKREFTELSER
forfatterne vil takke følgende spesialister fra Senter For Molekylær Immunologi for deres hyllest til dette arbeidet: Rolando Pé, Loany Calvo, Suhamy Oppmerksomhet, Belinda S ④nchez, Irene Beausoleil, Ernesto Chico, Airama Alvisa, Ileana Cartroman, Sergio Smaker, Ana Veloso, Reinaldo Crow, Yanelda Lopez, Yosniel Hern@ndez, Antonio Vallin, Alejandro Portillo, Liuva Tre, Guido Ferrer, Diana Borges, Niuvis Pé, Tamara Garcupuna, Idaine Basin, Mayra Santaelena, joaquin Solozabal, Aida Rodriguez, Maria Elena Garcia, Addis Torres, Eric Chong, Carmen Roll, Mauritius Catala, Soraida Acosta, Barbara Wilkinson, Olga Torres, Normando Iznaga Alle Av Dem Fra Sentrum Av Molekylær Immunologi, Og Også Til Daniel Gonz@lez, lourdes B Costa, Galina M Moya, Rolando Pá, Gerardo Guilluxe, Vivian Pujol , Dinorah Torres fra Senter for Genteknologi og Bioteknologi.
1. Gonz@lez G, Montero E, Leó K, Cohen IR, Lage A. Autoimmunisering Til Epidermal Vekstfaktor, en komponent av den immunologiske homunculus. Autoimmun Rev 2002; 1: 89-95.
2. Lage A, Crombet T, González G. målretting epidermal vekstfaktor reseptor signalering: tidlige resultater og fremtidige trender i onkologi. Ann Med 2003;5(35):327-36.
3. González G Og Lage A. Kreftvaksiner For Hormonimmunmangel: EGF Vaksine Tilnærming: Ledende Emner I Kreftforskning, Kapittel 11, Ed Nova Publishers, 2007.
4. González G Og Lage A. kreftvaksiner for hormon / vekstfaktor immunmangel: en mulig tilnærming til kreftbehandling. Curr Kreft Narkotika Mål 2007; 7: 229-41.
5. Gonz ④lez g, Crombet T, Torres F, Catala M, Alfonso L, Osorio M, et al. Epidermal Vekstfaktor-basert kreftvaksine for ikke – småcellet lungekreft terapi. Ann Oncol 2003; 14: 461-6.
6. Crombet T, Neninger E, Katalognummer M, Garcupuna B, Leonard I, Mart5ez L, Et al. Behandling AV NSCLC-pasienter med EN EGF-basert kreftvaksine. Rapport fra en fase i-rettssak. Kreft Biol Ther 2006;5 (2): 136-41.
7. Gonzá G, Crombet T, Neninger E, Viada C, Lage A. Terapeutisk vaksinasjon med epidermal vekstfaktor (EGF) ved avansert lungekreft: analyse av samlede data fra tre kliniske studier. Hum Vaksiner 2007; 3 (1): 8-13.
8. Neninger E, De La Torre A, Osorio M, Catald M, Bravo I, Mendoza M, Et al. Fase II randomisert kontrollert studie av en epidermal vekstfaktorvaksine ved avansert ikke-småcellet lungekreft. J Clin Oncol 2008;26: 1452-8.
9. Garcupuna B, Neninger E, De La Torre A, Leonard I, Mart@nez R, Viada C, et al. Effektiv hemming av epidermal Vekstfaktor / Epidermal Vekstfaktorreseptorbinding av Anti-Epidermale Vekstfaktorantistoffer er relatert til bedre overlevelse hos avanserte ikke-småcellet lungekreftpasienter behandlet med Epidermal Vekstfaktorvaksine. Clin Kreft Res 2008; 14 (3): 840-6.
10. Neninger E, Verdecia BG, Crombet T, Viada C, Pereda S, Leonard I, et al. Kombinere EN EGF – basert kreftvaksine med kjemoterapi i avansert ikke-småcellet lungekreft. J Immunother 2009; 32: 92-9.
11. A, A, A, a, a, A, A, A, a, a, a, et al. Produksjonsprosessutvikling for en epidermal vekstfaktorbasert kreftvaksine. Bio-pharm Int, Vaksiner Suppl, Okt 2008.
Leave a Reply