Carbon :essentials
Carbon Er En Gruppe 14 element og distribueres svært mye i naturen. Den finnes i overflod i solen, stjerner, kometer og atmosfærer på de fleste planeter. Karbon er tilstede som karbondioksid i atmosfæren og oppløst i alle naturlige farvann. Det er en komponent av bergarter som karbonater av kalsium (kalkstein), magnesium og jern. Atmosfæren På Mars er veldig tynn, men Hva det er inneholder ca 95 % CO2.Kull, petroleum og naturgass er hovedsakelig hydrokarboner. Karbon er unikt blant elementene i det store antallet forskjellige forbindelser det kan danne. Organisk kjemi, en 1/112 delmengde av uorganisk kjemi, er studiet av karbon og dets forbindelser. Mens silisium kan erstatte karbon i å danne en rekke relaterte forbindelser, er det ikke mulig for tiden å danne stabile forbindelser med svært lange kjeder av silisiumatomer.Karbon finnes fritt i naturen i tre allotrope former: amorf, grafitt og diamant. Grafitt er en av de mykeste kjente materialer mens diamant er en av de vanskeligste. Karbon, som mikroskopiske diamanter, finnes i noen meteoritter. Naturlige diamanter finnes i gamle vulkanske » rør » som finnes I Sør-Afrika. Diamanter er også utvinnes fra havbunnen utenfor Kapp Det Gode Håp.

en diamantring.
Mer nylig ble det oppdaget en annen form for karbon, buckminsterfullerene, C60. Denne form for karbon er gjenstand for stor interesse for forskningslaboratorier i dag.
Rent karbon er tilgjengelig i en rekke forskjellige former (allotroper). Den vanligste formen for rent karbon er α-grafitt. Dette er også den termodynamisk mest stabile formen. Diamant er en annen form for karbon, men er mye mindre vanlig. Andre former for karbon inkluderer fullerenene. Mens diamant og grafitt er uendelige gitter, er fullerener som buckminsterfullerene, C60, en diskret molekylær art. Amorfe former av karbon som sot og lampeblack er materialer som består av svært små partikler av grafitt.
de fleste grafitt er α-grafitt og den har en lagstruktur der hvert karbon er direkte bundet til tre andre karbonatomer i en avstand på 141.5 pm. Delokalisering i bindingen er tydelig siden C – c-avstandene er like og kortere enn normale karbon-karbon enkeltbindinger (typcally 154 pm). Avstanden mellom lagene av karbonatomer er 335,4 pm. I de fleste grafitt (α-grafitt)er lagene av atomer arrangert i EN ABABAB… gjenta mote men den β-formen (rhomboedral) stablingen ER ABCABCABC… selv om karbon-karbonavstandene og mellomlagsavstanden forblir de samme som i α-formen. Entalpi-forskjellen mellom α – og α-grafitt er mindre enn 1 kJ mol-1 (0.59 ± 0.17 kJ mol-1. Former av de tyngre elementene som svarer til grafitt er ikke kjent, og strukturer av silisium, germanium og grå tinn er relatert til diamantstrukturen (nedenfor).

Atomarrangementer i de vanligste allotrops av karbon: α-grafitt.
som diamant har en litt mer kompakt struktur dens tetthet er større enn grafitt. Utseendet til diamant er velkjent, og det er også et av de vanskeligste materialene som er kjent. Som grafitt er det relativt ureaktivt, men brenner i luft ved 600-800°C. Hvert karbonatom er bundet til fire naboer i en avstand på 154.45 pm på en tetrahedral måte, og hver diamantkrystall er en enkelt gigantisk gitterstruktur. I prinsippet (og i praksis!) grafitt kan omdannes til diamant ved anvendelse av varme og trykk. Enhetscellen av diamant er kubisk med a = 356,68 pm. Nesten alle diamanter besitter denne strukturen, men en svært liten prosentandel viser en sekskantet struktur relatert til wurtzite og disse kalles lonsdaleite.

Krystall strucutres av diamant.
nylig ble en annen allotrope av karbon karakterisert. Mens diamant og grafitt er uendelige gitter, er buckminsterfullerene, C60, en diskret molekylær art. Buckminsterfullerene molekylet er et nett av 12 pentagoner og 20 sekskanter brettet inn i en sfære. Effekten er veldig lik patchwork av 12 femkantede og 20 sekskantede lærstykker som sys sammen utgjør en fotballfotball (fotball). Navnet buckminsterfullerene (eller buckyball ble laget på grunn Av forholdet mellom strukturen Til C60 og R. Buckminster Fullers geodetiske kuppeldesign. Buckminsterfullerene er nå kommersielt tilgjengelige og har også blitt identifisert i interstellare rom og sot.
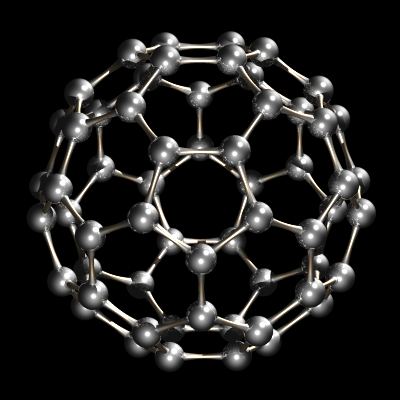
C60, Buckminsterfullerene.Andre fullerener (lukkede karbonmerder) Som C60 Og C84 er også kjent, og inded er tilgjengelig kommersielt. Den minste fullerene mulige er dodekahedral C20, bestående av 12 pentagoner og ingen sekskanter i det hele tatt. Nanorør er relatert til fullerener. De er rør som gir utseendet på rullet grafitt, selv om de er laget av grafitt. De er åpne, mens fullerener er lukkede strukturer.et interessant trekk ved fullerener er deres evne til å omslutte atomer som kalium og andre alkalimetaller for å lage endohedrale strukturer betegnet Som [email protected] 1961 vedtok International Union Of Pure And Applied Chemistry (Iupac) isotopen 12c som grunnlag for atomvekter. Karbon-14, 14c, en isotop med en halveringstid på 5730 år, brukes til å date slike materialer som tre, arkeologiske prøver, etc. Karbon-13, 13C, er spesielt nyttig for isotopiske merkingsstudier siden det ikke er radioaktivt, men er en spin i = 1/2 kjerne og derfor en god NMR-kjerne.
Leave a Reply