CIMAvax-EGF:進行肺癌のための新規治療ワクチン
レポート
CIMAvax-EGF:進行肺癌のための新規治療ワクチン
Gisela González1、Agustin Lage1、Tania Crombet1、Gryssel Rodríguez1、Beatriz García1、Ariadna Cuevas1、Lisel Viña1、Norkis Arteaga1、Elia neninger2
分子免疫学の1center、cimave。 216corner15,Atabey,Playa,POBox16 040,Havana,Cuba
2hermanos Ameijeiras HospitalSan Lázaro#701e/Belascoín y Marqués González,Centro Habana,Havana City,Cuba.
要約
キューバ規制庁(CECMED)が進行した非小細胞肺癌(NSCLC)のためのCIMAvax-EGF癌ワクチンへの衛生登録を許可することを可能にする結果が示されている。 これは、キューバでの治療用ワクチンの最初の登録であり、世界でも肺癌ワクチンの最初の登録でもありました。 したがって、肺がん患者には独自の治療ワクチンが提供され、生存率とその生活の質が向上します。 この目的のために、重要な前臨床、臨床、規制、生産性および交渉の課題に直面することになっていた。 これらの分野で得られた結果は、18の科学論文がインパクトの高い雑誌に掲載され、4つの発明の対象となり、キューバやその他の国でいくつかの特許 前臨床の設定では、免疫原性、安全性および抗腫瘍効果は、異なる動物種で実証された。 臨床経験は1995年に始まりました。 これまで、キューバでは第i-II相臨床試験が、キューバでは第II相臨床試験が、カナダと英国では第II相臨床試験が締結されており、現在、キューバでは第III相臨床試験と同様に最適化された第II-III相臨床試験が進行中である。 規制分野では、ファストトラック登録戦略が設計され、実行されました。 このユニークな製品を開発するには、新しい規制概念が必要でした。 拡張可能で、再生可能で、制御された生産的なプロセスは完全なGMPの承諾を保障した品質システムとともに、遂行された。 無形資産の交渉:製品開発のための資金は、新しい交渉戦略を実装することから来ました。
キーワード:癌ワクチン、NSCLC、ファストトラック登録、CIMAvax-EGF、第II-III相臨床試験
はじめに
上皮成長因子受容体(EGFR)によって形成される系と癌発症に伴うそのリガンドとの関係はよく知られている。 類表皮起源腫瘍では、悪い予後および手術後の早期再発に関連するEGFRの過剰発現がある。 そのため、このシステムは抗腫瘍療法の重要な標的となっています。
細胞増殖機構は、EGFのEGFRへの結合によって開始される。 我々の治療アプローチは、それを免疫原性にし、体液性免疫応答を誘導するEGF製剤を有するワクチンで構成されています。 自己egfに結合する特異的な抗EGF抗体の産生は、それがEGFRに結合するのを防ぎ、それによって、その相互作用に由来する細胞増殖機構を誘発する(1−4)。
ここでは、このワクチン(CIMAvax-EGF)のキューバでの登録の結果を報告します。 これは、新しい臨床、規制、技術およびビジネスへの貢献からなるグローバル戦略の一部であり、世界中の18の国際的な科学論文および知的財産によっ また、キューバとペルーでCIMAvax-EGFの登録を可能にしたさまざまな分野の技術革新についても説明します。
結果と議論
EGFによるワクチン接種は安全であり、免疫原性であり、進行期の肺癌患者における良好な生活の質で生存を増加させる
進行期の非小細胞肺癌(NSCLC)の治療におけるCIMAvax-EGFの臨床経験は1995年に始まった。 これまでにキューバで第I-II相臨床試験が締結されており、キューバでは2つの無作為化第II相臨床試験が締結されており、カナダと英国では第III相臨床試験が進行中である。 800人以上の進行癌患者がCIMAvax–EGFで治療されており、それによって安全で免疫原性であり、良好な生活の質で生存を増加させることができることを実証して
第I-II相試験の主な目的は、最良のワクチン製剤(キャリアタンパク質およびアジュバント)、用量および治療スケジュールを決定することであった。 これらの結果は、キャリアタンパク質としてP64Kタンパク質とアジュバントとしてモンタニドISA51の利点を示した。 用量のスケーリングアップの免疫原性の増加も実証された(5-7)。
すべての第i-II相試験からプールされたデータの分析は、より良い抗体応答または良好な抗体応答者(GAR)を有する患者およびワクチン接種に起因する 同時の歴史的対照と比較した場合、すべてのワクチン接種患者の生存率の有意な増加も実証された(7)。
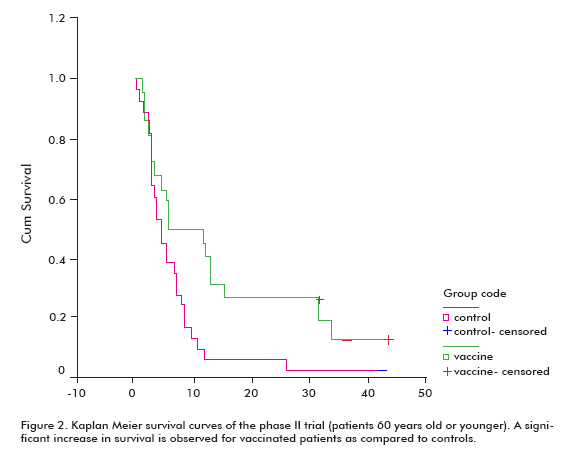
第II相臨床試験は、第一選択化学療法を締結した後、CIMAvax-EGFおよびbest supportive care(BSC)(40人の患者)またはBSC単独(40人の患者)を受けるために無作為化された80人の患者 前の調査結果はこの試験で裏付けられました。 ワクチン接種された患者の約50%はGARであり、GAR分類に達しなかった患者(貧しい抗体応答者、PARとして分類された患者)よりも有意に多く生存した。 同様に、最大の減少を有する患者は、この減少を示さなかった患者よりも有意に生存した(表1)。 抗EGF抗体価との間に有意な逆相関が観察され、これはワクチン接種患者では発生したが対照では発生しなかったため、ワクチン接種によって引き起こされたことが実証された(図1)。 非ワクチン接種対照(7.55±5)と比較して、すべてのワクチン接種患者(18.53±11.47;平均±中央値)で生存率が増加した傾向があった。33)、これは60歳以下の患者群で有意であった(Log rank test;p<0.05)(図2)(8)。 in vitro競合アッセイで証明されているように、ワクチン接種された患者からの血清は、EGFのEGFRへの結合を阻害した。
この結合阻害は、抗体力価および生存率に比例した。 さらに,ワクチン接種患者からの血清は,その抗EGF抗体価に比例してEGFRリン酸化を阻害した。
EGF/EGFR結合部位(EGF分子のループB)の優先認識を研究した。 その血清が優先的にループBを認識する患者は、このエピトープを認識しなかった患者よりも有意に多く生き残った(9)。
最近、キューバで用量/スケジュール最適化試験が締結されました(フェーズI-II)。 その設計では、以前の試験で免疫原性を増加させるすべての要素が考慮され、これには以下が含まれる: モンタニドISA51アジュバントとして、増加した用量、四つの注射部位およびワクチン接種に続く第一選択化学療法の前に二つのワクチン用量の投与。 この試験の結果は、免疫原性の有意な増加を示し、GARの95%は以前の最大抗体力価の10倍に達した。 すべてのワクチン接種されたpa-tientsは、第II相試験(10)からのコントロールよりも有意に多く生き残った。
EGF/EGFR結合およびEGFRリン酸化を阻害する患者の血清の能力の増加も見出された。 化学療法を終了した後,抗体応答はEGF分子のループBにシフトし,免疫応答の質の改善を示した。 この試験の結果は、用量および治療スケジュールを操作することによって到達できるCIMAvax-EGFに対する応答に改善の余地があることを実証した(10)。
これらの試験の結果は、キューバで現在進行中の第III相試験で検証されています。
すべての先進的な非小細胞肺癌患者が利用できるようにするためのワクチン登録のための規制戦略の設計と実施
CIMAvax-EGFは、世界でユニークな肺癌 グローバル戦略が設計され、実装されました;それは規制要件によって導かれました,キューバでのファーストトラック登録のための. スポンサー(CIM)とキューバ規制庁(CECMED)との密接な関係は、他の治療的代替なしに進行癌患者の利益のために製品を入手し、その迅速な適用のための要件を確 この戦略には、製品開発のさまざまなステップをカバーするための品質システム、品質管理、仕様、およびGMP要件の設計が含まれていました。 このグローバル戦略は、他の同様の製品の開発に使用することができます。
蓄積された規制上の経験と文書化は、さまざまな国での臨床試験の承認につながりました。 すべての情報を含む書類は、キューバとペルーでCIMAvax-EGFを登録することを可能にしました。 したがって、我々は異なる国での薬物登録のための定義された戦略を持っていることを述べることができます。
スケーラブルで一貫性があり、仕様に準拠した製品を生成するGMP製造プロセス
CIMAvax-EGFの製造プロセスを設計する最初の課題は、免疫原性EGF製剤を これは、ヒト組換えEGFの組換え膜タンパク質P6 4K(Neisseria meningitidis由来)への化学的結合によって得られた。 結合体は、適切なアジュバント(現在は、Seppic,FranceからのMontanide ISA5 1)と共に注入される。
実験室規模でのプロセスが最初に設計されました。 スケールアップ(および拡張可能な)衛生的で再現可能なプロセスは、後にGMPガイドラインに準拠して設計され、実装されました。 In vitroおよびin vivoの分析的な試金はまた原料および中間および最終製品の質を評価するために設計され、実行されました。
すべての変更は、現在の規制戦略によって評価され、サポートされました。 同等性試験の結果は、両方の製品を比較するために、スケールされたプロセスアプリケーションのCECMEDによる承認を受け、このプロセスで得られた製品の臨床 生産プロセスのスケールアップと最適化は、出版物(11)と新しい発明の対象に道を譲り、その後さまざまな国で特許が提示されました。
無形資産の交渉は、プロジェクト開発のための資金を米国に与え、また、異なる国の規制当局との共同作業での経験を学ぶ
このプロジェクトは、主に開発中の当社の製品の知的財産を通じてサポートされている”無形資産の交渉”の新しい概念に基づいて、外国のカウンターパートと交渉されました。 この交渉戦略は、他の国との共同開発のためのプロジェクトのライセンスで構成されていたため、外国のカウンターパートは、その地域での規制措置や臨床試験の費用をカバーしていたことを意味します。 これらの交渉の結果、キューバはマイルストーンの支払いを受けた。 交渉のためのこの様相はまた私達がそれにより私達の経験を高める専門家との一定した交換を国内外で持つことを可能にしました。 この交渉の様相の私達の肯定的な結果は私達の国で進行中の他のプロダクトに適用できます。
研究の関連性
CIMAvax-EGFは、キューバで登録された癌治療のための最初の治療ワクチンであり、肺癌治療のために世界で最初に登録されました。 肺がんは未解決の健康問題であり、毎年130万人以上の症例が診断され、世界中で同じ数の死亡者がいます。 キューバでは、それは年間4000人以上の死亡者の発生率を持つ男女両方の癌による死亡の主な原因です。 進行した段階で診断された患者に選択される治療法は、放射線療法と同時に投与することができる第一選択化学療法の治療法である。 これは緩和的で非治癒的な治療であり、化学療法に対する完全な反応は非常にまれであり、客観的な反応(完全または部分的)は患者の25%のみで起こる。
CIMAvax-EGFは、すでに第一選択化学療法を受けているこれらの患者のための代替治療を提供しています。 化学療法および/または放射線療法の治療の重篤な有害事象はよく知られており、生活の質を深刻に悪化させる。 代わりに、CIMAvax-EGFによるワクチン接種は、進行した肺癌患者の生存を改善し、良好な生活の質を提供しながら、従来の支持療法で解決することができる重
これまで、800人以上のキューバ人がCIMAvax-EGFで治療されており、全国の20以上の病院で治療されています。 CIMAvax-EGFの登録により、進行肺癌と診断された国のすべての患者に拡張することができます; 従ってキューバにこの治療上の代わりを使用して国民プログラムの世界の最初の国をすること。
経済的利益については、このプロジェクトの交渉を通じて、我々は6.346万ドルを得ています。 このプロジェクトの交渉戦略は、他の国との共同開発のためのものであり、外国の相手が自国の臨床試験の費用を負担し、手頃な価格にすることを意 これらの試験には数百万ドルの投資が必要であり、これは外国の対応者によってサポートされている場合にのみ可能です。 同時に、この戦略は、ここでの試験を実施する費用なしに、より多くの臨床データをキューバに提供します。 これまで、カナダ、英国、マレーシアで臨床試験が行われてきました。 近い将来、中国とヨーロッパで臨床試験が開始されます。
また、このライセンス戦略の一環として、外国のカウンターパートは、彼らが商業的権利を持っている地域での製品登録を担当しています。 登録およびマーケティングプロセス中に、キューバはマイルストーンの支払いを受け取り、その後、販売ロイヤリティとし
がんワクチンの世界市場は、数十億ドルのオーダーであると考えられています。 キューバに高度の肺癌の処置のための独特なプロダクトがあるという事実は私達の国民の健康システムのこのプロダクトの使用に資金を供給す
結論
CIMAvax-EGFによるワクチン接種は、安全で免疫原性であり、進行期の肺腫瘍患者における良好な生活の質を有する生存率の増加をもたらす。 このワクチンを登録するための規制戦略の設計と実施は、キューバの進行した非小細胞肺癌患者のすべての症例に対して利用可能にした
。 この肯定的な経験は、進行中の他の同様の製品にも適用可能である可能性があります。 生産プロセスは、スケーラブルで一貫性があり、再現性があり、GMPガイドラインに準拠しており、仕様に準拠した製品を生成するために開発されました。 無形資産の交渉の経験は非常に肯定的であり、異なる国の規制当局との共同作業から得られた学習経験を支援しながら、プロジェクト開発のための
謝辞
著者らは、この研究への彼らのcon-tributionのための分子免疫学センターから以下の専門家に感謝したいと思います: ロランド-ペレス、ロニー-カルボ、スハミー-アテンション、ベリンダ-サンチェス、アイリーン-ボーソレイユ、エルネスト-チコ、アイラマ-アルビサ、イレアナ-カルトロマン、セルヒオ-テイスティング、アナ-ヴェローゾ、レイナルド-クロウ、ヤネルダ-ロペス、ヨスニエル-エルナンデス、アントニオ-ヴァリン、アレハンドロ-ポルティージョ、リウバ-ウッド、グイド-フェレール、ダイアナ-ボルヘス、ニウビス-ペレス、タマラ-ガルシア、イダイン-ベイスン、マイラsantaelena、ホアキン-ソロザバル、アイダ-ロドリゲス、マリア-エレナ-ガルシア、アディス-トーレス、エリック-チョン、カルメン-ロール、モーリシャス-カタラ、ソライダ-アコスタ、バーバラ-ウィルキンソン、オルガ-トーレス、ノルマンド-イズナガ分子免疫学の中心から、またダニエルにそれらのすべて ゴンサレス、ルルドBコスタ、ガリーナMモヤ、ローランドPáez、ジェラルドGuillén、ヴィヴィアンPujol、遺伝子工学とバイオテクノロジーセンターからディノラトレス。
1. González G,Montero E,León K,Cohen IR,Lage A.im-munological homunculusの成分である表皮成長因子への自己免疫。 2002年1月89日から95日まで放送された。
2. Lage A,Crombet T,González G.上皮成長因子受容体シグナル伝達を標的とする:腫瘍学における初期の結果と将来の動向。 Ann Med2003;5(35):327-36.
3. González gおよびLage A.ホルモンの免疫剥奪のための癌ワクチン: EGFワクチンアプローチ:癌研究の主要なトピック、第11章、エド-ノヴァ出版社、2007。
4. González gおよびLage A.ホルモン/成長因子の免疫の剥奪のための癌ワクチン:癌治療のための実行可能なアプローチ。 Curr Cancer Drug Targets2007;7:229-41。
5. González G,Crombet T,Torres F,Catala M,Alfonso L,Osorio M,et al. 非小細胞肺癌治療のための上皮成長因子ベースの癌ワクチン。 アン-オンコール2003;14:461-6.
6. Crombet T,Neninger E,Catalá M,García B,Leonard I,Martínez L,et al. EGFベースの癌ワクチンを用いたNSCLC患者の治療。 第I相試験の報告書。 Cancer Biol Ther2 0 0 6;5(2):1 3 6−4 1.
7. González G,Crombet T,Neninger E,Viada C,Lage A.進行肺癌における表皮成長因子(EGF)による治療ワクチン接種:三つの臨床試験からのプールされたデータの分析。 2007年3月1日、8月13日にメジャー契約を結んでアクティブ-ロースター入りした。
8. Neninger E,De la Torre A,Osorio M,Catald M,Bravo I,Mendoza M,et al. 進行非小細胞肺癌における表皮成長因子ワクチンの第II相無作為化比較試験。 J Clin Oncol2008;26:1452-8.
9. ガルシアB,ネニンガー E,デ-ラ-トーレA,レナードI,マルティネスR,ヴィアダC,et al. 抗表皮成長因子抗体による表皮成長因子/表皮成長因子受容体結合の効果的阻害は,表皮成長因子ワクチンで治療された進行性非小細胞肺癌患者におけるより良い生存に関連している。 Clin Cancer Res2008;14(3):840-6.
10. Neninger E,Verdecia BG,Crombet T,Viada C,Pereda S,Leonard I,et al. 進行非小細胞肺癌における化学療法とEGFベースの癌ワクチンを組み合わせる。 2009年(平成32年)9月9日に廃止された。
11. A,A,a,a,a,a,a,a,a,a,a,a,a,a,a,a,a,a,a,a,a,a,a,a,a,a 上皮成長因子ベースの癌ワクチンの製造プロセス開発。 Bio-pharm Int,Vaccines Suppl,Oct2008.
Leave a Reply