水酸化ナトリウム
水酸化ナトリウム化学的性質、用途、生産
化学的性質
水酸化ナトリウムは、ペレット、フレーク、塊、またはスティックとして固体形態で市販されている白色、無臭、不揮発性アルカリ材料である。 水へのその溶解度は1 1 1重量%であり、蒸気圧は0mmHgである(NIOSH、1 9 9 4)。
トリコロエチレン(TCE)と反応して可燃性のジクロロアセチレンを形成し、金属と反応して水素ガスを形成することができる(OEHHA、1993)。 金属との反応性は、貯蔵ユニットおよび容器に関して考慮されるべきである。
水酸化ナトリウムは、苛性ソーダ、ソーダ灰汁、またはアルカリ液として単純として知られている水溶液 それに酸の中和を含むさまざまな使用が、あります;ペーパー、織物、プラスチック、腐食物、染料、ペンキ、ペンキの除去剤および石鹸の製造;石油の精錬;電気めっき; 覚せい剤の違法製造に急成長の使用がありました。
用途
水酸化ナトリウム(NaOH)は、最も有用な工業用ナトリウム化合物の一つです。 それはまた、灰汁または苛性ソーダとして知られており、家庭市場で最も強い塩基アルカリ(高pH値)の1つです。 それは下水管およびオーブンの洗剤として使用され、石鹸のthemanufactureの脂肪を鹸化します。 それは深刻な皮膚の火傷を引き起こすこともできるので、注意して使用する必要があります。
説明
水酸化ナトリウムは、アルカリ液および苛性ソーダとしても知られており、製品のpHを確立し、保持するために化粧品に少量で使用される水酸化ナトリウムは非常に多くの用途があるため、私たちの生活の中で非常に重要な化合物です。 それは化学工業で使用される非常に一般的なベースであり、その多くは私たちの日常生活の中で起こる多くのものに使用されています。 水酸化ナトリウムの最もよく知られた使用の1つはunclogging下水管の使用です。 それは排水クリーナーの多くの異なるブランドで来るが、最も一般的なの一つはドラノです。 それはまた、あなたの顔に皿から、実質的に何かを洗うために使用することができます灰汁石鹸の形で来ます。
水酸化ナトリウム構造
室温では、水酸化ナトリウムは、空気から水分を吸収する白色結晶無臭の固体 それは製造された物質です。 水酸化ナトリウムは、pHレベルを制御するために使用される無機化合物であり、化粧品およびパーソナルケア製品の緩衝剤として使用される。 それは石鹸の公式で歴史的に使用されたが、いろいろな方式で現在、浴室プロダクトを含んで、清潔になるプロダクト、芳香、フィートの粉、毛髪染料および色、構造、釘プロダクト、個人的な清潔プロダクト、シャンプー、剃るプロダクト、depilatories、スキンケアプロダクト、および日焼けプロダクト、また化学毛のストレートナおよび毛の波セット見られます。 それはまたWikipediaに従ってグリース、オイル、脂肪および蛋白質によって基づかせている沈殿物を、分解する機能のために石鹸、オーブンの洗剤、洗剤および下水管の洗剤のための化学基盤として産業溶媒の普及した原料である。 より少なく頻繁に、水酸化ナトリウムは歯磨き粉の原料として見られます。
水酸化ナトリウムはFDAの承認を受けており、直接食品添加物としてGRAS(一般的に安全として認識)の評価を受けています。 但し、それは主に農産物の洗浄そして化学皮で使用されます。 それはさまざまな集中の化粧品そしてパーソナルケアプロダクトの使用のために承認される:釘のクチクラの溶媒の重量5%、一般使用のための毛のストレートナの重量2%、専門の使用のための毛のストレートナの重量4.5%、depilatoriesのpH12.7まで、およびpHの調節装置として他の使用のpH11まで。
https://pubchem.ncbi.nlm.nih.gov/compound/sodium_hydroxide
http://sodiumhydroxide.weebly.com/uses.html
化学的性質
水酸化ナトリウム、NaOHは、苛性ソーダまたはナトリウム水和物(以前は灰汁として知られていた)とも呼ばれ、水、アルコール、グリセロールに可溶性の白色、塊状、潮解性の結晶性固体である。 それは318°C(606の)で溶け、最も広く利用され、利用できるアルカリ化学薬品です。 ほとんどの水酸化ナトリウムは、電解セルを使用して塩素の副生成物として生成されます。 ほとんどは蒸発し、50%および73%溶液または無水ビーズとして販売されます。 ほとんどの腐食性の最終用途は比較的低い集中の解決を要求する。 苛性ソーダは、分析試薬および化学中間体として、精練および洗浄浴、ゴム再利用および石油精製、鋼の熱処理のための焼入れ浴、切断および可溶性油、石鹸および洗剤、および他の多種多様な用途で使用される。
化学特性
NaOHは餌、薄片、固まり、または棒として販売される白く、無臭の、deliquescent材料です。 水溶液は、ソーダ灰汁として知られています
化学的性質
水酸化ナトリウムは、白色またはほぼ白色の融合塊として発生します。 それは小さい餌でisavailable、薄片、棒および他の形または形態。 それは堅く、壊れやすく、結晶のひびを示します。 Sodiumhydroxideは非常にdeliquescentであり、空気への露出でそれをrapidlyabs二酸化炭素および水吸収します。
物理的性質
ペレット、塊、スティック、ビーズ、チップ、フレークまたは溶液の形で製造された白色斜方晶結晶;吸湿性;非常に腐食性;急速にCO2と水を空気から吸収;密度2.13g/cm3;323°Cで溶融;1388°Cで気化;蒸気圧1torr at739°cと5torr at843°C;水に非常に可溶(室温で110g/100ml)、熱を発生させる溶解時;高アルカリ性水溶液、0.5%溶液約13および0.05%溶液約12のph;メタノール、エタノールおよびグリセロールに可溶(23.8g/100MLメタノールおよび13。周囲温度で9g/100mLのエタノール。).
用途
苛性ソーダは、最も広く使用されている化学物質。 酸を中和することを使用します;tomakeナトリウムの塩;金属のastheirの水酸化物を沈殿させるため;石油の精錬;エステルのthesaponification;処置のofcellulose、プラスチックおよびゴム;
使用
水酸化ナトリウムは無水薄片か餌としてまたは50%か73%の水溶液として商業的に販売されます。 それに無数の産業使用があり、地球規模の生産そして使用の点では上の10の化学薬品の1つです。 年間約1,500万トンの水酸化ナトリウムが使用されています。 生産の約半分を消費するその最も大きい使用は他の化学薬品の作成の基盤としてあります。 これは、pHを制御し、化学プロセスで酸を中和するために使用されます。 製紙業はパルプ化プロセスのナトリウムのhydoxideの広範な使用をする。 水酸化ナトリウムが接続のリグニンを分解することによって繊維を分けるのに使用されています。 これは、セルロースからのレーヨンの製造において同様の方法で使用される。 水酸化ナトリウムは石鹸の主化学薬品ですindustry.In ケン化プロセスは、動物や植物から得られたトリグリセリドは、グリセロールと石鹸を与えるためにabasic溶液中で加熱されます:
水酸化ナトリウムは、より容易に染料を作るために繊維を漂白し、処理するために繊維産業で使用されています。 石油産業は鋭い泥およびasaの殺菌剤で水酸化ナトリウムを使用します。 次亜塩素酸ナトリウム(NaOCl)は、洗浄および消毒剤として広く使用されています。一般的な家庭用漂白剤は、約5%次亜塩素酸ナトリウム溶液で構成されています。 亜塩素酸ソーダは、塩素を水酸化ナトリウムと反応させることによって調製される:Cl2(g)+2NaOH(aq)→NaOCl(aq)+NaCl(aq)+H2O(l)。 水酸化ナトリウムは、食品産業で洗浄に使用されています果物や野菜を剥がす。 水酸化ナトリウムは、多くの一般的な家庭用製品ではわずかな成分ですが、いくつかの製品では製品の半分以上を構成する可能性があります。 Dranocrystalsは30%の間で含み、60%の水酸化ナトリウムおよびある下水管の洗剤はconsistof100%の水酸化ナトリウムできます。
用途
水酸化ナトリウムは、水に可溶であり、水1mlに1gの溶解度を有するアルカリである。 これは、黒オリーブになるオリーブの苦い化学物質を破壊するために使用されます。 それはまたさまざまな食料品の酸を中和するために作用します。
使用
水酸化ナトリウムは、製品のpHを調整して皮膚に受け入れられるようにするために使用されます。 それは一般に苛性ソーダと呼ばれ、石鹸を作るときに化学試薬として役立つことが多い。 あまりにも集中した場合、それは重度の皮膚刺激を引き起こす可能性があります。
用途
水酸化ナトリウムは、最も重要な工業用化学物質の一つです。 容積では、それは米国で作り出される上の10の化学薬品にあります。 これは、いくつかのナトリウム塩を含む多数の化合物の製造、レーヨンおよびセロハンを製造するためのセルロースの処理、および石鹸、洗剤、パルプ、および紙の製造に使用される。 水酸化ナトリウムは、酸-塩基滴定および石油精製における酸の一般的な中和剤である。 別の主要な用途は、苛性ソーダとの融合などのアルカリ融合がしばしば鉱石を開くために適用される鉱石から金属を抽出することである。 さらに、水酸化ナトリウムが水酸化物として金属を沈殿させるのに使用されています。 他の用途は、ゴムの回収、プラスチック製造におけるカゼインの溶解、植物油の精製、繊維の加工、イオンクロマトグラフィー、エッチングおよび電気めっきの溶離液として、および実験室試薬としてである。 水酸化ナトリウムはまた、多くの有機合成および塩基触媒反応において強力な塩基として使用される。
使用
NaOHの解決が酸を中和し、硫酸および有機酸を取除く石油の精錬のナトリウムの塩を、例えば作るのに使用されています;ビスコースレーヨンおよ; カゼインを溶解するプラスチックを作ることで。 NaOHの解決は脂肪を加水分解し、石鹸を形作ります;それらは塩の水溶液からアルカロイド(基盤)およびほとんどの金属を(水酸化物として)沈殿させます。 薬の援助(alkalizer)。
調製
水酸化ナトリウムは、塩化ナトリウム溶液の電気分解によって塩素と一緒に製造される。 様々なタイプの電解セルが商業的に使用されている。 それらには、水銀細胞、横隔膜細胞、および膜細胞が含まれる。
塩水の飽和溶液を電気分解する。 塩素ガスは陽極で遊離し,ナトリウムイオンは陰極で遊離する。 水の分解は水素と水酸化物イオンを生成します。 水酸化イオンはnaohを形成するナトリウムイオンと結合する。 全体的な電解反応は次のように表すことができます。
2na++2cl-+2H2O→Cl2(g)+H2(g)+2naoh(aq)
水銀セルは、二つのセルで別々に起こる二段階で進行します。 最初のものは塩水セルまたはアマルガムを形成する水銀陰極にナトリウムイオンが沈着し、塩素ガスが陽極で遊離される一次電解槽として知られて:
Na++Cl–→Na-Hg(陰極)+β cl2(g)(陽極)
分解セルとして知られている第二のセルでは、グラファイト陰極が使用され、ナトリウムアマルガムが陽極として機能する。 水は分解器のアマルガムのナトリウムの金属と反応します:
Na-Hg+H2O→Na++OH–+Γ h2+Hg
塩素アルカリのダイヤフラムの細胞では、ダイヤフラムは陰極で発生する水酸化ナトリウムおよび水素から陽極で解放される塩素を分けるために用いられます。 ダイヤフラムがなければ、形成された水酸化ナトリウムは塩素と結合して次亜塩素酸ナトリウムおよび塩素酸塩を形成する。 多くの細胞では、石綿ダイヤフラムは、このような分離のために使用されています。 多くのタイプのダイヤフラムの細胞は利用できます。
水酸化ナトリウムは、無水固体または50%水溶液として製造される。
定義
最も重要な商業caustic。
製造方法
水酸化ナトリウムは、inert電極を用いて塩水を電気分解することによって製造される。 塩素は陽極でガスとして発生し、水素は陰極でガスとして発生します。 Chlorideandの水素イオンの取り外しは解決でナトリウムおよび水酸化物イオンを残します。溶液を乾燥させて固体水酸化ナトリウムを生成する。
第二の方法は、Kellner–Solvayセルを使用しています。 飽和塩化ナトリウム溶液を炭素陽極と水銀陰極の間で電気分解する。 この場合ナトリウムは水銀で分解する準備のofsodiumのために水素よりもむしろthecathodeで作り出されます。 ナトリウム-水銀アマルガムは水に曝され、水酸化ナトリウム溶液が生成される。
反応
水酸化ナトリウムは強アルカリ性であり、酸と反応して塩および水を形成することができる。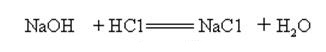
水酸化ナトリウムは酸性酸化物と反応して塩と水を形成するので、水酸化ナトリウムは実験室または工業的に酸性ガスを吸収す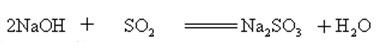
水酸化ナトリウムは、ナトリウム塩と金属水酸化物を形成するために多くの金属塩の水溶液と反応することができます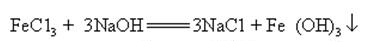
水酸化ナトリウムとアンモニア塩が一緒に加熱されると、アンモニアを放出することができます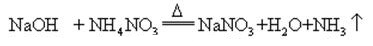
水酸化ナトリウムは非常に腐食性があり、水酸化ナトリウムを格納するガラス瓶溶液はゴム栓でなければならず、化学反応が開くのを防ぐためにガラス栓を使用すべきではありません。 水酸化ナトリウムは重要な工業原料であり、生理食塩水の電気分解によって工業的に製造することができる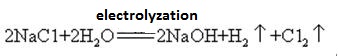
一般的な説明
白色固体。 金属およびティッシュに腐食性。 、石油の精錬化学製造業で使用される、クリーニングの混合物、下水管の洗剤。
空気&水の反応
水に可溶。 溶解は、十分な熱を放出して蒸気や飛散を引き起こし、隣接する可燃性物質を発火させる可能性があります。
反応性プロファイル
苛性ソーダ(水酸化ナトリウム)は強い塩基です。 有機および無機の両方の酸と急速かつ発熱的に反応する。 容易に可燃性の水素ガスの進化を用いるアルミニウムそして亜鉛を攻撃する腐食性の半固体を与えるために空気からの湿気を吸収します。 アセトアルデヒドおよび他の重合可能な混合物の重合に触媒作用を及ぼします;これらの反作用は激しく起こることができます例えば、acroleinは水酸化ナ 局所加熱によって開始されると五酸化リンと大きな暴力と反応する。 しばしば過酸化物を含むテトラヒドロフランとの接触(乾燥剤として)は危険である可能性がある—化学的に類似した水酸化カリウムのような使用で爆発が発生している。 氷酢酸、無水酢酸、アクロレイン、クロロヒドリン、クロロスルホン酸、エチレンシアノヒドリン、グリオキサール、塩酸(36%)、フッ化水素酸(48.7%)、硝酸(70%)、発煙硫酸、プロピオラクトン、硫酸(96%)。 苛性洗浄液(おそらく水酸化ナトリウムを含む)とペントールとの間の偶発的な接触は、激しい爆発を引き起こした。 . 試みられた合成中にメチルアルコールとトリクロロベンゼンの混合物を用いて加熱すると,圧力が急激に上昇し,爆発した。 高温および/または濃縮されたNaOHは、ハイドロキノンが高温で発熱的に分解する可能性があります。 (Nfpa Pub. 491M,1975,385)
ハザード
mois-tureの存在下で組織に腐食性,組織への強い刺激物(目,皮膚,粘膜,および上気道),毒byingestion.
健康被害
接触した組織に対する強い腐食作用。 吸入:塵により上気道および肺自体への損害を与えるかもしれま穏やかな鼻の苛立ちからpneumonitisに作り出します。 摂取:粘膜への厳しい損傷;厳しい傷の形成かパーホレーションは起こるかもしれません。 アイコンタクト:深刻な損傷を生成します。
健康上の危険
水酸化ナトリウムは非常に腐食性のsubstancethatの原因人間のティッシュへの損傷です。皮膚へのその作用は多少異なる酸の火傷から。 即時の痛みはありませんが、皮膚に浸透します。 それはそれ以上の浸透を防ぐために凝固しない従って腐食性の焼跡はsevereandの遅い治療になることができます。 集中した溶液を目にこぼすと、重度の刺激または永久的な傷害を引き起こす可能性があります。
それはそのほこりの吸入だけでなく、摂取によって毒性があります。 腐食性ソーダの口頭毒性のofa5-10%の解決が試験動物で低いfoundtoだったが、高い適量のatgreaterの集中により嘔吐、衰弱および崩壊を引き起こすことができます。 経口致死用量は500mg/kgである(NIOSH1986)。
水酸化ナトリウムの粉塵やエアロゾルが目、鼻、喉に刺激を与えます。 空気中の高濃度への延長暴露鼻道の潰瘍を生じる可能性がある。
火災危険
不燃性、物質自体は燃えませんが、腐食性および/または有毒な発煙を作り出すために熱することに分解するかもしれません。 いくつかは酸化剤であり、可燃物(木材、紙、油、衣類など)を発火させる可能性があります。). 金属との接触は可燃性の水素ガスを発生させる可能性があります。 容器は熱されたとき爆発するかもしれません。
可燃性およびExplosibility
水酸化ナトリウムおよび水酸化カリウムは固体またはaqueoussolutionsとして可燃性ではないです。
薬剤の適用
水酸化ナトリウムは薬剤の公式のtoadjustで広く利用されています解決のpH。 また、弱酸と反応して塩を形成するために使用することができる。
産業使用
苛性ソーダ(NaOH)は最も強いアルカリpHの調整装置とみなされます。 腐食性のsodaisは非常に活動的な物質非常に腐食性です。 苛性ソーダの大部分は製造されている飽和塩水(NaCl)の電気分解によって。 苛性ソーダは、他のアルカリ性物質と比較して比較的低い用量で非常に強いpHregulatingcapability(すなわちpH7からpH14まで)を有する。 商業的には、苛性ソーダは無水形態で入手可能であるが、ほとんどの鉱業用途では、苛性ソーダは50%溶液として供給される。
鉱物加工業界では、水酸化ナトリウムは、主に非金属鉱物の処理中のアルカリ度制御のために使用されています。 母材の浮遊では、水酸化ナトリウムはまれです。
安全プロファイル
腹腔内経路による毒。 摂取によって適度に有毒。 突然変異データが報告された。 皮膚、目、および粘膜への腐食性の刺激物。 分解するために熱されたときそれはナノの有毒な発煙を出します。
安全
水酸化ナトリウムは薬剤およびfoodindustriesで広く利用されて、lowconcentrationsの無毒な材料と一般にみなされます。 高濃度では、それは腐食性の刺激物である皮膚、眼、および粘膜。LD50(マウス、IP):0.04g/kg LD50(ウサギ、経口):0.5g/kg
潜在的な暴露
NaOHは、酸を中和し、石油精製、ビスコースレーヨンでナトリウム塩を作るために利用さ; そして、それらの塩の溶液の埋め立てで。 それは金属のクリーニングのmercerized綿、ペーパー、爆薬および染料の製造で使用されます;亜鉛の電気分解の抽出;錫めっき;酸化物のコーティング;洗濯、dishwashing bleaching;そし
貯蔵
splashgogglesおよび不浸透性の手袋は目および皮膚の接触を防ぐためにthesesubstancesを扱うときいつも身に着けられているべきです。 エアロゾルを生成する可能性のある金属水酸化物溶液を用いた操作は、吸入による暴露を防ぐために、煙道で行うべきである。 NaOHおよびKOHは水で分解するかなりのheatwhenを発生させます;水と混合した場合、thewaterに腐食剤を常にゆっくり加え、絶えずかき混ぜて下さい。 決してsolidhydroxidesに限られた量の水を加えないで下さい。 水酸化物の容器は、酸および相容れない物質から分離された涼しく乾燥した場所に保管する必要があります。
貯蔵
水酸化ナトリウムは涼しく、乾燥した場所の気密のnonmetalliccontainerで貯えられるべきです。 空気に曝されると、水酸化ナトリウムは急速に水分を吸収して液化するが、その後二酸化炭素の吸収と炭酸ナトリウムの形成により再び固体になる。
出荷
UN1823NaOH、固体、危険クラス:8;ラベル:8-腐食性材料。 UN1824NaOHの解決、危険のクラス:8;ラベル:8腐食性材料
浄化方法
共通の不純物は水および炭酸ナトリウムです。 水酸化ナトリウムは、100gを1Lの純粋なEtOHに溶解し、微細な焼結ガラスディスクを介して真空下で溶液を濾過して不溶性の炭酸塩およびハロゲン化物を除去することによって精製することができる。 (これおよびそれに続く操作は乾燥した、二酸化炭素なしの箱で行われるべきです。)溶液を穏やかな加熱を用いて真空下で濃縮し、モノアルコラートの厚いスラリーを得、これを粗い焼結ガラスディスクに移し、母液を含まない排気する。 微量の水を除去するために精製されたアルコールで結晶を数回洗浄した後、それらを真空中で穏やかな加熱で約30時間乾燥させてアルコラートを分解し、微細な白色の結晶性粉末を残す。 苛性ソーダ 水酸化ナトリウム溶液(苛性)、14.77。 炭酸イオンは、陰イオン交換カラム(Amberlite IR A−4 0 0;O H−形態など)を通過することによって除去することができる。 カラムは塩化物の形態から流水が塩化物イオンのためのテストを与えないまで水酸化ナトリウムの解決の遅い前の道によって新たに準備される 使用の後で、コラムは希薄なHClとの洗浄、そして水によって再生することができます。 同様に、他の金属イオンは、1M(またはそれ以上の希釈)Naoh溶液が、そのNa+−形態のdowexイオン交換a−1樹脂のカラムを通過するときに除去される。 また、炭酸塩の汚染はNAOH(分析的な試薬の質)の棒をH2Oと急速に洗浄し、次に蒸溜されたH2Oで分解するか、またはNaOHの集中された水溶液を準備し、明確な上清の液体を離れて引くことによって減らすことができます。 (不溶性のNa2Co3は残されています。 炭酸塩汚染は、わずかに過剰の濃縮されたBacl2またはB a(O H)2をNaoh溶液に添加し、よく振盪し、Baco3沈殿物を沈降させることによって減少させることがで 溶液中のB Aの存在が許容されない場合、電解精製を使用することができる。 例えば、ナトリウムのアマルガムは陰極のための純粋な水銀の3Lの30%NaOHの500ml、および厚い壁のポリエチレンのびんの15のfaradaysを4ampsで渡すプラチナ陽極の電気分解によって、準備されます。 びんは入口および出口の管、二酸化炭素なしのN2によって洗い流される使われた解決によってそれから合います。 アマルガムは大量の脱イオン水で完全に洗浄されます(電解電流はNaの損失を最小限に抑えるためにオンになっています)。 最後に、きれいな鋼鉄棒はアマルガムが付いている解決で接触に(水素の進化を促進するために)置かれ、適した集中が達されるまで、貯蔵容器に移り、要求されるように薄くなる前に進行するように反作用。
非互換性
強い塩基と強い酸化剤。 酸との激しい反応。 水と互換性がない;可燃性液体; 有機ハロゲン、ニトロメタン、およびニトロ化合物、可燃物。 急速に空気からの二酸化炭素そして水を吸収します。 水分や水と接触すると熱が発生することがあります。 金属に腐食性があります。 爆発性の水素ガスを形作る湿気の前の亜鉛、アルミニウム、錫および鉛が付いている接触。 プラスチック、ゴムまたはコーティングのある形態を攻撃する。
非互換性
水酸化ナトリウムは強塩基であり、容易に加水分解または酸化を受けるanycompoundと互換性がありません。 それは水溶液の酸、エステルおよびエーテルと、特にwillreact。
廃棄物処理
水を含むタンクに排出し、中和し、次に水で下水道に洗い流す。
規制ステータス
GRASが記載されています。 ヨーロッパの食品添加物として使用のために受け入れられる。FDA不活性成分データベースに含まれています(歯科準備;注射;吸入;鼻、眼科、経口、耳、直腸、局所、および膣の調製物)。 イギリスで認可されるnonparenteralandの非経口的な薬に含まれていて。 許容される非薬用成分のカナダのリストに含まれています。
Leave a Reply