最近の記事を見てみましょう
要約
頸動脈体腫瘍はまれであり、成長が遅い、血管過多神経内分泌腫瘍である。 これらの腫瘍は良性新生物であるが、悪性形質転換の傾向もある。 完全な外科切除は頸動脈ボディ腫瘍の処置のための金本位の治療上の様相である。 早期の外科的除去は、より高い罹患率および死亡率に関連するより大きく、より高度な腫瘍の発症を予防するために推奨される。 本報告では,完全外科的切除に成功した頚動脈体腫ようの三つの症例を提示し,現在の文献をレビューした。 さらに,患者の年齢や腫ようの大きさにかかわらず,早期の外科的管理の必要性を強調した。
キーワード
頸動脈体腫瘍、管理、外科的切除
はじめに
頸動脈体腫瘍(CBTs)は、傍神経節腫またはchemodectomasとしても知られており、胚性神経堤に由来するグロームス細胞内の頸動脈分岐部付近に生じるまれな神経内分泌新生物である。 Cbtの報告された発生率は1-2あたり100,000です。 これらの腫瘍の大部分は無症候性であり、最初は身体検査中の頸部腫脹の検査および触診によって、またはより一般的には放射線画像検査の付随的 それにもかかわらず、最も観察された症状は、症候性の症例における痛み、嚥下障害および自律神経機能障害である。 Cbtは良性病変ですが、全症例の約10%で悪性腫瘍になる傾向があります。 したがって,局所浸潤および転移を避けるために,早期の外科的切除がCbtの治療のためのプライマー治療の選択肢として考えられる。 本稿では,完全外科的切除に成功したCBTの三つの症例を報告し,現在の文献をレビューした。
外科的アプローチ
手術について通知し、外科的同意書を取得した後、全身麻酔下での一次切除のために手術室に連れて行った。 腫よう腫りゅうは斜め頚部切開を介して接近した。 基本的な外科的原則は,腫よう切除を試みる前に完全な解剖学的解剖と血管制御を含んでいた。 この目的のために、すべての神経血管構造が同定され、頸動脈の高度周囲切開が行われた。 総頸動脈、内頸動脈および外頸動脈は、腫瘍切除前に血管テープを用いて拘束された(図1)。 腫瘍を供給する栄養血管を最初に結紮し、その後、腫瘍を隣接する構造から単離し、切除した(図2aおよび2b)。 Shamblin型iおよびIIでは頚動脈の下部切開なしで腫りゅうを完全に切除したが,Shamblin型IIIでは動脈の下部平面に沿って切開を行い,完全な局所腫よう切除と頚動脈の保存を可能にした。 全ての症例において,腫りゅうは神経血管損傷を伴わずに切除した。
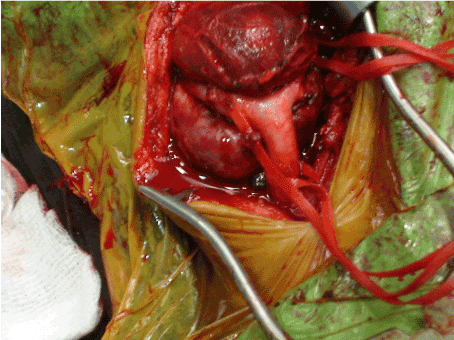
図1. 完全切除前の頸動脈体腫ようの術中所見。
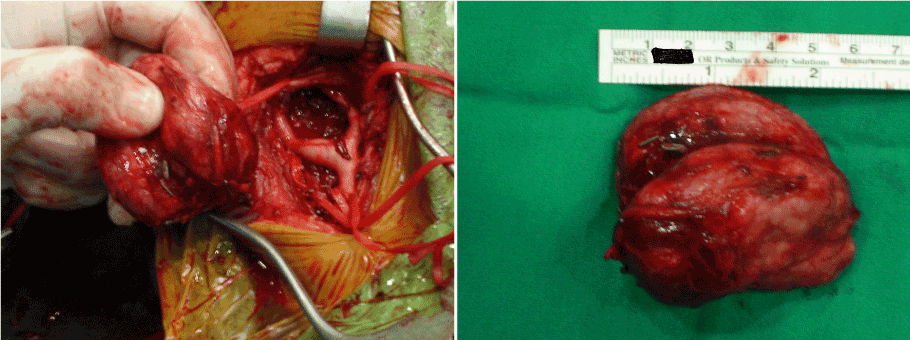
図2aおよび2b。 完全切除後の頸動脈体腫ようの術中所見。
ケースプレゼンテーション
ケース1
66歳の女性患者は、右頸部の腫れの存在のために私たちの外来診療所に入院しました。 身体検査、二重超音波検査およびコンピュータ断層撮影血管造影は、CBTと考えられていた15x15x11mmを測定する右頸動脈分岐上の塊を明らかにした。 診断成立後できるだけ早期に手術を行った。 術中にShamblini型と認めた。 彼女は手術後の綿密な監視のために集中治療室に移された。 術後1日目にドレーンを除去して診療所に転院した後,同日に問題なく退院した。
ケース2
75歳の女性患者は、右頸部にめまいや腫れの存在のために私たちの外来診療所に入院しました。 身体検査、二重超音波検査およびコンピュータ断層撮影血管造影は、CBTと考えられていた40x30x24mmを測定する右頸動脈分岐に塊を明らかにした。 さらに、椎骨基底不全は、二重超音波検査所見(椎骨動脈の総体積=166mL/分)に従って検出された。 診断成立後できるだけ早期に手術を行った。 術中にShamblinii型と診断した。 彼女は手術後の綿密な監視のために集中治療室に移された。 術後1日目にドレーンを除去し、患者は診療所に移送され、その後術後2日目に問題なく退院した。
ケース3
50歳の女性患者は、右頸部にめまいや腫れの存在のために私たちの外来診療所に入院しました。 徐々に増加した彼女の症状は約15年間存在していた。 身体検査、二重超音波検査およびコンピュータ断層撮影血管造影は、CBTと考えられていた75x55x45mmを測定する右頸動脈分岐上の塊を明らかにした。 診断成立後できるだけ早期に手術を行った。 術中にShambliniii型と診断した。 彼女は手術後の綿密な監視のために集中治療室に移された。 術後4時間目に、患者は診療所に移された。 術後1日目にドレーンを除去し、術後2日目に問題なく退院した。頸動脈体は、1743年にフォン-ハラーによって初めて記載されました。 これは、主に外頸動脈の上行咽頭枝から走る摂食血管によって供給され、舌咽頭および迷走神経を介して神経支配される、頸動脈分岐部の外膜に位置する赤褐色の、十分に外接された、高度に特殊化された円形器官である2-6mmの大きさである。 それはアシドーシス、低酸素症およびhypercapneaによって刺激される化学受容器器官として作用し、sympathetic神経の流れを高めることによってこれらの変数の変更に応じて血圧、心拍数、呼吸および血の温度の自律的な制御の役割を担う。
Cbtは、すべての新生物の約0.03%を表す成長が遅い血管過多腫瘍です。 彼らは1:1.9の男女比で女性の性別でより一般的に表示されます。 これらの腫瘍は、10%で悪性、10%で家族性、および散発的な症例の10%で両側性であることが報告され、両側性は家族性の症例で30%に達することができる。
1971年、Shamblin、et al。 これらの腫瘍の切除可能性を決定するために、頸動脈との関係に応じた分類システムを導入した。 ShamblinのタイプIの腫瘍は集中させた固まりであり、周囲の頸動脈を含まない、タイプIIの腫瘍は付着しているか、または部分的に頸動脈を囲み、こうして切除することは比較的より困難であり、タイプIIIの腫瘍は大きく、容器を包み、こうして切除を試みる最も困難なタイプです。 Shamblin分類によれば、III型腫瘍は、より周術期の神経血管合併症および複雑な外科的処置と関連している。 それにもかかわらず、この分類システムに頸動脈を維持することは可能であるかどうか決定する頸動脈の壁を通って深い腫瘍がいかに浸透するか 従って、Luna−Oriz,et a l. 腫ようの大きさに関係なく血管外膜に浸潤することが臨床的または組織学的に確認されたShambliniibを作るためのShamblin分類システムの修正を示唆した。
Cbtの鑑別診断には、頸部反応性リンパ節腫脹、外側頸部嚢胞、上腕嚢胞、迷走神経傍神経節腫、甲状腺結節、頸動脈動脈瘤、および耳下腺腫瘍が含まれる。 これらに加えて、頸動脈体過形成も記憶されるべきであり、慢性低酸素症のために発症する可能性があり、主に高地に住む患者に記載されている。
Cbtは、診断と治療のためのガイドラインが文献に不足しているため、診断と管理の困難を抱えています。 詳細な身体検査の後にCBTの診断が疑われる場合,診断はほとんどの場合,二重超音波検査,コンピュータ断層撮影血管造影,磁気共鳴血管造影およびデジタル減算血管造影などの放射線画像法によって確立される。 この頃は、超音波検査はそれが容易に利用でき、非侵襲的なイメージ投射様相であるのでスクリーニングのために広く利用されています。 さらに、彼らの多施設レビューとメタ分析では、共同血管研究グループは、二重超音波検査がCBTsの診断のための一次診断検査であることを推奨しています。 コンピュータ断層撮影および磁気共鳴は、腫瘍の大きさ、程度および侵襲性を評価するために提供する。 血管造影法は、腫瘍および術前塞栓形成を供給する血管の評価を可能にする。 これらの腫瘍のさまざまな管および神経構造へのhypervascularizationそして近さのために、診断方法としてバイオプシーは大きい出血および播種の危険を示し、pseudoaneurysmの形成
CBTの最初の成功した外科的除去は1889年にAlbertによって適用され、Gordon-Taylorは1940年に安全な亜adventitial解剖を定義しました。 手術中の摂食血管の結紮によるCbtの血管剥離は、1980年代から一般的な実用的な外科的方法であった。2008年には、van der Bogt,et al. 失血を最小限に抑え,周術期の罹患率のリスクを軽減する頭蓋尾郭清技術を示唆した。 この頃は、外科切除はまだcbtsの処置のための金本位の治療上の様相に残ります。
放射線療法(RT)は、腫瘍の大きさを減少させるか、またはその増殖を停止させる可能性のある代替治療法である。
放射線療法(RT)は、腫瘍の大きさを減 それは広範な介入、多数の腫瘍および高い操作中および麻酔の危険のために外科を経ることができない患者のために推薦されます。 Gilboらによって行われた研究では。 RTで治療された156例の傍神経節腫症例を有する最大のシリーズであり、著者らは45年の経験を提示し、わずか5つの腫瘍(3.2%)でサイズが減少し、5年後の腫瘍増殖の欠如が患者の99%で観察された。
術前塞栓術の有用性の問題は議論の余地がある。 いくつかの研究によれば、術前塞栓術は、血流を低下させ、腫瘍のサイズを減少させるので有益であり、それによって、特に大きな腫瘍においてより少ない失血を伴う完全な腫瘍除去を容易にする可能性がある。 一方,他のいくつかの研究では,術前塞栓術は,その無駄だけでなく,一過性脳虚血発作や塞栓粒子による脳卒中などの塞栓後の罹患率のリスクも考慮して推奨されなかった。
Cbtの外科的治療に関する主要な合併症には、血管損傷に続発する出血、脳神経欠損、および周術期脳卒中が含まれる。 合併症の割合はShamblin分類と正の相関を示した。 Davila,et al. 永久的な脳神経損傷の率は5.5%であり、脳卒中の率は1%の脳卒中であり、183例からなる一連の周術期死亡率はないと報告されている。 Pacheco-Ojedaはちょうど215外科的に切除されたCbtと文献の中で最大のケースシリーズを提示しています。 彼のケースシリーズでは、累積合併症率は27.5%であり、これらの合併症は主に軽度であり、脳神経機能障害に関連しており、周術期の脳卒中および死亡はな Cbts手術の合併症を検討した興味深い包括的なレビュー研究が最近発表された。 本研究では、625の19の研究からのケースの合計が見直され、一過性脳神経損傷、血管損傷、永久脳神経損傷、脳卒中および周術期死亡率の割合は、次のように見31%, 28%, 17%, 2.5% そして、それぞれ0,5%。
患者の年齢および腫瘍の大きさにかかわらず、より高い罹患率および死亡率に関連するより大きく進行した腫瘍(Shamblin class III)の発症を防ぐために、Cbtの早期 Cbtの完全な外科的切除は、主要なnorovascular構造への近接のために技術的に挑戦することができます,だけでなく、首の複雑な解剖学. 手術中、合併症の頻度を減少させるために、すべての神経血管構造を同定すべきである。 完全な腫よう切除を達成するためには,摂食枝の結さつを伴う頚動脈の近位および遠位の制御が重要である。 Cbtsの外科的切除は,主要な神経血管合併症および死亡率が低い非常に効果的で安全な手技であると結論した。 Cbtの早期発見そして完全な外科取り外しは結果を改善します。
- セビージャ-ガルシアMA,ジョレンテ-ペンダスJL,ロドリゴ-タピアJP,ガルシア-ロスタンG,スアレス-フェンテV,et al. (2007)頭頸部paragangliomas:89例の改訂73患者. アクタオトリノラリンゴルエスピーロ58: 94-100.
- イエナA、Reddy GV、Kadiyala V、Brinda K、Patnayak R、Chowhan AK(2016)大きな頸動脈体腫瘍の症例:外科的挑戦。 インドのJ Vasc Endovasc Surg3:96-98.
- Dixon JL、Atkins MD、Bohannon WT、Buckley CJ、Lairmore TC(2016)頸動脈体腫瘍の外科的管理:学際的なアプローチを採用した15年の単一機関の経験。 Proc(Bayl Univ Med Cent)29:16-20.
- Albsoul NM,Alsmady MM,Al-Aardah MI,Altaher RN(2009)頸動脈体paraganglioma管理と結果. Eur J Sci Res37:567-574.
- Gratiot JH(1943)頸動脈体腫瘍:集団レビュー。 77:177-186.
- Jianu DC、Jianu SN、Motoc AG、Dan TF、Poenaru M、et al. (2016)頸動脈体傍神経節腫の集学的管理に関する評価:七つの症例の報告。 Rom J Morphol Embryol57(2Suppl):853-859.
- Toktas F,Yümün G,Gücü A,Göncü T,Eris C,et al. ら(2 0 1 4)頸動脈体腫瘍のための保護的外科的処置:症例シリーズ。 Erciyes Med J36:133-135.
- Dorobisz K,Dorobisz T,Temporale H,ZatoÅ”ski T,et al. (2016)臨床経験および文献のレビューに基づく頸動脈傍神経節腫における診断および治療上の困難。 Adv Clin Exp Med25:1173-1177.
- Shamblin WR,ReMine WH,Sheps SG,Harrison EG Jr(1971)頸動脈体腫瘍(chemodectoma). 九十例の臨床病理学的分析。 アムJ Surg122:732-739.
- Luna-Oriz K,Rascon-Oriz M,Villavicencio-Valencia V,Herrera-Gomez A(2006)Shamblinの分類は頸動脈体腫瘍の術後罹患率を予測していますか? Shamblinの分類を変更する提案。 ユーロアーチオトルヒノリンゴル263: 171-175.
- Sajid MS,Hamilton G,Baker DM,Joint Vascular Research Group(2007)a multicenter review of carotid body tumour management. Eur J Vasc Endovasc Surg34:127-130.
- Ferrante AM、Boscarino G、Crea MA、Minelli F、Snider F(2015)子宮頸部傍神経節腫:44例の単一センター経験。 Acta Otorhinolaryngol Ital35:88-92.
- トンY(2012)頸動脈体腫瘍の診断および評価における二重超音波の役割:文献レビュー。 難治性希少Dis Res1:129-133.
- van der Mey AG、Jansen JC、van Baalen JM(2001)頸動脈体腫瘍の管理。 耳鼻咽喉科クリンノースAm34:907-924.
- Gordon-Taylor g(1940)頸動脈腫瘍について。 Br J Surg28:163-172.
- van der Bogt KE,Vrancken Peeters MP,van Baalen JM,Hamming JF(2008)頸動脈体腫瘍の切除:進化する外科的技術の結果。 Ann Surg247:877-884.
- Moore MG,Netterville JL,Mendenhall WM,Isaacson B,Nussenbaum B(2016)頭頸部paragangliomas:評価と管理に関する更新。 耳鼻咽喉科頭頸部外科154:597-605.
- Carroll W,Stenson K,Stringer S(2004)悪性頸動脈体腫瘍。 26:301-306
- Gilbo P,Morris CG,Amdur RJ,Werning JW,Dziegielewski PT,et al. (2014)良性頭頸部傍神経節腫に対する放射線療法:45年の経験。 癌120:3738-3743。
- Persky MS,Setton A,Niimi Y,Hartman J,Frank D,et al. (2002)頭頸部傍神経節腫の血管内および外科的治療を組み合わせた-チームアプローチ。 24:423-431.
- Kasper GC,Welling RE,Wladis AR,CaJacob DE,Grisham AD,et al. (2006)頸動脈傍神経節腫への学際的なアプローチ。 Vasc血管内Surg40:467-474.
- Jackson RS、Myhill JA、Padhya TA、McCaffrey JC、McCaffrey TVなど。 (2015)術前塞栓術が頸動脈傍神経節腫手術に及ぼす影響:系統的レビューおよびメタ分析。 耳鼻咽喉科頭頸部外科:943-950.
- Zeitler DM,Glick J,Har-El G(2010)頸動脈腫瘍手術における術前塞栓術:それは必要ですか? Ann Otol Rhinol Laryngol119:279-283.
- Sen I,Stephen E,Malepathi K,Agarwal S,Shyamkumar NK,et al. (2013)頸動脈体腫瘍における神経学的合併症:6年間の単一センターの経験。 J Vasc Surg57:64S-8S.
- Davila VJ,Chang JM,Stone WM,Fow RJ,Bower TC,et al. ら(2 0 1 6)頸動脈体腫瘍の現在の外科的管理。 J Vasc Surg64:1703-1710.
- Pacheco-Ojeda LA(2017)頸動脈体腫瘍:215例における外科的経験。 J Craniomaxillofac Surg.
- Amato B,Serra R,Fappiano F,Rossi R,Danzi M,et al. (2015)頸動脈体腫瘍手術の外科的合併症:レビュー。 34:15-22
Leave a Reply