化学結合
化学結合は、化合物を形成するために 結合には、分子化合物を結合する共有結合、塩やイオン結晶を結合するイオン結合、金属の原子を結合する金属結合の三つの主要なタイプがあります。
分子と共有結合
ほとんどの燃料、プラスチック、および天然物は、分子に一緒に結合した原子で作られた分子化合物です。
分子と共有結合
ほとんどの燃料、 分子の原子を接合する結合のタイプは、二つの原子の外側の電子が二つの原子の間で共有され、二つの原子の間に引力を作成するときに発生する共有結合である。
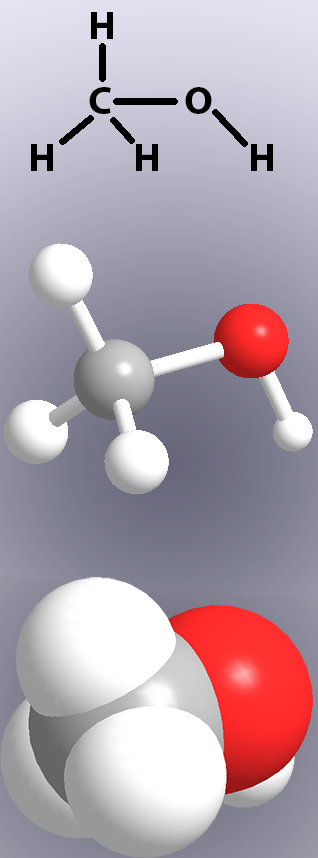
共有結合は、化学構造を線で示し(図1、上)、”棒”または原子の重なり合いを示す(図1、中央および下部)。
共有結合中の電子は、常に2つの原子間で等しく共有されているとは限りません。
共有が等しくない場合、一方の原子は非常にわずかな正の電荷を持ち、他方の原子はわずかに負になります。 この木枠は小さい電気双極子-双極子を含んでいる分子極性の化合物です。 分子が極性であるか非極性であるかは、融点や沸点、水素結合などの特性に影響します。 化学LibreText上の共有結合についての詳細を読みます。
イオンと金属結合
共有結合は二つの原子間の電子を共有することを含むが、イオン結合はある原子から別の原子への電子の完全な移動を含み、正と負のイオンを生成する。 これらのイオンは反対の充満間の引力によってそれから一緒に握られます。 イオン性化合物は、これらの誘因に基づいて結晶を形成する。
金属結合は、金属原子の価電子を完全に共有し、電子が自由に移動する「電子海」を作り出すことを含む。
金属結合は、金属原子の価電子を完全に共有することを含む。
これは金属の高い導電率の理由の一部です。 化学LibreTextで金属結合についての詳細を読む
エネルギーと化学結合
一般的に、エネルギーは、結合の種類に関係なく、二つの原子の間に結合が形成 同様に、2つの原子の間にすでに結合が存在する場合、それを破壊するためにエネルギーが必要になります。 結合を破壊するために必要なエネルギーの量は、それが形成されたときに放出されるエネルギーの量と同じである。 ほとんどの化学反応には、化学結合の破壊と生成の両方が含まれます。
新しい結合を形成することによって放出されるエネルギーが、「古い」結合を破壊するのに必要なエネルギーよりも大きい場合、エネルギーは反応によって全体的に放出されるであろう。 このエネルギーは熱として失われたり、電力に使用されたりすることがあります。
例えば、メタン(CH4)の燃焼は、この化学反応に従います:
この反応は、メタン中の四つの炭素-水素結合とO2中の酸素-酸素結合の破壊を含む。 形成される新しい結合は、2つの炭素-酸素結合(CO2中)および水素-酸素結合(H2O中)である。 これらの新しい結合は、元の結合よりも全体的にエネルギーが少ないため、この反応によってエネルギーが放出されます。 エネルギーを放出することは燃焼反応の特徴であり、熱い炎を感じるときにこれに気づいたかもしれません。 下のアニメーションは、メタンの炭化水素燃焼を示しています。 メタンのような炭化水素の燃焼中にCO2とH2Oを形成すると大量のエネルギーが放出されるため、これらは良好な一次エネルギー源です。
また、CO2中の結合を破壊し、他の分子を形成するために大量のエネルギーが必要であることを意味します。 これは、光合成がCO2を炭水化物に変換するために(日光から)非常に多くのエネルギーを必要とする理由の1つです。
さらに読むために
- 化学エネルギー
- 燃焼
- 一次エネルギー
- エネルギー変換技術
- またはランダムなページを探る
Leave a Reply