Recherche analytique et pharmaceutique
Spectres d’absorption
Le spectre d’absorption de la thiamine a été enregistré contre l’eau (Figure 1), il a été constaté que la thiamine présente un pic d’absorption maximal (λ max) à 235 nm. En raison du λ max fortement décalé vers le bleu de la thiamine, sa détermination sous la forme posologique basée sur la mesure directe de son absorption pour les ultraviolets est sensible aux interférences potentielles des excipients courants. Par conséquent, la dérivatisation de la thiamine pour atteindre des espèces absorbantes dans l’aire visible était sans aucun doute nécessaire. Ainsi, la dérivatisation de la thiamine avec le NBD-Cl a été réalisée et le spectre d’absorption du produit a été enregistré par rapport au blanc de réactif (figure 1). Il a été constaté que le produit est de couleur brune présentant λmax à 434 nm, et le λmax de NBD-Cl était de 342 nm. Le λmax du dérivé thiamine-NBD-Cl a été décalé vers le rouge, éliminant toute interférence potentielle. La longueur d’onde 434 nm a donc été fixée comme optimale.
Optimisation des conditions réactionnelles
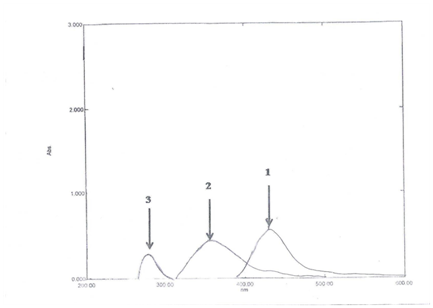
Figure 1 : Spectres d’absorption de la thiamine (3), du NBD-Cl(2) et du complexe qui les sépare (1).
Les conditions optimales pour la méthode développée ont été établies en faisant varier les paramètres un à la fois tout en maintenant les autres paramètres constants et en suivant l’effet exercé sur l’absorbance du produit coloré. Afin d’établir des conditions expérimentales, l’effet de divers paramètres tels que le pH, le temps, le volume tampon et la concentration de NBD-Cl ont été étudiés.
Effet du pH
L’effet du pH sur la réaction entre la thiamine et le NBD-Cl a été testé en faisant varier la forme de pH de 7,0 à 12,0. Comme le montre la figure 2, l’absorbance du produit est faible à pH 7,0, ce qui indique que la thiamine ne peut pas réagir avec (NBD-Cl) en milieu neutre. Ceci était peut-être dû à l’existence du groupe amino de la thiamine sous forme de sel de chlorhydrate, ce qui entrave la capacité de substitution nucléophile. À mesure que le pH augmentait de 7 à 12, les lectures augmentaient considérablement, libérant le groupe amino de la thiamine et facilitant la substitution nucléophile. L’absorption maximale a été atteinte à une valeur de pH de 10,5. À des valeurs de pH supérieures à 10,5, une diminution de l’absorption s’est produite. Ceci a été attribué probablement à l’augmentation de la quantité d’ion hydroxyde qui augmente la vitesse de réaction arrière de la thiamine avec le NBD-Cl.
Effet du temps de réaction
L’absorbance du produit de réaction a été surveillée à différents moments (Figure 3). En gardant les autres conditions intactes, l’absorbance du produit de réaction a été suivie après avoir été debout pendant différentes durées à 25 ° C. Les résultats montrent que la thiamine réagit avec le NBD-Cl à 25 ° C et que l’absorbance commence à augmenter progressivement et à atteindre un maximum après 25min. Pour des temps de réaction plus longs, une légère baisse de l’absorbance a été observée. En conséquence, 25 minutes ont été définies comme temps de réaction pratique pour la détermination.
Effet de la quantité du tampon
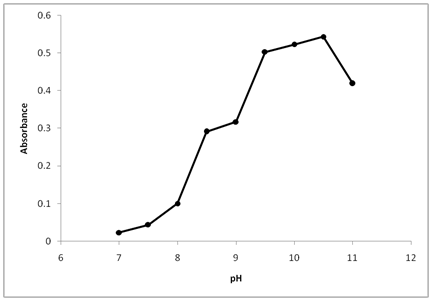
Figure 2 : Effet du pH sur la réaction de la Thiamine avec le NBD-Cl.
Thiamine (20µg/ml): 1 ml, NBD-Cl conc. 0,2% (p/v), temps de réaction 20 min.
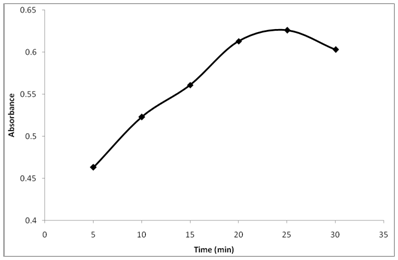
Figure 3: Effet du temps de réaction sur la réaction de la thiamine avec le NBD-Cl.
Thiamine (20µg/ml): 1 ml, Tampon (pH 10.5): 1,5 ml, NBD-Cl conc. 0,2% (p/v).
En maintenant un pH à 10,5, l’effet de la quantité de solution tampon sur l’absorbance du produit de réaction a également été étudié (Figure 4). La figure révèle que l’absorbance du produit de réaction augmente rapidement avec l’augmentation de la quantité de solution tampon, et devient maximale lorsque la quantité de solution tampon atteint 1,5 mL. Par conséquent, la quantité de solution tampon de 1,5 mL a été choisie pour assurer l’absorbance la plus élevée.
Effet de la concentration de NBD-Cl
L’étude de l’effet des concentrations de NBD-Cl a montré que la réaction dépendait de la concentration de réactif. L’intensité d’absorption la plus élevée a été atteinte à une concentration de NBD-Cl de 0,2% (p / v), et une concentration plus élevée de NBD-Cl entraîne une diminution de l’absorbance (figure 5).
À partir des expériences de réglage des paramètres ci-dessus, les conditions optimisées utilisées pour le test étaient: pH 10,5, concentration de NBD-Cl 0,2% (p / v), volume du tampon 1,5 mL, temps de réaction 25min et température 25ºC.
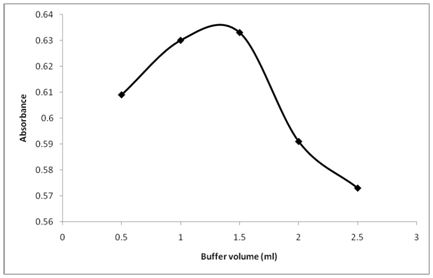
Figure 4: Effet de la quantité de tampon (ml) sur la réaction de la thiamine avec le NBD-Cl.
Thiamine (20µg/ml): 1 ml, pH du tampon: 10,5, NBD-Cl conc. 0,2% (p/v), temps de réaction 25 min.
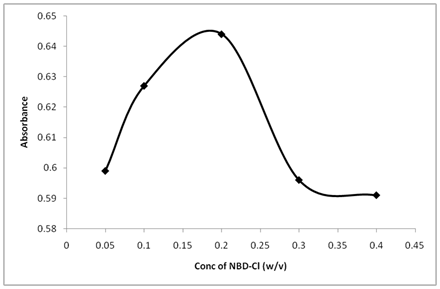
Figure 5: Effet de la concentration de NBD-Cl sur sa réaction avec la thiamine.
Thiamine (20µg / ml): 1 ml, Tampon (pH 10,5): 1,5 ml, temps de réaction 25 min.
Validation de la méthode
La méthode a été validée pour les paramètres suivants: spécificité, linéarité, précision, précision, limite de détection (LOD), limite de quantification (LOQ) et robustesse selon les directives de la Conférence internationale sur l’harmonisation (ICH).
Linéarité, limite de détection (LOD)limite de quantification (LOQ)
La linéarité a été évaluée par une analyse de régression linéaire déterminée en construisant sept concentrations de thiamine, dans la plage de 05–35µg / mL, qui a été calculée par la méthode de régression par les moindres carrés pour calculer l’équation d’étalonnage et le coefficient de corrélation. Les courbes d’étalonnage ont été construites en traçant la concentration par rapport à l’absorbance, à l’aide d’une analyse de régression linéaire. L’équation de régression pour les résultats était A = 0,033x-0,009 (r2 = 0,999), où A est l’absorbance à 434 nm, x est la concentration de thiamine en µg / mL dans la plage de 05 à 35 µg / mL, et r est le coefficient de corrélation (tableau 1). Il a été constaté que la plage de concentration linéaire est comparable à notre méthode précédente utilisant NQS. La limite de détection (LOD) et la limite de quantification (LOQ) ont été déterminées selon la formule suivante LOD = 3.3×SDa/b, et LOQ = 10 ×SDa/b, SDa est l’écart-type de l’ordonnée à l’origine; b est la pente selon les directives de l’ICH. La LOD et la LOQ étaient respectivement de 0,667 et 2,020 µg/mL (tableau 1).
|
Paramètre |
Valeur |
|
Longueur d’onde de mesure (nm) |
|
|
Plage linéaire (µg/mL) |
|
|
Équation de régression |
y = 0,033x-0.009 |
|
Intercept |
|
|
Standard deviation of intercept |
|
|
Slope |
|
|
Standard deviation of slope |
|
|
Correlation coefficient (r2) |
|
|
Limit of detection, LOD (μg/mL) |
|
|
Limit of quant., LOQ (μg/mL) |
Table 1: Parameters for the performance of the proposed method.
Précision
La précision de la méthode proposée a été réalisée en appliquant 3 concentrations différentes de 10, 20 et 30 µg / mL de médicament thiamine dans une plage linéaire calculée comme le pourcentage de médicament récupéré dans les échantillons (tableau 2).
|
Sample No |
Sample Content (µg/mL) |
Thiamine Standard Amount (µg/mL) |
Amount Found (Total) (µg/ml) |
Recovery + SD* |
|
96.29+0.015 |
||||
|
98.90+0.018 |
||||
|
101.47+0.148 |
Table 2: Études de récupération pour la détermination de la thiamine par la méthode proposée.
* Les valeurs sont la moyenne de trois déterminations.
L’erreur relative (RE) se situait à 0,24 % et l’écart type correspondant à 0,004 pour trois déterminations différentes (tableau 3).
|
Sample No |
Concentration (μg/mL) |
Concentration |
Recovery (% + SD) |
Relative Error (%) |
|
95.5±0.004 |
||||
|
96.46±0.002 |
||||
|
97,50±0,003 |
Tableau 3: Évaluation de la précision et de la précision.
Robustesse
Mécanisme réactionnel: Il a été rapporté que le NBD-Cl réagit avec un groupe amino de dérivés d’amines primaires ou secondaires. De même, le groupe amino de la thiamine peut agir comme un nucléophile en raison de la seule paire d’électrons sur l’atome d’azote, ayant tendance à attaquer le centre déficient en électrons dans NBD–Cl (Tableau 4 & Figure 6). Dans le même temps, il a été prouvé que la composition du produit est 1:1 de thiamine et de NBD-Cl (Figure 7). On en conclut donc que le groupe amino de la thiamine réagit avec le NBD-Cl pour former un adduit brun. L’équation de réaction est illustrée à la figure 7.

Figure 6: The Job’s method plot for the stoichiometry of the reaction of Thiamine with NBD-Cl Vr: Volume of NBD-Cl (7.5×10-4 mol/L), Vt: Volume of Thiamine (7.5×10-4 mol/L), Vr + Vt=10 ml.
|
Parameter |
Recovery (% ± SD) |
|
Recommended condition |
97.50±0.003 |
|
NBD-Cl concentration (0.22%) |
98.75±0.002 |
|
NBD-Cl concentration (0.180%) |
96.76%±0,003 |
|
PH du tampon (10,7) |
96,90 ±0,002 |
|
PH du tampon (10,3) |
95,79 ±0,22 |
|
Temps de réaction min (23) |
96,09±0,009 |
|
Temps de réaction min (27) |
98,01±0,003 |
Tableau 4: Influence de la faible variation de la condition de dosage sur la performance analytique de la méthode spectrophotométrique proposée pour la détermination de la thiamine à l’aide du réactif NBD-Cl.
Application de la méthode proposée à l’analyse de la forme posologique de la thiamine
Les comprimés de thiamine ont été soumis à l’analyse par la méthode proposée et l’allégation figurant sur l’étiquette concorde bien avec notre nouvelle méthode, comme le montre le tableau 5. La méthode proposée présente l’avantage d’être pratiquement exempte d’interférences des excipients.
|
Brand Name of Label Claim (Mg) |
Amount Found (Mg) |
(% Found ± SD)a |
|
Thiamine tablets (100 mg) |
99.9±0.025 |
Table 5: Analysis of Thiamine-containing dosage form by the proposed method.
a: values are mean of five determinations.
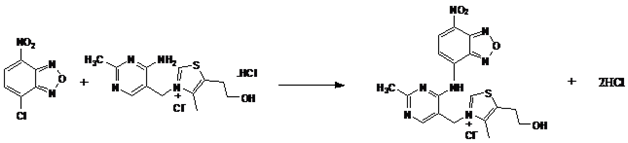
Figure 7: Réaction de la thiamine avec le NBD-Cl montrant une stoechiométrie 1:1.
Leave a Reply