Manejo de Extravasaciones de Quimioterapia
US Pharm. 2009; 34 (9) (suppl Oncológico): 3-11.
RESUMEN: Los medicamentos quimioterapéuticos intravenosos (IV) tienen el potencial de causar lesiones por extravasación o necrosis tisular en el sitio de administración. Aunque la mayoría de las extravasaciones se pueden prevenir con una administración de infusión adecuada y completa, se han reconocido y estudiado varios antídotos para prevenir lesiones tisulares adicionales.
La infiltración y la extravasación son dos complicaciones bien conocidas y distintas de la terapia de infusión intravenosa. De acuerdo con la Infusion Nurses Society y la Oncology Nursing Society, ambas complicaciones involucran la fuga inadvertida de una solución IV en el tejido circundante; sin embargo, el tipo de solución difiere. La infiltración es la administración inadvertida de una solución o medicamento no tóxico o irritante en los tejidos circundantes.1,2 Los agentes no tóxicos son agentes que rara vez producen reacciones agudas o destruyen el tejido cuando se infiltran. Los agentes irritantes pueden inducir dolor en el lugar de la inyección o a lo largo de la vena, con o sin una reacción inflamatoria, generalmente sin daño tisular persistente. Sin embargo, los irritantes pueden causar úlceras en los tejidos blandos solo si se extravasa inadvertidamente una gran cantidad de solución de fármaco concentrada para inducir reacciones inflamatorias sin daño tisular persistente.3,4
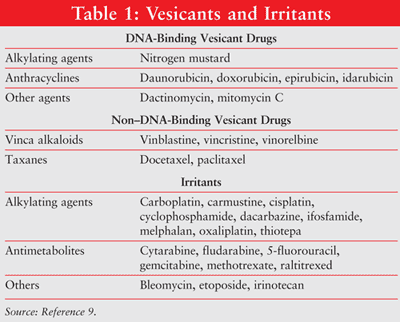
La extravasación se refiere a la instilación o fuga involuntaria de material vesicante en los espacios perivascular y subcutáneo durante la administración de medicamentos.1,2 La extravasación produce reacciones locales que van desde irritación local hasta necrosis tisular grave de la piel, vasculatura circundante y estructuras de soporte.5-8 Los agentes quimioterapéuticos se pueden clasificar, en función de su potencial para causar lesiones tisulares locales, como vesicantes, irritantes o no vesicantes. (En la TABLA 1.9 se describen varios vesicantes e irritantes) La extravasación accidental de fármacos intravenosos ocurre en aproximadamente el 0,1% al 6% de las perfusiones intravenosas periféricas y del 0,3% al 4,7% de las perfusiones de puertos de acceso venoso implantados.10-12
Fisiopatología del daño tisular
La extensión del daño tisular depende de la capacidad de unión del agente quimioterapéutico al ADN. Los agentes fijadores de ADN incluyen antraciclinas, antibióticos antitumorales, análogos de platino y algunos agentes alquilantes.3,4 Los antineoplásticos de unión al ADN causan daño tisular al propagar enlaces cruzados letales de ADN o roturas de hebras causadas por radicales libres, que conducen a la apoptosis celular.13-17 antineoplásticos que no se unen al ADN (p. ej., alcaloides de vinca, taxanos, inhibidores de la topoisomerasa) interfieren con la mitosis. Los agentes que no se unen al ADN se eliminan más fácilmente de los sitios de extravasación y causan menos daño tisular que los agentes que se unen al ADN.17
Los factores de riesgo de extravasación
Los riesgos de extravasación son multifactoriales y se pueden modificar en gran medida. Muchos de estos riesgos se derivan de errores en el uso y la colocación del dispositivo. Los factores del dispositivo intravenoso que afectan el riesgo de extravasación incluyen el material de la aguja (es decir, metal), el tamaño de la cánula (plástico grande frente a plástico pequeño) y el tipo de catéter (es decir, catéter venoso central). Las agujas de metal pueden causar más daño al insertarlas y son inflexibles dentro del vaso, mientras que las agujas de gran calibre pueden impedir el flujo sanguíneo, ralentizando la dilución del infusado.18,19 La extravasación del CVC puede ocurrir con desplazamiento de la aguja desde un puerto de acceso venoso implantado (IVAP), oclusión mecánica y daño posterior del CVC, migración del catéter o formación de manguitos de fibrina y trombosis. La colocación incorrecta de la IVAP es más probable que ocurra en pacientes con dispositivos nuevos, aquellos con hinchazón posoperatoria significativa y pacientes obesos o mujeres de pecho grande.20 Las oclusiones mecánicas pueden deberse a la formación de trombo, al precipitado del fármaco, al desplazamiento retrógrado del catéter o a un pinchazo (es decir, a una oclusión intermitente y posicional del catéter; se debe sospechar si la oclusión de la infusión se puede aliviar haciendo que el paciente mueva la posición del brazo).2,21,22 Evitar la extravasación depende en gran medida del mantenimiento adecuado del lugar de la vía intravenosa y de la garantía de que se está implantando la velocidad de perfusión correcta. Estos factores de riesgo están relacionados con los antineoplásticos utilizados, los pacientes y el médico que administra el medicamento.
Prevención
La estrecha vigilancia de los pacientes y la educación de los pacientes y los profesionales sobre los riesgos y el manejo de la extravasación vesicante parecen ser las piedras angulares de la prevención. Si bien los médicos tienen la responsabilidad de escribir órdenes precisas, las enfermeras son responsables de garantizar la colocación adecuada y calificada de los dispositivos y el monitoreo de las infusiones de quimioterapia visualmente y a través de entrevistas con los pacientes. Durante la administración de vesicantes, se debe vigilar el lugar en busca de hinchazón, enrojecimiento y dolor. Los vesicantes deben administrarse de acuerdo con las recomendaciones del fabricante (por ejemplo, dilución adecuada, tiempo de administración especificado). Se deben enjuagar las vías intravenosas antes y después de la administración de quimioterapia. El papel del farmacéutico sería ayudar a desarrollar políticas que garanticen la verificación, el etiquetado y la dispensación adecuados de los agentes quimioterapéuticos. Una forma en que esto podría ejecutarse es usar un etiquetado discriminativo al dispensar antineoplásticos vesicantes para que las enfermeras usen las medidas de precaución adecuadas. Los farmacéuticos pueden desempeñar un papel integral en la educación al proporcionar información sobre medicamentos y servicios de rutina a todos los miembros del equipo de atención médica sobre el uso y la administración adecuados de los diversos agentes quimioterapéuticos. Debe adoptarse un enfoque de colaboración multidisciplinario para garantizar la aplicación de prácticas seguras. La administración de quimioterapia en pacientes requiere la capacitación adecuada del personal y la educación de los pacientes, así como apoyo administrativo a través de la implementación de políticas.2,23
Documentación de los acontecimientos
Cada incidente de extravasación debe documentarse y notificarse exhaustivamente. La documentación sirve para varios propósitos, que incluyen proporcionar un relato preciso de lo que sucedió, proteger a los profesionales de la salud involucrados, recopilar información sobre extravasaciones y resaltar los déficits en la práctica.23 La documentación y la notificación a las entidades apropiadas de reacciones adversas a medicamentos y errores de medicación es otra forma en que los farmacéuticos pueden ayudar a prevenir eventos futuros. Los datos recopilados a partir de las reacciones adversas a los medicamentos notificadas y los errores de medicación podrían utilizarse como herramientas de aprendizaje para examinar sistemáticamente los medios por los que ocurren estos eventos. Los procedimientos y protocolos locales son primordiales para el reconocimiento y el manejo oportunos de la extravasación y la prevención de daños tisulares graves. Se deben realizar esfuerzos de colaboración para garantizar intentos multidisciplinarios oportunos de educar a todos los miembros del equipo de atención de la salud involucrados en el manejo de estos pacientes una vez que el evento haya ocurrido. Se deben realizar esfuerzos adicionales para poner en marcha políticas que impidan nuevos acontecimientos. Si existen políticas, éstas deberían ponerse a disposición de los interesados y actualizarse periódicamente para reflejar las prácticas actuales. Las directrices de extravasación de la Sociedad Europea de Enfermería Oncológica (EONS) de 2007 proporcionan datos y plantillas sugeridos que pueden utilizarse para recopilar información en caso de un caso.23
Los signos y síntomas de extravasación
Los signos y síntomas de extravasación vesicante incluyen hinchazón, enrojecimiento y / o molestias que a menudo se describen como ardor o escozor. La resistencia durante la administración del medicamento, una infusión lenta o lenta y la falta o pérdida de retorno de sangre de la cánula INTRAVENOSA, el puerto implantado u otro dispositivo de acceso venoso central pueden ser indicadores de que se está produciendo una extravasación vesicante.23 La decoloración y la induración de la piel pueden progresar aún más con el desarrollo de ampollas o necrosis y posiblemente ulceración y lesión de tejido profundo. Puede tardar varios días en darse cuenta de toda la extensión del daño epitelial.
Tratamiento de la extravasación inducida por quimioterapia
Las modalidades de tratamiento utilizadas para el manejo de la extravasación vesicante incluyen la interrupción inmediata de la quimioterapia y el enfriamiento o dilución del sitio de la extravasación. Para reducir la morbilidad asociada con la extravasación, es vital que los médicos estén bien informados de los tratamientos disponibles y trabajen rápidamente para evitar más daños al paciente. El tratamiento de la extravasación no tóxica por lo general incluye la elevación de la extremidad y el enfriamiento, y por lo general no incluye el uso de terapia farmacológica.23
Manejo inicial de la Extravasación Vesicante
La facilidad para proporcionar una intervención temprana puede facilitarse poniendo a disposición de la institución un kit de extravasación. La mayoría de los kits de extravasación contienen jeringas y cánulas desechables, compresas frías y calientes, gasas, yeso adhesivo, guantes estériles y protectores, y medicamentos para tratar la extravasación (por ejemplo, hialuronidasa, sulfóxido de dimetilo al 99%, dexrazoxano). Se debe colocar una lista del contenido del kit dentro del kit y un farmacéutico debe mantener regularmente la verificación regular del contenido del medicamento con fechas de caducidad actualizadas.2
Una vez que se produce la extravasación del vesicante, el médico debe interrumpir inmediatamente la perfusión; sin embargo, la cánula o la aguja de puerto sin cierre debe mantenerse en su lugar e intentar aspirar el vesicante con una jeringa de 10 ml. Se debe marcar y fotografiar el área de extravasación; a continuación, se debe retirar la cánula o aguja y se debe notificar al médico. Los pacientes pueden requerir el uso de analgésicos para ayudar a controlar el dolor que pueden experimentar. Una vez que se han tomado las medidas iniciales, es muy importante documentar a fondo la reacción adversa al medicamento y/o el error de medicación que se ha producido.23
Para alcaloides de vinca, donde esté indicada la dispersión o dilución del vesicante, aplicar calor local durante 20 minutos 4 veces al día durante 1 durante 2 días. Para otras extravasaciones vesicantes, incluidas las antraciclinas, el tratamiento inicial está orientado a localizar y neutralizar el agente extravasante con compresas frías durante 20 minutos, 4 veces al día durante 1 a 2 días, limitando la absorción celular de estos agentes.23
Tratamiento farmacológico
DMSO: El DMSO es un disolvente común que penetra en los tejidos y mejora la permeabilidad de la piel, lo que puede facilitar la absorción de un medicamento extravasado. Cuando se aplica tópicamente, tiene propiedades de eliminación de radicales libres / antioxidantes que pueden acelerar la eliminación del medicamento extravasado. DMSO (Rimso-50) solo está disponible para la compra minorista en los Estados Unidos en una solución al 50% (vol/vol) en agua. Esta solución está aprobada por la FDA solo para el tratamiento de la cistitis intersticial recurrente.La eficacia de la DMSO para el tratamiento de la extravasación quimioterapéutica se describió por primera vez en varios informes de casos y en pequeños estudios clínicos.
En un caso, se trató una extravasación de daunorrubicina de 10 mg en un varón de 42 años de edad con bicarbonato de sodio, dexametasona (4 mg), compresas de hielo y 1,5 ml de DMSO tópico al 70%, que se aplicó cada 3 a 4 horas durante 10 días. Este régimen proporcionó alivio del dolor y prevención de úlceras.25
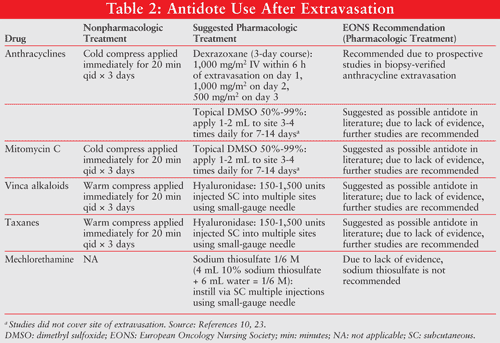
Olver y Schwarz notificaron tres casos de resolución de extravasación con el uso de DMSO.26 En un caso, la aplicación diaria de DMSO 99% durante 14 días dio lugar a la resolución completa del dolor en 2 días sin ulceración en un paciente con extravasación de doxorrubicina. El paciente también recibió bicarbonato de sodio 8,4% y el tratamiento no farmacológico adecuado. (Ver TABLA 2 para opciones no farmacológicas.) En otro caso, un hombre de 49 años que recibió de 4 a 6 mg de doxorrubicina fue tratado por extravasación de doxorrubicina con 5 ml de 8.bicarbonato de sodio al 4%, bolsas de hielo y DMSO al 99% aplicados diariamente durante 14 días. No se produjo ulceración; sin embargo, se produjo una extensión de codo limitante de área indurada de 3 x 2,5 cm.26 En un tercer caso, una aplicación tópica de DMSO al 99% (cada 6 horas durante 1 semana y luego dos veces al día durante otra semana) previno la ulceración; sin embargo, la pigmentación residual permaneció.26
Berghammer et al también reportaron un caso de extravasación de docetaxel.El extravasato se diluyó con solución salina normal (0,9%) y se trató con compresas de hielo. Se aplicó DMSO 3 veces cada 45 minutos, y se administraron corticosteroides orales y diclofenaco el día de la extravasación. Todos los síntomas se resolvieron en 24 horas; sin embargo, los síntomas retardados (decoloración marrón, hiperplasia de la piel) aparecieron el día 5 y aumentaron a partir de entonces. No fue necesaria ninguna intervención quirúrgica plástica. Aunque la DMSO en combinación con hipotermia y solución salina isotónica no fue eficaz para prevenir los síntomas retardados, sí restringió la inflamación y la necrosis tisular.
Ludwig et al informaron que el uso de una mezcla de DMSO al 90% y alfa-tocoferol al 10% dentro de las 48 horas posteriores a la extravasación de antraciclinas o mitomicina C en 8 pacientes no produjo ulceración de la piel ni deterioro funcional o neurovascular.28 Desafortunadamente, el alfa-tocoferol no es un medicamento fácilmente disponible y se deben realizar más ensayos aleatorizados para validar su uso.
En un estudio prospectivo de 20 pacientes con extravasaciones de antraciclinas, se administró DMSO 99% dos veces, 6 veces al día durante 2 semanas.29 No se describieron úlceras después del tratamiento con DMSO, aunque se evidenciaron hinchazón inicial (85%), eritema (75%) y dolor (60%). Después de un periodo de seguimiento de 3 meses en 16 pacientes, 6 (38%) pacientes no presentaron síntomas aparentes y 10 (63%) presentaron induraciones pigmentadas. Bertelli también llevó a cabo un estudio prospectivo para evaluar los efectos de la DMSO en las extravasaciones de antraciclinas.30 La doxorrubicina representó 11 casos y la epirrubicina representó 46 casos. Los pacientes fueron tratados con DMSO 99% cada 8 horas durante 7 días. El setenta por ciento de los pacientes (40/57) tuvieron resolución completa de la extravasación en 1 semana, un paciente tuvo induración residual de tejidos blandos y un paciente tuvo hiperpigmentación residual.
En estos informes de casos y estudios pequeños, las extravasaciones se diagnosticaron clínicamente y no mediante biopsia. DMSO puede ser una opción para el tratamiento de antraciclinas extravasadas, mitomicina C y actinomicina D. Se recomienda aplicar una capa delgada de DMSO en el área extravasada y dejar que se seque. Se debe aplicar un apósito no oclusivo dentro de 10 a 25 minutos. Estos pasos deben repetirse cada 8 horas durante 7 días.23 Aunque el DMSO se ha utilizado en la práctica como una opción de tratamiento, la falta de ensayos prospectivos puede limitar su uso. Las directrices de extravasación de EONS 2007 recomiendan que se realicen más estudios; sin embargo, se puede considerar el uso de DMSO del 50 al 99% a discreción del médico.23 Es importante señalar que ninguno de los estudios prospectivos de DMSO utilizó un vendaje para permitir que la piel absorba completamente el DMSO.
Hialuronidasa: Se cree que la hialuronidasa es capaz de descomponer la matriz extracelular que subyace a las células epiteliales. La matriz se aferra a grandes cantidades de moléculas de agua, y al descomponerse, es capaz de liberar el fluido en el medio extracelular. En el caso de una extravasación, permite aumentar el líquido en el sitio, diluyendo así la concentración real de la piel en el sitio de contacto.31,32 La hialuronidasa se ha utilizado para el tratamiento de extravasaciones de alcaloides de vinca y taxanos.Se han utilizado 33 Dosis de hialuronidasa de 150 a 1.500 unidades diluidas en 1 ml de solución salina normal subcutánea o intradérmica en el plazo de 1 hora tras la extravasación.
En un pequeño estudio clínico de 6 pacientes con extravasación de vinblastina (n = 1), vincristina (n = 1) y vinorelbina (n = 4), se inyectaron 250 unidades de hialuronidasa en el catéter permanente o por vía subcutánea (6 inyecciones) en caso de lesión. No se aplicaron esteroides ni compresas frías. El dolor se resolvió a los pocos días del tratamiento con hialuronidasa en todos los pacientes. Un paciente se quejó de una induración ligeramente dolorosa 3 meses después de la extravasación de vincristina.30 Estos informes revelan información prometedora; sin embargo, todavía hay una falta general de evidencia para el uso de hialuronidasa para el tratamiento de extravasaciones de alcaloides de vinca. Se deben realizar más ensayos prospectivos. Las guías de extravasación de EONS 2007 recomiendan que se realicen más estudios; sin embargo, la hialuronidasa puede considerarse como una opción a las dosis sugeridas a discreción del médico.23
Tiosulfato de Sodio: El tiosulfato de sodio previene la alquilación y la destrucción de tejidos al proporcionar un sustrato para la alquilación en el tejido subcutáneo. Se ha demostrado que el tiosulfato de sodio es eficaz en experimentos con animales y en un informe de caso para el tratamiento de la extravasación de mecloretamina (mostaza nitrogenada).33,34 La dosis recomendada es de 2 mL de 0,17 M (una solución de 4 ml de tiosulfato de sodio al 10% y 6 ml de agua estéril para preparaciones inyectables). Debido a la falta de evidencia, las guías de extravasación de EONS 2007 no recomiendan esto como antídoto.22
Dexrazoxano: El dexrazoxano (Totect) fue aprobado recientemente por la FDA para el tratamiento de extravasaciones inducidas por antraciclinas. El dexrazoxano tiene un doble mecanismo de acción: 1) actúa como quelante del hierro, previniendo la formación de complejos de hierro-antraciclina y radicales hidroxilo mediados por el hierro que causan daño oxidativo; y 2) estabiliza la topoisomerasa II y la hace inaccesible a la quimioterapia con antraciclinas. El dexrazoxano bloquea la enzima para que ya no se vea afectada por la antraciclina y previene el daño a las células sanas del tejido.La eficacia del dexrazoxano se demostró en dos ensayos clínicos realizados en Europa.36 Ambos ensayos fueron ensayos clínicos prospectivos, abiertos, de un solo brazo y multicéntricos, realizados entre julio de 2001 y agosto de 2005, con un total de 80 pacientes incluidos. En el primer estudio se incluyeron pacientes de 17 sitios de cáncer en Dinamarca, y en el segundo se incluyeron pacientes de 34 sitios de cáncer en Dinamarca, Alemania, Italia y los Países Bajos. La extravasación de antraciclinas se diagnosticó y confirmó mediante microscopía de fluorescencia de tejido biopsiado tomado dentro de las 6 horas posteriores al dexrazoxano. Se requirió un tamaño de muestra de 32 pacientes evaluables para mostrar una reducción del 70% o superior en la incidencia de cirugía (prueba binomial unilateral, a = .025, ß = .20). El criterio de valoración primario fue la tasa de resección quirúrgica y necrosis. Cincuenta y cuatro de los 80 pacientes (estudio 1: n = 18; estudio 2: n = 36) fueron evaluables (n = 13 biopsias negativas; n = 4 no se realizaron biopsias; n = 8 violaciones del protocolo), con una edad media de 56 años (rango, 34-81 años). El sesenta y nueve por ciento (n = 37) de los pacientes evaluados eran mujeres. El dexrazoxano se administró en perfusión INTRAVENOSA durante 1 a 2 horas; 1.000 mg/m2 en 6 horas; 1.000 mg/m2 después de 24 horas; y 500 mg / m2 después de 48 horas de extravasación.Se evaluó la eficacia y seguridad de 36 pacientes
en los días 7, 14, 21 y 28, y la eficacia en el día 9036.El diagnóstico de cáncer más frecuente fue cáncer de mama (50%), seguido de linfoma (39%) y otros tipos de cáncer (9%). Los pacientes experimentaron extravasaciones de doxorrubicina (n = 23) o epirrubicina (n = 31). El área media de extravasación fue de 23,6 cm2 en el estudio 1 y de 39 cm2 en el estudio 2. Once pacientes tenían áreas de extravasación superiores a 75 cm2. No hubo incidencias de cirugía en el estudio 1 y en el incidente 1 (2,8%, IC 95% 0,1%-14,5%) en el estudio 2. El paciente que desarrolló necrosis tisular por extravasación tenía un área muy grande de extravasación de doxorrubicina de 253 cm2. Los síntomas aumentaron en los días posteriores a la extravasación, la necrosis tisular comenzó a ocurrir 9 días después de la extravasación del paciente y la necrosis se extirpó quirúrgicamente. En el estudio 1, hubo 1 (5,6%) incidente de necrosis por biopsia, 6 (33).3%) incidentes de aplazamiento o cancelación del tratamiento programado para el cáncer y 9 (50%) hospitalizaciones debido a la extravasación. En el estudio 2, hubo 1 (2,8%) incidente de necrosis por extravasación, 3 (8,3%) incidentes de necrosis por biopsia, 10 (27,8%) incidentes de aplazamiento o cancelación del tratamiento programado para el cáncer por extravasación y 13 (36,1%) incidentes de hospitalización por extravasación. A los 3 meses de seguimiento, el 88,9% (n = 16) no tuvo secuelas negativas en el estudio 1 y el 63,9% (n = 23) en el estudio 2. Quince de los 80 pacientes experimentaron trastornos sensoriales (n = 9), atrofia de la piel (n = 5), dolor (n = 10), desfiguración (n = 1) y limitación (n = 3). La mayoría de los pacientes (71%) pudieron recibir más tratamiento de quimioterapia a tiempo.
Los efectos adversos más frecuentes incluyeron disminución del recuento de glóbulos blancos (72,5%), disminución de la hemoglobina (42,5%), disminución del recuento de plaquetas (26%), aumento de la aspartato aminotransferasa (36,8%), aumento de la alanina aminotransferasa (23,9%), reacción en el lugar de inyección (27,5%) y náuseas (18,8%).36 Los resultados de los ensayos clínicos revelaron que el dexrazoxano es un agente eficaz para el tratamiento de extravasaciones agudas de antraciclinas y la prevención de síntomas retardados.
En la TABLA 2 se presenta un resumen de estas recomendaciones de tratamiento, incluidas las directrices EONS 2007.
Función del farmacéutico
Los farmacéuticos deben participar estrechamente en la evaluación y el tratamiento de todas las extravasaciones inducidas por quimioterapia. Pueden desempeñar un papel integral de varias maneras, incluyendo: 1) desarrollo de políticas y protocolos; 2) educación multidisciplinaria, familiar y del paciente; 3) documentación y notificación de extravasaciones y otras reacciones adversas a medicamentos posteriores a la terapia; y 4) monitoreo de la dosificación, administración y eficacia adecuadas del tratamiento.
Conclusión
Todos los estudios revisados involucraron adultos, ya que los pacientes pediátricos habrían tenido un mayor riesgo de agitación y tirones de las líneas. Hasta la fecha, el dexrazoxano es el único agente de extravasación que se ha estudiado en ensayos prospectivos multicéntricos grandes que utilizaron pruebas objetivas y confiables para diagnosticar casos de extravasación; esto proporciona pruebas sólidas de la utilidad del dexrazoxano. A pesar de sus usos comunes en la práctica, otros tratamientos farmacológicos, como la DMSO y la hialuronidasa, no se han estudiado ampliamente; por lo tanto, faltan recomendaciones basadas en la evidencia. El tratamiento de la extravasación debe llevarse a cabo a discreción del médico en colaboración con todos los miembros del equipo de atención médica.
1. Sociedad de Enfermeras de Infusión. Estándares de práctica de enfermería de infusión. J Infus Nurs. 2006; 29 (suppl 1): S1-S92.
2. Polovich M, White J, Kelleher L. Pautas y recomendaciones para la práctica de Quimioterapia y Bioterapia. 2nd ed. Pittsburgh, PA: Sociedad de Enfermería Oncológica; 2005.
3. Ener RA, Meglathery SB, Styler M. Extravasación de terapias hemato-oncológicas sistémicas. Ann Oncol. 2004;15:858-862.
4. Sauerland C, Egelking C, Wickman R, Corbi D. Extravasación vesicante parte I: mecanismos, patogénesis y cuidados de enfermería para reducir el riesgo. Foro de Oncol Nurs. 2006;33:1134-1141.
5. Cassagnol M, Cohen H. Dermatologic toxicities of chemotherapeutic agents. US Pharm. 2008;33(1)(Oncology suppl):10-20.
6. Schulmeister L. Extravasation management. Semin Oncol Nurs. 2007;23:184-190.
7. Viale P. Chemotherapy and cutaneous toxicities: implications for oncology nurses. Semin Oncol Nurs. 2006;22:144-151.
8. Cox K, Stuart-Harris R, Abdini G, et al. The management of cytotoxic-drug extravasation: guide-lines drawn up by a working party for the Clinical Oncological Society of Australia. Med J Aust. 1988;148:185-189.
9. Schrijvers DL. Extravasation: una temida complicación de la quimioterapia. Ann Oncol. 2003; 14 (suplemento 3): iii26-iii30.
10. El Servicio Nacional de Información sobre Extravasaciones. www.extravasation.org.uk/home.html Consultado el 25 de marzo de 2009.
11. Lemmers N, Gels M, Sleijfer D, et al. Complicaciones de los puertos de acceso venoso en 132 pacientes con cáncer de testículo diseminado tratados con policemoterapia. J Clin Oncol. 1996;14:2916-2922.12. Shetty PC, Mody MK, Kastan DJ. Resultado de 350 puertos torácicos implantados colocados por radiólogos intervencionistas. J Vasc Radiol Interv. 1997;8:991-995.13. Dorr RT. Antídotos para extravasaciones de quimioterapia vesicante. Blood Rev. 1990; 4: 41-60.14. Langer SW, Sehested M, Jensen PB. Tratamiento de la extravasación de antraciclinas con dexrazoxano. Clin Cancer Res. 2000; 6: 3680-3686.15. Raymond E, Faivre S, Woynarowski JM, Chaney SG. Oxaliplatino: mecanismo de acción y actividad antineoplásica. Semin Oncol. 1998; 2 (suppl 5): 4-12.16. Rivory LP. Nuevos fármacos para el cáncer colorrectal-mecanismos de acción. Aust Prescr. 2002;25:108-110. www.australianprescriber.com/magazine/25/5/108/10/. Consultado el 25 de marzo de 2009.17. Skeel RT. Manual de Quimioterapia para el Cáncer. 5th ed. New York, NY: Lippincott Williams & Wilkins; 1999.18. Boyle DM, Engelking C. Extravasación vesicante: mitos y realidades. Foro de Oncol Nurs. 1995;22:57-67.19. Hadaway LC. Prevención y gestión de la extravasación periférica. Enfermería. 2004;34:66-67.20. Shulmeister L, Camp-Sorrell D. Extravasación de quimioterapia de puertos implantados. Foro de Oncol Nurs. 2000;27:531-538.21. Debets JM, Wils JA, Schlangen JT. Una complicación poco frecuente de los dispositivos de acceso venoso central implantados: fractura de catéter y embolización. Atención de Apoyo para el Cáncer. 1995;3:432-434.22. Gorski LA. Oclusiones del dispositivo de acceso venoso central. Parte 2: Causas no trombóticas y tratamiento. Enfermera de Salud en el Hogar. 2003;21:168-171.23. Directrices de extravasación 2007. Sociedad Europea de Enfermería Oncológica. www.cancerworld.org/CancerWorld/getStaticModFile.aspx?id=2340 Consultado el 25 de marzo de 2009.24. Prospecto de Rimso-50 (sulfóxido de dimetilo). Lake Forest, IL: Bioniche Pharma USA LLC; 2009.25. Lawrence HJ, Buenas noches SH. Daño tisular limitante del sulfóxido de dimetilo causado por extravasación de agentes de doxorrubicina. Ann Intern Med. 1983;98:1025.26. Olvídalo, Schwarz MA. Use of dimethyl sulfoxide in limiting tissue damage caused by extravasation of doxorubicin . Cancer Treat Rep. 1983;67:407-408.
27. Berghammer P, Pohnl R, Baur M, Dittrich C. Docetaxel extravasation. Support Care Cancer. 2001;9:131-134.
28. Ludwig CU, Stoll HR, Obrist R, Obrecht JP. Prevention of cytotoxic drug-induced skin ulcers with dimethyl sulfoxide (DMSO) and alpha-tocopherole. Eur J Cancer Clin Oncol. 1987;23:327-329.
29. Olver IN, Aisner J, Hament A, et al. A prospective study of topical dimethyl sulfoxide for treating anthracycline extravasation. J Clin Oncol.1988;6:1732-1735.
30. Bertelli G. Prevention and management of extravasation of cytotoxic drugs. Drug Saf. 1995;12:245-255.
31. Balazs EA, Laurent TC, Jeanloz RW. Nomenclature of hyaluronic acid. Biochem J. 1986;235:903.
32. Girish KS, Kemparaju K. The magic glue hyaluronan and its eraser hyaluronidase. Life Sci. 2007;80:1921-1943.
33. Dorr T. Antidotes to vesicant chemotherapy extravasations. Blood Rev. 1990;4:41-60.
34. Owen OE, Dellatorre DL, Van Scott EJ, Cohen MR. Accidental intramuscular injection of mechlorethamine. Cancer. 1980;45:2225-2226.
35. Totect (dexrazoxane for injection) package insert. Copenhagen, Denmark: TopoTarget A/S; October 2007.
36. Mouridsen HT, Langer SW, Buter J, et al. Treatment of anthracycline extravasation with Savene (dexrazoxane). Results from two prospective clinical multicenter studies. Ann Oncol. 2007;18:546-550.
Leave a Reply