Management von Chemotherapie-Extravasationen
US Pharm. 2009;34(9)(Onkologie suppl): 3-11. ZUSAMMENFASSUNG: Intravenöse (IV) chemotherapeutische Medikamente haben das Potenzial, eine Extravasationsverletzung oder Gewebenekrose am Verabreichungsort zu verursachen. Obwohl die meisten Extravasationen durch eine ordnungsgemäße und gründliche Infusionsverabreichung verhindert werden können, wurden mehrere Gegenmittel erkannt und untersucht, um weitere Gewebeverletzungen zu verhindern. Infiltration und Extravasation sind zwei bekannte, unterschiedliche Komplikationen der IV-Infusionstherapie. Laut der Infusion Nurses Society und der Oncology Nursing Society beinhalten beide Komplikationen das unbeabsichtigte Austreten einer IV-Lösung in das umgebende Gewebe; Die Art der Lösung unterscheidet sich jedoch. Infiltration ist die unbeabsichtigte Verabreichung einer nichtvesizierenden oder reizenden Lösung oder eines Medikaments in das umgebende Gewebe.1,2 Nonvesicants sind Mittel, die selten akute Reaktionen hervorrufen oder das Gewebe zerstören, wenn sie infiltrieren. Reizstoffe können Schmerzen an der Injektionsstelle oder entlang der Vene hervorrufen, mit oder ohne Entzündungsreaktion, in der Regel ohne anhaltende Gewebeschädigung. Reizstoffe können jedoch nur dann Weichteilgeschwüre verursachen, wenn eine große Menge konzentrierter Arzneimittellösung versehentlich extravasiert wird, um Entzündungsreaktionen ohne anhaltende Gewebeschädigung auszulösen.3,4
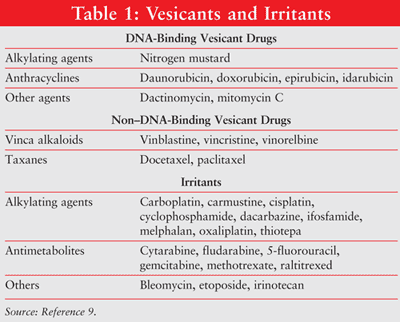
Extravasation bezieht sich auf das unbeabsichtigte Einträufeln oder Austreten von Vesikelmaterial in den perivaskulären und subkutanen Raum während der Verabreichung von Medikamenten.1,2 Die Extravasation führt zu lokalen Reaktionen, die von lokaler Reizung bis zu schwerer Gewebenekrose der Haut, des umgebenden Gefäßsystems und der Stützstrukturen reichen.5-8 Chemotherapeutika können aufgrund ihres Potenzials, lokale Gewebeverletzungen zu verursachen, als Vesikel, Reizstoffe oder Nichtvesikel eingestuft werden. (Mehrere Vesikel und Reizstoffe sind in TABELLE 1.9 aufgeführt) Die versehentliche Extravasation von IV-Arzneimitteln tritt bei etwa 0,1% bis 6% der peripheren IV-Infusionen und 0,3% bis 4,7% der implantierten venösen Zugangsportinfusionen auf.10-12
Pathophysiologie der Gewebeschädigung
Das Ausmaß der Gewebeschädigung hängt von der Bindungskapazität des Chemotherapeutikums an die DNA ab. DNA-Bindemittel umfassen Anthracycline, Antitumorantibiotika, Platinanaloga und einige Alkylierungsmittel.3,4 DNA-bindende Antineoplastika verursachen Gewebeschäden durch Vermehrung tödlicher DNA-Querverbindungen oder Strangbrüche durch freie Radikale, die zur Zellapoptose führen.13-17 Nicht-DNA-bindende Antineoplastika (z.B., Vinca-Alkaloide, Taxane, Topoisomerase-Inhibitoren) stören die Mitose. Nicht-DNA-Bindemittel werden leichter von Extravasationsstellen entfernt und verursachen weniger Gewebeschäden als DNA–Bindemittel.17
Risikofaktoren für Extravasation
Risiken für Extravasation sind multifaktoriell und sind weitgehend modifizierbar. Viele dieser Risiken sind auf Fehler bei der Verwendung und Platzierung von Geräten zurückzuführen. IV-Gerät Faktoren, die das Extravasationsrisiko beeinflussen, umfassen Nadelmaterial (d. H. Metall), Kanülengröße (großer Kunststoff vs. kleiner Kunststoff) und Kathetertyp (d. H. Zentralvenenkatheter). Metallnadeln können beim Einführen mehr Schaden anrichten und sind im Gefäß unflexibel, während Nadeln mit großem Messgerät den Blutfluss behindern und die Verdünnung des Infusats verlangsamen können.18,19 Extravasation von CVCs kann mit Nadelverschiebung von einem implantierten venösen Zugangsport (IVAP), mechanischer Okklusion und anschließender CVC-Schädigung, Kathetermigration oder Fibrinhülsenbildung und Thrombose auftreten. Eine falsche Platzierung von IVAP tritt häufiger bei Patienten mit neuen Geräten, Patienten mit erheblicher postoperativer Schwellung und adipösen Patienten oder Frauen mit großen Brüsten auf.20 Mechanische Verschlüsse können auf Thrombusbildung, Arzneimittelniederschlag, retrograde Katheterverschiebung oder Abklemmen zurückzuführen sein (d. H. Auf einen intermittierenden und positionellen Katheterverschluss; Es sollte vermutet werden, ob der Infusionsverschluss dadurch gelindert werden kann, dass der Patient seine Armpositionierung bewegt).2,21,22 Die Vermeidung einer Extravasation hängt in hohem Maße von der ordnungsgemäßen Aufrechterhaltung der Infusionsstelle und der Gewährleistung der korrekten Infusionsrate ab. Diese Risikofaktoren hängen mit den verwendeten Antineoplastika, den Patienten und dem Kliniker zusammen, der das Medikament verabreicht.
Prävention
Eine engmaschige Überwachung der Patienten und die Aufklärung von Patienten und Ärzten über die Risiken und das Management der vesikulären Extravasation scheinen die Eckpfeiler der Prävention zu sein. Während Ärzte die Verantwortung tragen, genaue Anweisungen zu schreiben, sind Krankenschwestern dafür verantwortlich, die fachgerechte und ordnungsgemäße Platzierung von Geräten und die Überwachung von Chemotherapieinfusionen visuell und durch Patienteninterviews sicherzustellen. Während der Verabreichung von Vesicant sollte die Stelle auf Schwellung, Rötung und Schmerzen überwacht werden. Vesikel sollten gemäß den Empfehlungen des Herstellers verabreicht werden (z. B. richtige Verdünnung, angegebene Verabreichungszeit). IV-Linien sollten vor und nach der Chemotherapie gespült werden. Die Rolle des Apothekers wäre es, bei der Entwicklung von Richtlinien zu helfen, die die ordnungsgemäße Überprüfung, Kennzeichnung und Abgabe von Chemotherapeutika sicherstellen. Eine Möglichkeit, dies zu erreichen, besteht darin, bei der Abgabe von vesikulären Antineoplastika eine diskriminierende Kennzeichnung zu verwenden, damit Krankenschwestern die entsprechenden Vorsichtsmaßnahmen ergreifen. Apotheker können eine integrale Rolle bei der Aufklärung spielen, indem sie allen Mitgliedern des Gesundheitsteams Arzneimittelinformationen und Routinedienste über die ordnungsgemäße Verwendung und Verabreichung der verschiedenen Chemotherapeutika zur Verfügung stellen. Es muss ein multidisziplinärer, kollaborativer Ansatz verfolgt werden, um sicherzustellen, dass sichere Praktiken umgesetzt werden. Die Verabreichung von Chemotherapie bei Patienten erfordert die ordnungsgemäße Schulung des Personals und die Aufklärung der Patienten sowie die administrative Unterstützung durch die Umsetzung der Politik.2,23
Dokumentation von Ereignissen
Jeder Vorfall einer Extravasation muss gründlich dokumentiert und gemeldet werden. Die Dokumentation dient mehreren Zwecken, einschließlich der Bereitstellung einer genauen Darstellung des Geschehens, des Schutzes der beteiligten Angehörigen der Gesundheitsberufe, der Sammlung von Informationen über Extravasationen und der Hervorhebung von Defiziten in der Praxis.23 Die Dokumentation und Meldung von Nebenwirkungen und Medikationsfehlern an die zuständigen Stellen ist eine weitere Möglichkeit, wie Apotheker dazu beitragen können, zukünftige Ereignisse zu verhindern. Daten, die aus den gemeldeten Nebenwirkungen und Medikationsfehlern gesammelt wurden, könnten als Lerninstrumente verwendet werden, um systemisch zu untersuchen, mit welchen Mitteln diese Ereignisse auftreten. Lokale Verfahren und Protokolle sind für die rechtzeitige Erkennung und Behandlung von Extravasationen und die Prävention schwerwiegender Gewebeschäden von größter Bedeutung. Es sollten gemeinsame Anstrengungen unternommen werden, um sicherzustellen, dass zeitnah multidisziplinäre Versuche unternommen werden, alle Mitglieder des Gesundheitsteams, die an der Behandlung dieser Patienten beteiligt sind, nach Eintritt des Ereignisses zu schulen. Es sollten zusätzliche Anstrengungen unternommen werden, um Maßnahmen einzuleiten, die weitere Ereignisse verhindern würden. Wenn Richtlinien vorhanden sind, sollten sie leicht verfügbar gemacht und regelmäßig aktualisiert werden, um die aktuellen Praktiken widerzuspiegeln. Die European Oncology Nursing Society (EONS) 2007 Extravasation Guidelines bieten vorgeschlagene Daten und Vorlagen, die verwendet werden können, um Informationen im Falle eines Falles zu sammeln.23
Anzeichen und Symptome einer Extravasation
Anzeichen und Symptome einer vesikulären Extravasation umfassen Schwellungen, Rötungen und / oder Beschwerden, die häufig als Brennen oder Stechen beschrieben werden. Resistenzen während der Arzneimittelverabreichung, eine langsame oder träge Infusion und das Fehlen oder der Verlust von Blutrückfluss aus der IV-Kanüle, dem implantierten Port oder einer anderen zentralvenösen Zugangsvorrichtung können Indikatoren dafür sein, dass eine vesikuläre Extravasation auftritt.23 Die Verfärbungen und Verhärtungen der Haut können mit der Entwicklung von Blasen oder Nekrosen und möglicherweise Ulzerationen und tiefen Gewebeverletzungen weiter fortschreiten. Es kann mehrere Tage dauern, bis das volle Ausmaß der Epithelschädigung erreicht ist.
Behandlung der Chemotherapie-induzierten Extravasation
Zu den Behandlungsmodalitäten für die Behandlung der vesikulären Extravasation gehören das sofortige Absetzen der Chemotherapie und die Abkühlung oder Verdünnung der Extravasationsstelle. Um die mit der Extravasation verbundene Morbidität zu verringern, ist es wichtig, dass Kliniker über die verfügbaren Behandlungen gut informiert sind und schnell arbeiten, um weitere Patientenschäden zu vermeiden. Das Management der nichtvesikanten Extravasation umfasst typischerweise das Anheben der Extremität und das Abkühlen und schließt normalerweise nicht die Verwendung einer pharmakologischen Therapie ein.23
Anfängliches Management der vesikulären Extravasation
Eine einfache frühzeitige Intervention kann erleichtert werden, indem ein Extravasationsset innerhalb der Einrichtung zur Verfügung gestellt wird. Die meisten Extravasations-Kits enthalten Einwegspritzen und -kanülen, Kalt-Heiß-Packungen, Mullbinden, Heftpflaster, sterile und Schutzhandschuhe sowie Medikamente zur Behandlung der Extravasation (z. B. Hyaluronidase, Dimethylsulfoxid 99%, Dexrazoxan). Eine Liste des Inhalts des Kits sollte in das Kit aufgenommen werden, und eine regelmäßige Überprüfung des Arzneimittelinhalts mit aktualisierten Verfallsdaten sollte regelmäßig von einem Apotheker durchgeführt werden.2
Sobald eine Vesikelextravasation auftritt, sollte der Arzt die Infusion sofort abbrechen; Die Kanüle oder die Nadel mit dem nicht konischen Anschluss sollten jedoch an Ort und Stelle gehalten werden, und es sollte versucht werden, das Vesikel mit einer 10-ml-Spritze abzusaugen. Der Extravasationsbereich sollte markiert und fotografiert werden; dann sollte die Kanüle oder Nadel entfernt und der Arzt benachrichtigt werden. Patienten können die Verwendung von Analgetika benötigen, um die Schmerzen zu bewältigen, die sie erfahren können. Sobald erste Maßnahmen ergriffen wurden, ist es sehr wichtig, die aufgetretenen Nebenwirkungen und / oder Medikationsfehler gründlich zu dokumentieren.23
Bei Vinca-Alkaloiden, bei denen eine Verteilung oder Verdünnung des Vesikans angezeigt ist, 20 Minuten lang 4-mal täglich 1 für 2 Tage lokal erhitzen. Bei anderen vesikulären Extravasationen, einschließlich Anthracyclinen, ist die Erstbehandlung darauf ausgerichtet, das extravasierte Mittel 20 Minuten lang 4-mal täglich für 1 bis 2 Tage mit kalten Kompressen zu lokalisieren und zu neutralisieren, wodurch die zelluläre Aufnahme dieser Mittel begrenzt wird.23
Pharmakologische Behandlung
DMSO: DMSO ist ein übliches Lösungsmittel, das in Gewebe eindringt und die Hautpermeabilität erhöht, was die Absorption eines extravasierten Arzneimittels erleichtern kann. Bei topischer Anwendung hat es Radikalfänger / antioxidative Eigenschaften, die die Entfernung des extravasierten Arzneimittels beschleunigen können. DMSO (Dmso-50) ist in den USA nur in einer 50% igen (vol / vol) Lösung in Wasser erhältlich. Diese Lösung ist von der FDA nur zur Behandlung von rezidivierender interstitieller Zystitis zugelassen.24 Die Wirksamkeit von DMSO zur Behandlung der Chemotherapie-Extravasation wurde erstmals in mehreren Fallberichten und kleinen klinischen Studien beschrieben.
In einem Fall wurde eine 10-mg-Daunorubicin-Extravasation bei einem 42-jährigen Mann mit Natriumbicarbonat, Dexamethason (4 mg), Eisbeuteln und 1,5 ml topischem DMSO 70% behandelt, das 10 Tage lang alle 3 bis 4 Stunden angewendet wurde. Dieses Regime sorgte für Schmerzlinderung und Ulkusprävention.25
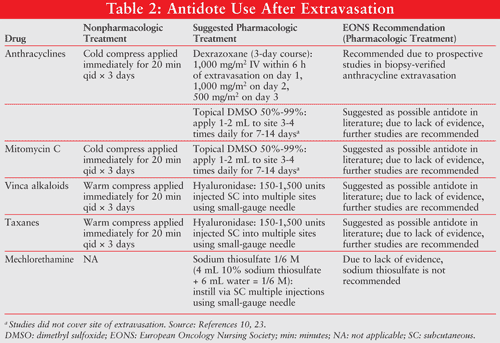
Olver und Schwarz berichteten über drei Fälle von Extravasationsauflösung bei DMSO-Anwendung.26 In einem Fall führte die tägliche Anwendung von DMSO 99% über 14 Tage zu einer vollständigen Schmerzlinderung innerhalb von 2 Tagen ohne Ulzeration bei einem Patienten mit Doxorubicin-Extravasation. Der Patient erhielt auch Natriumbicarbonat 8,4% und die entsprechende nicht-pharmakologische Behandlung. (Siehe TABELLE 2 für nicht-pharmazeutische Optionen.) In einem anderen Fall wurde ein 49-jähriger Mann, der 4 bis 6 mg Doxorubicin erhielt, zur Extravasation von Doxorubicin mit 5 ml 8 behandelt.4% Natriumbicarbonat, Eisbeutel und DMSO 99% täglich für 14 Tage angewendet. Ulzerationen traten nicht auf; Es trat jedoch ein 3 x 2,5 cm verhärteter Bereich auf, der die Ellenbogenstreckung einschränkte.26 In einem dritten Fall verhinderte eine topische Anwendung von DMSO 99% (alle 6 Stunden für 1 Woche, dann zweimal täglich für eine weitere Woche) Ulzerationen; Die Restpigmentierung blieb jedoch bestehen.26
Berghammer et al berichteten auch über einen Fall von Docetaxel-Extravasation.27 Das Extravasat wurde mit normaler (0,9%iger) Kochsalzlösung verdünnt und mit Eisbeuteln behandelt. DMSO wurde 3-mal alle 45 Minuten angewendet, und orale Kortikosteroide und Diclofenac wurden am Tag der Extravasation verabreicht. Alle Symptome klangen innerhalb von 24 Stunden ab; verzögerte Symptome (braune Verfärbung, Hauthyperplasie) traten jedoch am 5. Tag auf und nahmen danach zu. Es war kein plastischer chirurgischer Eingriff erforderlich. Obwohl DMSO in Kombination mit Hypothermie und isotonischer Kochsalzlösung die verzögerten Symptome nicht wirksam verhinderte, schränkte es die Entzündung und Gewebenekrose ein. Ludwig et al berichteten, dass die Verwendung einer Mischung aus DMSO 90% und Alpha-Tocopherol 10% innerhalb von 48 Stunden nach Extravasationen von Anthracyclinen oder Mitomycin C bei 8 Patienten zu keiner Hautulzeration oder funktionellen oder neurovaskulären Beeinträchtigung führte.28 Leider ist Alpha-Tocopherol kein leicht verfügbares Arzneimittel, und es sollten weitere randomisierte Studien durchgeführt werden, um seine Verwendung zu validieren.
In einer prospektiven Studie mit 20 Patienten mit Anthracyclin-Extravasationen wurde DMSO 99% zweimal, 6-mal täglich für 2 Wochen verabreicht.29 Nach DMSO-Behandlung wurden keine Geschwüre beschrieben, obwohl anfängliche Schwellungen (85%), Erytheme (75%) und Schmerzen (60%) offensichtlich waren. Nach einer 3-monatigen Nachbeobachtungszeit bei 16 Patienten hatten 6 (38%) Patienten keine offensichtlichen Symptome und 10 (63%) pigmentierte Verhärtungen. Bertelli führte auch eine prospektive Studie durch, in der die Auswirkungen von DMSO auf Anthracyclin-Extravasationen untersucht wurden.30 Doxorubicin entfielen 11 Fälle und Epirubicin entfielen 46 Fälle. Die Patienten wurden 7 Tage lang alle 8 Stunden zu 99% mit DMSO behandelt. Siebzig Prozent der Patienten (40/57) hatten eine vollständige Auflösung der Extravasation innerhalb von 1 Woche, ein Patient hatte eine restliche Weichteilverhärtung und ein Patient hatte eine restliche Hyperpigmentierung.
In diesen Fallberichten und kleinen Studien wurden Extravasationen klinisch und nicht durch Biopsie diagnostiziert. DMSO kann eine Option für die Behandlung von extravasierten Anthracyclinen, Mitomycin C und Actinomycin D sein. Ein nicht okklusiver Verband sollte innerhalb von 10 bis 25 Minuten aufgetragen werden. Diese Schritte sollten 7 Tage lang alle 8 Stunden wiederholt werden.23 Obwohl DMSO in der Praxis als Behandlungsoption verwendet wurde, kann das Fehlen prospektiver Studien seine Verwendung einschränken. Die Extravasationsrichtlinien von EONS 2007 empfehlen die Durchführung weiterer Studien; DMSO 50% bis 99% können jedoch nach Ermessen des Klinikers in Betracht gezogen werden.23 Es ist wichtig zu beachten, dass keine der prospektiven DMSO-Studien einen Verband verwendete, damit die Haut das DMSO vollständig absorbieren konnte.
Hyaluronidase: Es wird angenommen, dass Hyaluronidase in der Lage ist, die extrazelluläre Matrix, die den Epithelzellen zugrunde liegt, abzubauen. Die Matrix hält große Mengen an Wassermolekülen fest und kann bei ihrem Abbau die Flüssigkeit in das extrazelluläre Milieu abgeben. Im Falle einer Extravasation ermöglicht es eine erhöhte Flüssigkeit an der Stelle, wodurch die tatsächliche Konzentration der Haut an der Kontaktstelle verdünnt wird.31,32 Hyaluronidase wurde zur Behandlung von Vinca-Alkaloid- und Taxan-Extravasationen eingesetzt.Es wurden 33 Dosen Hyaluronidase im Bereich von 150 bis 1.500 Einheiten verwendet, die in 1 ml normaler Kochsalzlösung subkutan oder intradermal innerhalb von 1 Stunde nach Extravasation verdünnt wurden.
In einer kleinen klinischen Studie mit 6 Patienten mit Vinblastin (n = 1), Vincristin (n = 1) und Vinorelbin (n = 4) Extravasation wurden 250 Einheiten Hyaluronidase in den Verweilkatheter oder subkutan injiziert (6 Injektionen) im Falle einer Verletzung. Es wurden keine Steroide oder Kühlpackungen angewendet. Die Schmerzen verschwanden bei allen Patienten innerhalb weniger Tage nach der Behandlung mit Hyaluronidase. Ein Patient klagte 3 Monate nach der Extravasation von Vincristin über eine leicht schmerzhafte Verhärtung.30 Diese Berichte liefern vielversprechende Informationen; Es mangelt jedoch insgesamt noch an Beweisen für die Verwendung von Hyaluronidase zur Behandlung von Vinca-Alkaloid-Extravasationen. Es müssen mehr prospektive Studien durchgeführt werden. Die Extravasationsrichtlinien von EONS 2007 empfehlen die Durchführung weiterer Studien; Hyaluronidase kann jedoch nach Ermessen des Arztes in empfohlenen Dosen als Option in Betracht gezogen werden.23
Natriumthiosulfat: Natriumthiosulfat verhindert Alkylierung und Gewebezerstörung, indem es ein Substrat für die Alkylierung im Unterhautgewebe bereitstellt. Natriumthiosulfat hat sich in Tierversuchen und in einem Fallbericht zur Behandlung der Mechlorethamin (Stickstoffmonoxid) -Extravasation als wirksam erwiesen.33,34 Die empfohlene Dosis beträgt 2 ml 0,17 M (eine Lösung von 4 ml 10% Natriumthiosulfat und 6 ml sterilem Wasser zur Injektion). Aufgrund fehlender Beweise empfehlen die Extravasationsrichtlinien von EONS 2007 dies nicht als Gegenmittel.22
Dexrazoxan: Dexrazoxan (Totect) wurde kürzlich von der FDA zur Behandlung von Anthracyclin-induzierten Extravasationen zugelassen. Dexrazoxan hat einen doppelten Wirkungsmechanismus: 1) Es wirkt als Eisenchelator und verhindert die Bildung von Eisen-Anthracyclin-Komplexen und eisenvermittelten Hydroxylradikalen, die oxidative Schäden verursachen; und 2) Es stabilisiert die Topoisomerase II und macht es für die Anthracyclin-Chemotherapie unzugänglich. Dexrazoxan blockiert das Enzym, so dass es nicht mehr von Anthracyclin beeinflusst wird und verhindert Schäden an den gesunden Zellen im Gewebe.35
Die Wirksamkeit von Dexrazoxan wurde in zwei klinischen Studien in Europa nachgewiesen.36 Beide Studien waren prospektive, offene, einarmige, multizentrische klinische Studien, die von Juli 2001 bis August 2005 mit insgesamt 80 Patienten durchgeführt wurden. Die erste Studie umfasste Patienten aus 17 Krebszentren in Dänemark und die zweite Patienten aus 34 Krebszentren in Dänemark, Deutschland, Italien und den Niederlanden. Die Anthrazyklin-Extravasation wurde diagnostiziert und durch Fluoreszenzmikroskopie von biopsiertem Gewebe bestätigt, das innerhalb von 6 Stunden nach Dexrazoxan entnommen wurde. Eine Stichprobengröße von 32 bewertbaren Patienten war erforderlich, um eine Verringerung der Inzidenz von Operationen um 70% oder mehr zu zeigen (einseitiger Binomialtest, a = .025, ß = .20). Der primäre Endpunkt war die Rate der chirurgischen Resektion und Nekrose. Vierundfünfzig der 80 Patienten (Studie 1: n = 18; Studie 2: n = 36) waren auswertbar (n = 13 negative Biopsien; n = 4 keine Biopsien durchgeführt; n = 8 Protokollverletzungen) mit einem Durchschnittsalter von 56 Jahren (Bereich 34-81 Jahre). Neunundsechzig Prozent (n = 37) der untersuchten Patienten waren weiblich. Dexrazoxan wurde als intravenöse Infusion über 1 bis 2 Stunden verabreicht; 1.000 mg / m2 innerhalb von 6 Stunden; 1.000 mg / m2 nach 24 Stunden; und 500 mg / m2 nach 48 Stunden Extravasation.36
Die Patienten wurden an den Tagen 7, 14, 21 und 28 auf Wirksamkeit und Sicherheit sowie an Tag 90 auf Wirksamkeit untersucht.36 Die häufigste Krebsdiagnose war Brustkrebs (50%), gefolgt von Lymphomen (39%) und anderen Krebsarten (9%). Bei den Patienten traten Extravasationen von Doxorubicin (n = 23) oder Epirubicin (n = 31) auf. Die mittlere Extravasationsfläche betrug in Studie 1 23,6 cm2 und in Studie 2 39 cm2. Elf Patienten hatten Extravasationsbereiche von mehr als 75 cm2. Es gab keine Inzidenz von Operationen in Studie 1 und 1 Vorfall (2,8%, 95% KI 0,1% -14,5%) in Studie 2. Der Patient, der aufgrund einer Extravasation eine Gewebenekrose entwickelte, hatte eine sehr große Doxorubicin-Extravasationsfläche von 253 cm2. Die Symptome nahmen in den Tagen nach der Extravasation zu, die Gewebenekrose trat 9 Tage nach der Extravasation des Patienten auf und die Nekrose wurde chirurgisch herausgeschnitten. In Studie 1 gab es 1 (5,6%) Nekrose aufgrund einer Biopsie, 6 (33.3%) Fälle von Verschiebung oder Absage einer geplanten Krebsbehandlung und 9 (50%) Krankenhausaufenthalte aufgrund der Extravasation. In Studie 2 gab es 1 (2,8%) Fälle von Nekrose aufgrund von Extravasation, 3 (8,3%) Fälle von Nekrose aufgrund von Biopsie, 10 (27,8%) Fälle von Verschiebungen oder Absagen der geplanten Krebsbehandlung aufgrund der Extravasation und 13 (36,1%) Fälle von Krankenhausaufenthalten aufgrund der Extravasation. Nach 3-monatiger Nachbeobachtung hatten 88,9% (n = 16) in Studie 1 keine negativen Folgen und 63,9% (n = 23) in Studie 2. Bei fünfzehn der 80 Patienten traten sensorische Störungen (n = 9), Hautatrophie (n = 5), Schmerzen (n = 10), Entstellung (n = 1) und Einschränkung (n = 3) auf. Die meisten Patienten (71%) konnten planmäßig eine weitere Chemotherapie erhalten. Zu den häufigsten Nebenwirkungen gehörten eine verminderte Anzahl weißer Blutkörperchen (72,5%), vermindertes Hämoglobin (42,5%), verminderte Thrombozytenzahl (26%), erhöhte Aspartataminotransferase (36,8%), erhöhte Alaninaminotransferase (23,9%), Reaktionen an der Injektionsstelle (27,5%) und Übelkeit (18,8%).36 Ergebnisse aus den klinischen Studien zeigten, dass Dexrazoxan ein wirksames Mittel zur Behandlung von akuten Anthracyclin-Extravasationen und zur Vorbeugung von verzögerten Symptomen ist. Eine Zusammenfassung dieser Behandlungsempfehlungen, einschließlich der EONS 2007-Richtlinien, ist in TABELLE 2 enthalten.
Rolle des Apothekers
Apotheker sollten eng in die Beurteilung und Behandlung aller chemotherapeutisch induzierten Extravasationen einbezogen werden. Sie können auf verschiedene Arten eine integrale Rolle spielen, darunter: 1) entwicklung von Richtlinien und Protokollen; 2) Patienten-, Familien- und multidisziplinäre Ausbildung; 3) Dokumentation und Berichterstattung über Extravasationen und andere unerwünschte Arzneimittelwirkungen nach der Therapie; und 4) Überwachung der richtigen Dosierung, Verabreichung und Wirksamkeit der Behandlung.
Schlussfolgerung
Alle überprüften Studien betrafen Erwachsene, da pädiatrische Patienten ein erhöhtes Risiko für Unruhe und Ziehen der Leitungen gehabt hätten. Bis heute ist Dexrazoxan das einzige Extravasationsmittel, das in großen, multizentrischen, prospektiven Studien untersucht wurde, die objektive, zuverlässige Tests zur Diagnose von Extravasationsfällen verwendeten. Trotz ihrer gemeinsamen Verwendung in der Praxis, andere pharmakologische Behandlungen, wie DMSO und Hyaluronidase, wurden nicht umfassend untersucht; Daher fehlen evidenzbasierte Empfehlungen. Das Management der Extravasation sollte nach Ermessen des Arztes in Zusammenarbeit mit allen Mitgliedern des Gesundheitsteams durchgeführt werden.
1. Infusion Krankenschwestern Gesellschaft. Infusion Pflege Standards der Praxis. In: J Infus Nurs. 2006;29(Ergänzung 1):S1-S92.
2. Polovich M, White J, Kelleher L. Richtlinien und Empfehlungen für Chemotherapie und Biotherapie für die Praxis. 2. Aufl. Pittsburgh, PA: Gesellschaft für Onkologie; 2005.
3. Ener RA, Meglathery SB, Styler M. Extravasation systemischer hämatoonkologischer Therapien. Ann Oncol. 2004;15:858-862.
4. Sauerland C, Egelking C, Wickman R, Corbi D. Vesikante Extravasation Teil I: Mechanismen, Pathogenese und Pflege zur Risikominderung. In: Oncol Nurs Forum. 2006;33:1134-1141.
5. Cassagnol M, Cohen H. Dermatologic toxicities of chemotherapeutic agents. US Pharm. 2008;33(1)(Oncology suppl):10-20.
6. Schulmeister L. Extravasation management. Semin Oncol Nurs. 2007;23:184-190.
7. Viale P. Chemotherapy and cutaneous toxicities: implications for oncology nurses. Semin Oncol Nurs. 2006;22:144-151.
8. Cox K, Stuart-Harris R, Abdini G, et al. The management of cytotoxic-drug extravasation: guide-lines drawn up by a working party for the Clinical Oncological Society of Australia. Med J Aust. 1988;148:185-189.
9. Schrijvers DL. Extravasation: eine gefürchtete Komplikation der Chemotherapie. Ann Oncol. 2003;14(suppl 3): iii26-iii30.
10. Der nationale Extravasationsinformationsdienst. www.extravasation.org.uk/home.html . Zugriff am 25. März 2009.
11. Lemmers N, Gels M, Sleijfer D, et al. Komplikationen von venösen Zugangsöffnungen bei 132 Patienten mit disseminiertem Hodenkrebs, die mit Polychemotherapie behandelt wurden. In: J Clin Oncol. 1996;14:2916-2922.
12. Shetty PC, Mody MK, Kastan DJ. Ergebnis von 350 implantierten Brustports, die von interventionellen Radiologen platziert wurden. In: J Vasc Interv Radiol. 1997;8:991-995.
13. In: Dorr RT. Antidote gegen vesikuläre Chemotherapieextravasationen. Blood Rev. 1990;4:41-60.
14. Langer SW, Sehested M, Jensen PB. Behandlung der Anthracyclin-Extravasation mit Dexrazoxan. Clin Cancer Res. 2000;6:3680-3686.
15. Raymond E, Faivre S, Woynarowski JM, Chaney SG. Oxaliplatin: Wirkungsmechanismus und antineoplastische Aktivität. In: Semin Oncol. 1998;2(Ergänzung 5):4-12.
16. Rivory LP. Neue Medikamente gegen Darmkrebs-Wirkmechanismen. Aust Prescr. 2002;25:108-110. www.australianprescriber.com/magazine/25/5/108/10 /. Zugriff am 25.März 2009.
17. Skeel RT. Handbuch der Krebschemotherapie. 5. Aufl. New York, NY: Lippincott Williams & Wilkins; 1999.
18. Boyle DM, Engelking C. Vesikante Extravasation: Mythen und Realitäten. In: Oncol Nurs Forum. 1995;22:57-67.
19. Hadaway LC. Prävention und Management peripherer Extravasation. Krankenpflege. 2004;34:66-67.
20. Shulmeister L, Camp-Sorrell D. Chemotherapie Extravasation von implantierten Ports. In: Oncol Nurs Forum. 2000;27:531-538.
21. Debets JM, Wils JA, Schlangen JT. Eine seltene Komplikation implantierter zentralvenöser Zugangsgeräte: Katheterfraktur und Embolisation. Unterstützung Pflege Krebs. 1995;3:432-434.
22. Gorski LA. Zentralvenöse Zugangsvorrichtung Verschlüsse. Teil 2: Nichtthrombotische Ursachen und Behandlung. Startseite Healthc Krankenschwester. 2003;21:168-171.
23. Extravasationsrichtlinien 2007. In: European Oncology Nursing Society. www.cancerworld.org/CancerWorld/getStaticModFile.aspx?id=2340 . Zugriff am 25. März 2009.
24. Rimso-50 (Dimethylsulfoxid) Packungsbeilage. Lake Forest, IL: Bioniche Pharma USA LLC; 2009.
25. Lawrence HJ, Gute Nacht SH. Dimethylsulfoxid, das Gewebeschäden begrenzt, die durch Extravasation von Doxorubicin-Wirkstoffen verursacht werden. In: Ann Intern Med. 1983;98:1025.
26. Olver IN, Schwarz MA. Use of dimethyl sulfoxide in limiting tissue damage caused by extravasation of doxorubicin . Cancer Treat Rep. 1983;67:407-408.
27. Berghammer P, Pohnl R, Baur M, Dittrich C. Docetaxel extravasation. Support Care Cancer. 2001;9:131-134.
28. Ludwig CU, Stoll HR, Obrist R, Obrecht JP. Prevention of cytotoxic drug-induced skin ulcers with dimethyl sulfoxide (DMSO) and alpha-tocopherole. Eur J Cancer Clin Oncol. 1987;23:327-329.
29. Olver IN, Aisner J, Hament A, et al. A prospective study of topical dimethyl sulfoxide for treating anthracycline extravasation. J Clin Oncol.1988;6:1732-1735.
30. Bertelli G. Prevention and management of extravasation of cytotoxic drugs. Drug Saf. 1995;12:245-255.
31. Balazs EA, Laurent TC, Jeanloz RW. Nomenclature of hyaluronic acid. Biochem J. 1986;235:903.
32. Girish KS, Kemparaju K. The magic glue hyaluronan and its eraser hyaluronidase. Life Sci. 2007;80:1921-1943.
33. Dorr T. Antidotes to vesicant chemotherapy extravasations. Blood Rev. 1990;4:41-60.
34. Owen OE, Dellatorre DL, Van Scott EJ, Cohen MR. Accidental intramuscular injection of mechlorethamine. Cancer. 1980;45:2225-2226.
35. Totect (dexrazoxane for injection) package insert. Copenhagen, Denmark: TopoTarget A/S; October 2007.
36. Mouridsen HT, Langer SW, Buter J, et al. Treatment of anthracycline extravasation with Savene (dexrazoxane). Results from two prospective clinical multicenter studies. Ann Oncol. 2007;18:546-550.
Leave a Reply