Anorganische Chemie
Die beschreibende anorganische Chemie konzentriert sich auf die Klassifizierung von Verbindungen anhand ihrer Eigenschaften. Teilweise konzentriert sich die Klassifizierung auf die Position des schwersten Elements (des Elements mit dem höchsten Atomgewicht) in der Verbindung im Periodensystem, teilweise durch Gruppierung von Verbindungen nach ihren strukturellen Ähnlichkeiten.
Klassifikationen der anorganischen Chemie:
Koordinationsverbindungenbearbeiten
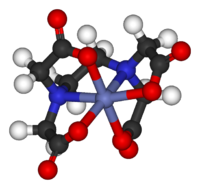
Klassische Koordinationsverbindungen weisen Metalle auf, die an „lone“ gebunden sind Elektronenpaare“, die sich auf den Hauptgruppenatomen von Liganden wie H2O, NH3, Cl− und CN- befinden. In modernen Koordinationsverbindungen können fast alle organischen und anorganischen Verbindungen als Liganden verwendet werden. Das „Metall“ ist normalerweise ein Metall aus den Gruppen 3-13 sowie die Trans-Lanthaniden und Trans-Actiniden, aber aus einer bestimmten Perspektive können alle chemischen Verbindungen als Koordinationskomplexe beschrieben werden.Die Stereochemie von Koordinationskomplexen kann sehr reichhaltig sein, wie Werner’s Trennung von zwei Enantiomeren von 6+ andeutet, eine frühe Demonstration, dass Chiralität organischen Verbindungen nicht inhärent ist. Ein aktuelles Thema innerhalb dieser Spezialisierung ist die supramolekulare Koordinationschemie.
- Beispiele: −, 3+, TiCl4(THF)2.
Main group compoundsbearbeiten

Diese Arten weisen Elemente aus Gruppen auf I, II, III, IV, V,VI, VII, 0 (ohne Wasserstoff) des Periodensystems. Aufgrund ihrer oft ähnlichen Reaktivität sind im Allgemeinen auch die Elemente in Gruppe 3 (Sc, Y und La) und Gruppe 12 (Zn, Cd und Hg) enthalten, und manchmal sind auch die Lanthaniden und Aktiniden enthalten.
Hauptgruppenverbindungen sind seit den Anfängen der Chemie bekannt, z.B. elementarer Schwefel und der destillierbare weiße Phosphor. Experimente an Sauerstoff, O2, von Lavoisier und Priestley identifizierten nicht nur ein wichtiges zweiatomiges Gas, sondern ebneten auch den Weg für die Beschreibung von Verbindungen und Reaktionen nach stöchiometrischen Verhältnissen. Die Entdeckung einer praktischen Synthese von Ammoniak unter Verwendung von Eisenkatalysatoren durch Carl Bosch und Fritz Haber in den frühen 1900er Jahren beeinflusste die Menschheit zutiefst und demonstrierte die Bedeutung der anorganisch-chemischen Synthese.Typische Hauptgruppenverbindungen sind SiO2, SnCl4 und N2O. Viele Hauptgruppenverbindungen können auch als „metallorganisch“ eingestuft werden, da sie organische Gruppen enthalten, z. B. B (CH 3) 3). Hauptgruppenverbindungen kommen auch in der Natur vor, z.B. Phosphat in der DNA, und können daher als bioanorganisch eingestuft werden. Umgekehrt können organische Verbindungen, denen (viele) Wasserstoffliganden fehlen, als „anorganisch“ eingestuft werden, wie die Fullerene, Buckytubes und binäre Kohlenstoffoxide.
- Beispiele: Tetraschwefeltetranitrid S4N4, Diboran B2H6, Silikone, Buckminsterfullerene C60.
Übergangsmetallverbindungen
Verbindungen, die Metalle der Gruppen 4 bis 11 enthalten, gelten als Übergangsmetallverbindungen. Verbindungen mit einem Metall aus der Gruppe 3 oder 12 werden manchmal auch in diese Gruppe eingebaut, aber auch oft als Hauptgruppenverbindungen klassifiziert.
Übergangsmetallverbindungen zeigen eine reiche Koordinationschemie, die von tetraedrisch für Titan (z. B. TiCl4) über quadratisch planar für einige Nickelkomplexe bis oktaedrisch für Koordinationskomplexe von Kobalt variiert. Eine Reihe von Übergangsmetallen kann in biologisch wichtigen Verbindungen wie Eisen in Hämoglobin gefunden werden.
- Beispiele: Eisenpentacarbonyl, Titantetrachlorid, Cisplatin
Metallorganische Verbindungenbearbeiten

Normalerweise wird angenommen, dass metallorganische Verbindungen die M-C-H-Gruppe enthalten. Das Metall (M) in diesen Spezies kann entweder ein Hauptgruppenelement oder ein Übergangsmetall sein. Operativ ist die Definition einer metallorganischen Verbindung entspannter, um auch hochlipophile Komplexe wie Metallcarbonyle und sogar Metallalkoholate einzuschließen.
Metallorganische Verbindungen werden hauptsächlich als eine spezielle Kategorie angesehen, da organische Liganden häufig empfindlich gegenüber Hydrolyse oder Oxidation sind, was erfordert, dass die metallorganische Chemie speziellere präparative Methoden verwendet als dies bei Komplexen vom Werner-Typ der Fall war. Synthetische Methoden, insbesondere die Fähigkeit, Komplexe in Lösungsmitteln mit geringer Koordinationsleistung zu manipulieren, ermöglichten die Erforschung sehr schwach koordinierender Liganden wie Kohlenwasserstoffe, H2 und N2. Da die Liganden in gewissem Sinne petrochemisch sind, hat der Bereich der metallorganischen Chemie stark von seiner Relevanz für die Industrie profitiert.
- Beispiele: Cyclopentadienyliron dicarbonyl dimer (C5H5)Fe(CO)2CH3, ferrocene Fe(C5H5)2, molybdenum hexacarbonyl Mo(CO)6, triethylborane Et3B, Tris(dibenzylideneacetone)dipalladium(0) Pd2(dba)3)
Cluster compoundsEdit
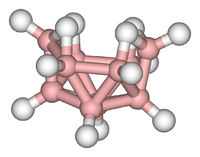

Cluster können in allen Klassen chemischer Verbindungen gefunden werden. Nach der allgemein akzeptierten Definition besteht ein Cluster minimal aus einem dreieckigen Satz von Atomen, die direkt miteinander verbunden sind. Metall-Metall-gebundene dimetallische Komplexe sind jedoch für den Bereich von hoher Relevanz. Cluster treten in „reinen“ anorganischen Systemen, der metallorganischen Chemie, der Hauptgruppenchemie und der bioanorganischen Chemie auf. Die Unterscheidung zwischen sehr großen Clustern und Schüttgütern verschwimmt zunehmend. Diese Grenzfläche ist die chemische Grundlage der Nanowissenschaften oder Nanotechnologie und entsteht speziell aus der Untersuchung von Quantengrößeneffekten in Cadmiumselenidclustern. Daher können große Cluster als eine Anordnung gebundener Atome beschrieben werden, deren Charakter zwischen einem Molekül und einem Feststoff liegt.
- Beispiele: Fe3(CO)12, B10H14, 2−, 4Fe-4S
Bioorganische Verbindungenbearbeiten

Per Definition kommen diese Verbindungen in der Natur vor, aber das Unterfeld umfasst anthropogene Arten wie Schadstoffe (z. B. Methylquecksilber) und Arzneimittel (z. B. Cisplatin). Das Gebiet, das viele Aspekte der Biochemie umfasst, umfasst viele Arten von Verbindungen, z. B. die Phosphate in der DNA, und auch Metallkomplexe, die Liganden enthalten, die von biologischen Makromolekülen, üblicherweise Peptiden, bis zu schlecht definierten Spezies wie Huminsäure reichen, und zu Wasser (z. B. koordiniert zu Gadoliniumkomplexen, die für die MRT verwendet werden). Traditionell konzentriert sich die bioanorganische Chemie auf den Elektronen- und Energietransfer in für die Atmung relevanten Proteinen. Die medizinische anorganische Chemie umfasst das Studium sowohl nicht essentieller als auch essentieller Elemente mit Anwendungen für Diagnose und Therapie.
- Beispiele: Hämoglobin, Methylquecksilber, Carboxypeptidase
Solid state Compoundsbearbeiten
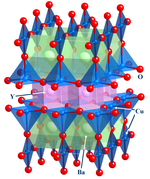
Dieser wichtige bereich konzentriert sich auf Struktur, Bindung und die physikalischen Eigenschaften von Materialien. In der Praxis verwendet die anorganische Festkörperchemie Techniken wie die Kristallographie, um ein Verständnis der Eigenschaften zu erlangen, die sich aus kollektiven Wechselwirkungen zwischen den Untereinheiten des Festkörpers ergeben. Zur Festkörperchemie gehören Metalle und deren Legierungen oder intermetallische Derivate. Verwandte Bereiche sind Physik der kondensierten Materie, Mineralogie und Materialwissenschaft.
- Beispiele: Siliziumchips, Zeolithe, YBa2Cu3O7
Leave a Reply