Analytische und pharmazeutische Forschung
Absorptionsspektren
Das Absorptionsspektrum von Thiamin wurde gegen Wasser aufgezeichnet (Abbildung 1), es wurde festgestellt, dass Thiamin eine maximale Absorptionsspitze (λ max) bei 235 nm aufweist. Aufgrund des stark blauverschobenen λ max von Thiamin ist seine Bestimmung in der Darreichungsform auf der Grundlage der direkten Messung seiner Absorption für Ultraviolett anfällig für mögliche Interferenzen durch die üblichen Hilfsstoffe. Daher war die Derivatisierung von Thiamin, um absorbierende Spezies im sichtbaren Bereich zu erreichen, zweifellos notwendig. So wurde eine Derivatisierung von Thiamin mit NBD-Cl durchgeführt und das Absorptionsspektrum des Produkts gegen Reagenzrohling aufgezeichnet (Abbildung 1). Es wurde gefunden, dass das Produkt braun gefärbt ist und λmax bei 434 nm aufweist, und das λmax von NBD-Cl betrug 342 nm. Das λmax des Thiamin-NBD-Cl-Derivats wurde rotverschoben, wodurch mögliche Interferenzen eliminiert wurden. Die Wellenlänge 434 nm wurde daher als optimal festgelegt.
Optimierung der Reaktionsbedingungen
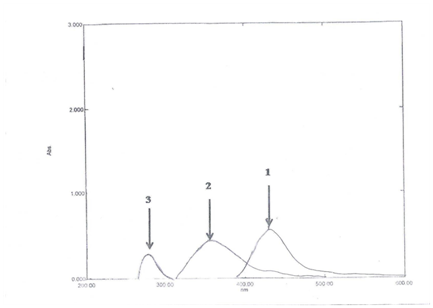
Abbildung 1: Absorptionsspektren von Thiamin (3), NBD-Cl (2) und dem Komplex dazwischen (1).
Die optimalen Bedingungen für das entwickelte Verfahren wurden durch Variation der Parameter nacheinander unter Beibehaltung der anderen Parameter und nach dem Effekt auf die Absorption des gefärbten Produkts festgelegt. Um experimentelle Bedingungen zu etablieren, wurde die Wirkung verschiedener Parameter wie pH-Wert, Zeit, Puffervolumen und Konzentration von NBD-Cl untersucht.
Wirkung des pH-Wertes
Die Wirkung des pH-Wertes auf die Reaktion zwischen Thiamin und NBD-Cl wurde durch Variation des pH-Wertes von 7,0 bis 12,0 getestet. Wie in Abbildung 2 gezeigt, ist die Absorption des Produkts bei pH 7,0 niedrig, was darauf hinweist, dass Thiamin in neutralen Medien nicht mit (NBD-Cl) reagieren kann. Dies war möglicherweise auf die Existenz der Aminogruppe von Thiamin in Form von Hydrochloridsalz zurückzuführen, was die nukleophile Substitutionsfähigkeit behindert. Als der pH-Wert von 7 auf 12 anstieg, stiegen die Messwerte dramatisch an, wodurch die Aminogruppe von Thiamin freigesetzt wurde und die nukleophile Substitution erleichtert wurde. Die maximale Absorption wurde bei einem pH-Wert von 10,5 erreicht. Bei pH-Werten über 10,5 trat eine Abnahme der Absorption auf. Dies wurde wahrscheinlich auf die Zunahme der Menge an Hydroxidion zurückgeführt, die die Geschwindigkeit der Rückreaktion von Thiamin mit NBD-Cl erhöht.
Einfluss der Reaktionszeit
Die Extinktion des Reaktionsproduktes wurde zu unterschiedlichen Zeitpunkten überwacht (Abbildung 3). Unter Beibehaltung anderer Bedingungen wurde die Extinktion des Reaktionsproduktes nach verschiedenen Standzeiten bei 25 ° C verfolgt. Die Ergebnisse zeigen, dass Thiamin bei 25 ° C mit NBD-Cl reagiert und die Extinktion allmählich ansteigt und nach 25min ein Maximum erreicht. Bei längeren Reaktionszeiten wurde ein leichter Abfall der Extinktion beobachtet. Dementsprechend wurden 25min als zweckmäßige Reaktionszeit für die Bestimmung eingestellt.
Wirkung der Puffermenge
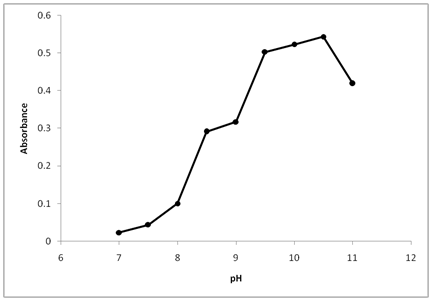
Abbildung 2: Wirkung des pH-Wertes auf die Reaktion von Thiamin mit NBD-Cl.
Thiamin (20 µg/ml): 1 ml, NBD-Cl Konz. 0,2% (w/v), Reaktionszeit 20 min.
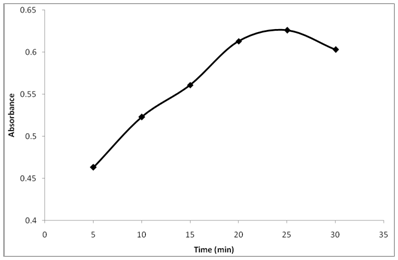
Abbildung 3: Einfluss der Reaktionszeit auf die Reaktion von Thiamin mit NBD-Cl.
Thiamin (20 µg/ml): 1 ml, Puffer (pH 10.5): 1,5 ml, NBD-Cl Konz. 0,2% (w/v).
Bei einem pH-Wert von 10,5 wurde auch der Einfluss der Menge der Pufferlösung auf die Absorption des Reaktionsprodukts untersucht (Abbildung 4). Die Abbildung zeigt, dass die Absorption des Reaktionsprodukts mit dem Anstieg der Menge an Pufferlösung schnell zunimmt und maximal wird, wenn die Menge an Pufferlösung 1,5 ml erreicht. Daher wurde die Menge an 1,5 ml Pufferlösung ausgewählt, um die höchste Absorption zu gewährleisten.
Wirkung der NBD-Cl-Konzentration
Die Untersuchung der Wirkung der NBD-Cl-Konzentrationen zeigte, dass die Reaktion von der Reagenzkonzentration abhängig war. Die höchste Absorptionsintensität wurde bei einer NBD-Cl-Konzentration von 0,2% (w / v) erreicht, und eine höhere Konzentration von NBD-Cl führt zu einer Abnahme der Extinktion (Abbildung 5).
Aus den obigen parametereinstellenden Experimenten wurden die optimierten Bedingungen für den Assay verwendet: pH 10,5, NBD-Cl-Konzentration 0,2% (w/ v), Volumen des Puffers 1,5 ml, Reaktionszeit 25min und Temperatur 25ºC.
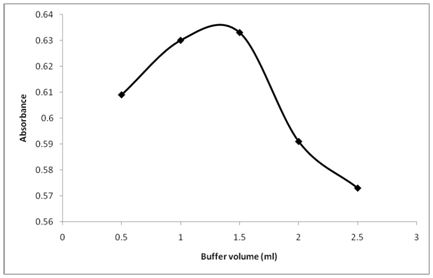
Abbildung 4: Wirkung der Puffermenge (ml) auf die Reaktion von Thiamin mit NBD-Cl.
Thiamin (20µg/ml): 1 ml, Puffer pH: 10,5, NBD-Cl Konz. 0,2% (w/v), Reaktionszeit 25 min.
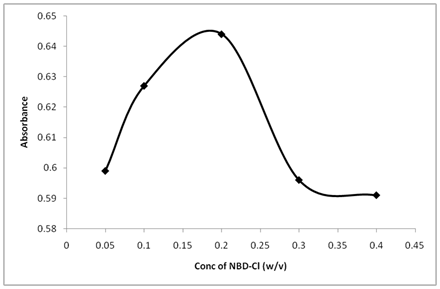
Abbildung 5: Einfluss der NBD-Cl-Konzentration auf die Reaktion mit Thiamin.
Thiamin (20µg/ml): 1 ml, Puffer (pH 10,5): 1,5 ml, Reaktionszeit 25 min.
Validierung der Methode
Die Methode wurde für die folgenden Parameter validiert: spezifität, Linearität, Präzision, Genauigkeit, Nachweisgrenze (LOD), Quantifizierungsgrenze (LOQ) und Robustheit gemäß den Richtlinien der International Conference on Harmonization (ICH) .
Linearität, Nachweisgrenze (LOD) Quantifizierungsgrenze (LOQ)
Die Linearität wurde durch lineare Regressionsanalyse bestimmt, indem sieben Thiaminkonzentrationen im Bereich von 05–35µg / ml konstruiert wurden, die mit der Methode der kleinsten quadratischen Regression berechnet wurden, um die Kalibrierungsgleichung und den Korrelationskoeffizienten zu berechnen. Die Kalibrierkurven wurden durch Zeichnen der Konzentration gegen die Extinktion unter Verwendung einer linearen Regressionsanalyse erstellt. Die Regressionsgleichung für die Ergebnisse war A = 0,033 x – 0,009 (r2 = 0,999), wobei A die Extinktion bei 434 nm ist, x die Konzentration von Thiamin in µg / ml im Bereich von 05-35 µg / ml ist und r der Korrelationskoeffizient ist (Tabelle 1). Es wurde festgestellt, dass der lineare Konzentrationsbereich mit unserer bisherigen Methode unter Verwendung von NQS vergleichbar ist. Die Detektionsgrenze (LOD) und die Quantifizierungsgrenze (LOQ) wurden gemäß der folgenden Formel LOD=3 bestimmt.3 × SDa / b und LOQ = 10 × SDa / b, SDa ist die Standardabweichung des Schnittpunkts; b ist die Steigung unter den ICH-Richtlinien . LOD und LOQ betrugen 0,667 bzw. 2,020 µg/ml (Tabelle 1).
|
Parameter |
Wert |
|
Messung wellenlänge (nm) |
|
|
Linearer Bereich (µg/ml) |
|
|
Regressionsgleichung |
y = 0,033x – 0.009 |
|
Intercept |
|
|
Standard deviation of intercept |
|
|
Slope |
|
|
Standard deviation of slope |
|
|
Correlation coefficient (r2) |
|
|
Limit of detection, LOD (μg/mL) |
|
|
Limit of quant., LOQ (μg/mL) |
Table 1: Parameters for the performance of the proposed method.
Genauigkeit
Die Genauigkeit der vorgeschlagenen Methode wurde durchgeführt, indem 3 verschiedene Konzentrationen von 10, 20 und 30 µg / ml Thiaminarzneimittel innerhalb eines linearen Bereichs angewendet wurden, der als Prozentsatz des aus den Proben gewonnenen Arzneimittels berechnet wurde (Tabelle 2).
|
Sample No |
Sample Content (µg/mL) |
Thiamine Standard Amount (µg/mL) |
Amount Found (Total) (µg/ml) |
Recovery + SD* |
|
96.29+0.015 |
||||
|
98.90+0.018 |
||||
|
101.47+0.148 |
Table 2: Rückgewinnungsstudien zur Bestimmung von Thiamin nach dem vorgeschlagenen Verfahren.
*Werte sind Mittelwert von drei Bestimmungen.
Der relative Fehler (RE) lag innerhalb von 0,24% mit einer entsprechenden Standardabweichung innerhalb von 0,004 für drei verschiedene Bestimmungen (Tabelle 3).
|
Sample No |
Concentration (μg/mL) |
Concentration |
Recovery (% + SD) |
Relative Error (%) |
|
95.5±0.004 |
||||
|
96.46±0.002 |
||||
|
97,50±0,003 |
Tabelle 3: Bewertung der Genauigkeit und Präzision.
Robustheit
Reaktionsmechanismus: Es wurde berichtet, dass NBD-Cl mit Aminogruppen von primären oder sekundären Aminderivaten reagiert . In ähnlicher Weise kann die Aminogruppe von Thiamin aufgrund des einsamen Elektronenpaares am Stickstoffatom als Nukleophil wirken und das Elektronenmangelzentrum in NBD–Cl angreifen (Tabelle 4 & Abbildung 6). Gleichzeitig wurde nachgewiesen, dass die Zusammensetzung des Produkts 1:1 aus Thiamin und NBD-Cl ist (Abbildung 7). So wird geschlossen, dass die Aminogruppe von Thiamin mit NBD-Cl reagiert, um ein braunes Addukt zu bilden. Die Reaktionsgleichung ist in Abbildung 7 dargestellt.

Abbildung 6: The Job’s method plot for the stoichiometry of the reaction of Thiamine with NBD-Cl Vr: Volume of NBD-Cl (7.5×10-4 mol/L), Vt: Volume of Thiamine (7.5×10-4 mol/L), Vr + Vt=10 ml.
|
Parameter |
Recovery (% ± SD) |
|
Recommended condition |
97.50±0.003 |
|
NBD-Cl concentration (0.22%) |
98.75±0.002 |
|
NBD-Cl concentration (0.180%) |
96.76%±0,003 |
|
Puffer-PH-Wert(10,7) |
96,90±0,002 |
|
Puffer-PH-Wert(10,3) |
95,79±0,22 |
|
Reaktionszeit min (23) |
96,09±0,009 |
|
Reaktionszeit min (27) |
98,01±0,003 |
Tabelle 4: Einfluss einer geringen Variation der Assaybedingung auf die analytische Leistung der vorgeschlagenen spektrophotometrischen Methode zur Bestimmung von Thiamin unter Verwendung von NBD-Cl-Reagenz.
Anwendung der vorgeschlagenen Methode zur Analyse der Thiamin-Darreichungsform
Thiamintabletten wurden der Analyse durch die vorgeschlagene unterzogen und der Etikettenanspruch stimmt gut mit unserer neuen Methode überein, wie in Tabelle 5 gezeigt. Das vorgeschlagene Verfahren hat den Vorteil, daß es praktisch frei von Störungen durch Hilfsstoffe ist.
|
Brand Name of Label Claim (Mg) |
Amount Found (Mg) |
(% Found ± SD)a |
|
Thiamine tablets (100 mg) |
99.9±0.025 |
Table 5: Analysis of Thiamine-containing dosage form by the proposed method.
a: values are mean of five determinations.
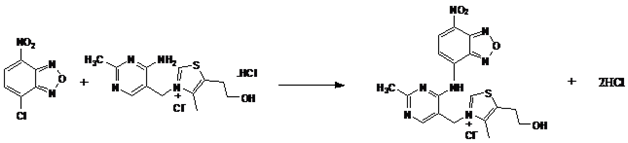
Figure 7: Reaktion von Thiamin mit NBD-Cl mit 1:1 Stöchiometrie.
Leave a Reply