2.4B: Dehydration Synthesis
Dehydration Synthesis
Die meisten Makromoleküle bestehen aus einzelnen Untereinheiten oder Bausteinen, die als Monomere bezeichnet werden. Die Monomere verbinden sich über kovalente Bindungen zu größeren Molekülen, die als Polymere bekannt sind. Dabei setzen Monomere Wassermoleküle als Nebenprodukte frei. Diese Art der Reaktion wird als Dehydrationssynthese bezeichnet, was bedeutet, „zusammenzufügen, während Wasser verloren geht. “ Es wird auch als Kondensationsreaktion angesehen, da zwei Moleküle zu einem größeren Molekül kondensiert werden, wobei ein kleineres Molekül (das Wasser) verloren geht.)
Bei einer Dehydratisierungssynthesereaktion zwischen zwei nicht ionisierten Monomeren, wie Monosaccharidzuckern, verbindet sich der Wasserstoff eines Monomers mit der Hydroxylgruppe eines anderen Monomers und setzt dabei ein Wassermolekül frei. Die Entfernung eines Wasserstoffs von einem Monomer und die Entfernung einer Hydroxylgruppe von dem anderen Monomer ermöglicht es den Monomeren, Elektronen zu teilen und eine kovalente Bindung zu bilden. Somit werden die Monomere, die miteinander verbunden sind, dehydriert, um die Synthese eines größeren Moleküls zu ermöglichen.
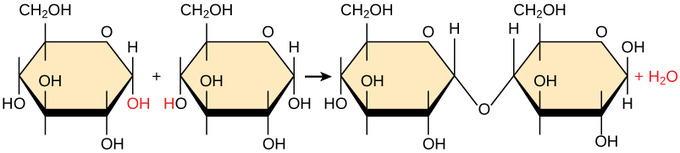
Wenn die Monomere ionisiert werden, wie dies bei Aminosäuren in einer wässrigen Umgebung wie Zytoplasma der Fall ist, werden zwei Wasserstoffatome vom positiv geladenen Ende eines Monomers mit einem Sauerstoff vom negativ geladenen Ende eines anderen Monomers kombiniert, wobei wiederum Wasser gebildet wird, das als Nebenprodukt freigesetzt wird, und die beiden Monomere erneut mit einer kovalenten Bindung verbindet.

Wenn sich zusätzliche Monomere über mehrere Dehydratisierungssynthesereaktionen verbinden, beginnt die Kette sich wiederholender Monomere ein Polymer zu bilden. Verschiedene Arten von Monomeren können sich in vielen Konfigurationen kombinieren, wodurch eine vielfältige Gruppe von Makromolekülen entsteht. Drei der vier Hauptklassen biologischer Makromoleküle (komplexe Kohlenhydrate, Nukleinsäuren und Proteine) bestehen aus Monomeren, die sich über Dehydrationssynthesereaktionen miteinander verbinden. Komplexe Kohlenhydrate werden aus Monosacchariden, Nukleinsäuren aus Mononukleotiden und Proteine aus Aminosäuren gebildet.
Es gibt eine große Vielfalt in der Art und Weise, wie sich Monomere zu Polymeren verbinden können. Beispielsweise sind Glucosemonomere die Bestandteile von Stärke, Glykogen und Cellulose. Diese drei sind Polysaccharide, klassifiziert als Kohlenhydrate, die sich als Ergebnis mehrerer Dehydrationssynthesereaktionen zwischen Glucosemonomeren gebildet haben. Die Art und Weise, wie sich Glucosemonomere miteinander verbinden, insbesondere die Lage der kovalenten Bindungen zwischen verbundenen Monomeren und die Orientierung (Stereochemie) der kovalenten Bindungen, führt jedoch zu diesen drei verschiedenen Polysacchariden mit unterschiedlichen Eigenschaften und Funktionen. In Nukleinsäuren und Proteinen variieren der Ort und die Stereochemie der kovalenten Bindungen, die die Monomere verbinden, nicht von Molekül zu Molekül, sondern die verschiedenen Arten von Monomeren (fünf verschiedene Monomere in Nukleinsäuren, A-, G-, C-, T- und U-Mononukleotide; 21 verschiedene Aminosäuremonomere in Proteinen) sind in einer Vielzahl von Sequenzen kombiniert. Jedes Protein oder jede Nukleinsäure mit einer anderen Sequenz ist ein anderes Molekül mit unterschiedlichen Eigenschaften.
Leave a Reply