13.7: Aromatische Verbindungen- Benzol
Lernziele
- Beschreibung der Bindung in Benzol und der Art und Weise, wie sich typische Reaktionen von Benzol von denen der Alkene unterscheiden.
Als nächstes betrachten wir eine Klasse von Kohlenwasserstoffen mit Molekülformeln wie die ungesättigten Kohlenwasserstoffe, die jedoch im Gegensatz zu den Alkenen nicht ohne weiteres Additionsreaktionen eingehen. Diese Verbindungen umfassen eine eigene Klasse, genannt aromatische Kohlenwasserstoffe, mit einzigartigen Strukturen und Eigenschaften. Wir beginnen mit der einfachsten dieser Verbindungen. Benzol (C6H6) ist von großer kommerzieller Bedeutung, hat aber auch bemerkenswerte gesundheitliche Auswirkungen.
Die Formel C6H6 scheint darauf hinzudeuten, dass Benzol einen hohen Grad an Ungesättigtheit aufweist. (Hexan, der gesättigte Kohlenwasserstoff mit sechs Kohlenstoffatomen, hat die Formel C6H14- acht Wasserstoffatome mehr als Benzol.) Trotz des scheinbar geringen Sättigungsgrades ist Benzol jedoch eher unreaktiv. Es reagiert beispielsweise nicht leicht mit Brom, was ein Test für die Ungesättigtheit ist.
Benzol ist eine Flüssigkeit, die nach Benzin riecht, bei 80 ° C siedet und bei 5,5 ° C gefriert. Es wurde früher zum Entkoffeinieren von Kaffee verwendet und war ein wesentlicher Bestandteil vieler Verbraucherprodukte, wie z. B. Abbeizmittel, Gummizemente und Fleckenentferner für die chemische Reinigung zu Hause. Es wurde in den 1950er Jahren aus vielen Produktformulierungen entfernt, aber andere verwendeten weiterhin Benzol in Produkten bis in die 1970er Jahre, als es mit Leukämie-Todesfällen in Verbindung gebracht wurde. Benzol ist in der Industrie immer noch wichtig als Vorläufer bei der Herstellung von Kunststoffen (wie Styropor und Nylon), Arzneimitteln, Reinigungsmitteln, synthetischem Kautschuk, Pestiziden und Farbstoffen. Es wird als Lösungsmittel für die Reinigung und Wartung von Druckgeräten und für Klebstoffe verwendet, wie sie zum Befestigen von Sohlen an Schuhen verwendet werden. Benzol ist ein natürlicher Bestandteil von Erdölprodukten, aber da es ein bekanntes Karzinogen ist, ist seine Verwendung als Zusatzstoff in Benzin jetzt begrenzt.
Um die überraschenden Eigenschaften von Benzol zu erklären, nehmen Chemiker an, dass das Molekül eine zyklische, hexagonale, planare Struktur von sechs Kohlenstoffatomen mit jeweils einem Wasserstoffatom aufweist. Wir können eine Struktur mit alternativen Einfach- und Doppelbindungen schreiben, entweder als vollständige Strukturformel oder als Linien-Winkel-Formel:
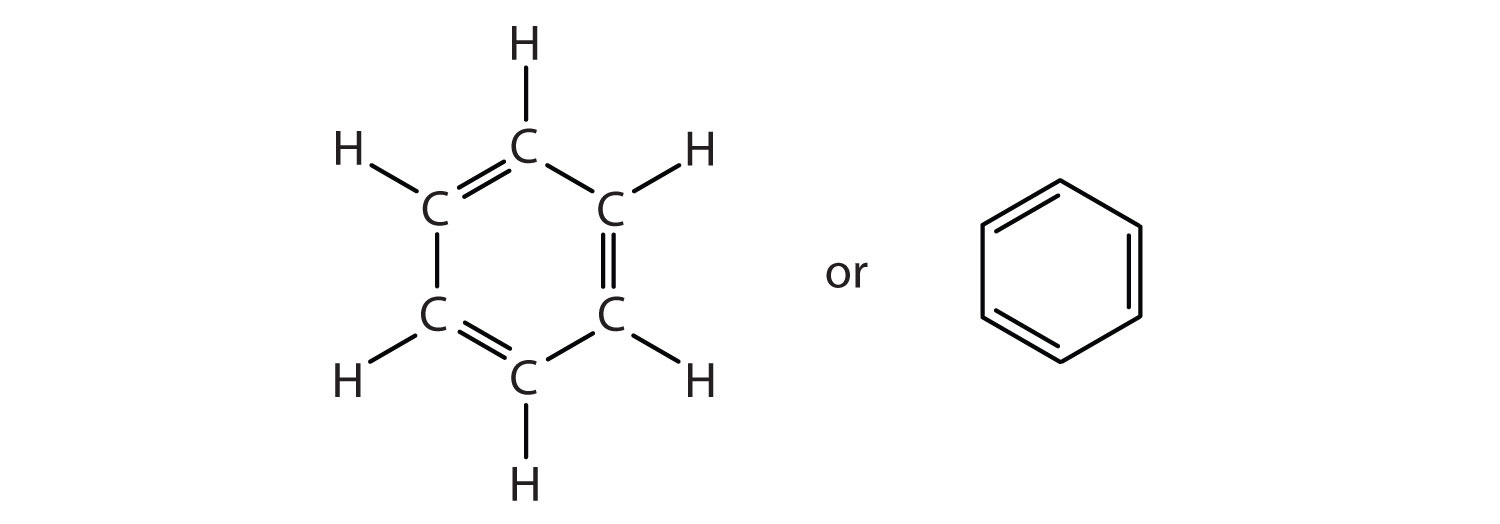
Diese Strukturen erklären jedoch nicht die einzigartigen Eigenschaften von Benzol. Darüber hinaus zeigen experimentelle Beweise, dass alle Kohlenstoff-zu-Kohlenstoff-Bindungen in Benzol äquivalent sind und das Molekül ungewöhnlich stabil ist. Chemiker stellen Benzol oft als Sechseck mit einem eingeschriebenen Kreis dar:

Der innere Kreis zeigt an, dass die Valenzelektronen gleichmäßig von allen sechs Kohlenstoffatomen geteilt werden (dh die Elektronen sind delokalisiert oder über alle Kohlenstoffatome verteilt). Es versteht sich, dass jede Ecke des Sechsecks von einem Kohlenstoffatom besetzt ist und an jedes Kohlenstoffatom ein Wasserstoffatom gebunden ist. Jedes andere Atom oder jede andere Gruppe von Atomen, die für ein Wasserstoffatom substituiert sind, muss an eine bestimmte Ecke des Sechsecks gebunden sein. Wir verwenden diese moderne Symbolik, aber viele Wissenschaftler verwenden immer noch die frühere Struktur mit alternativen Doppel- und Einfachbindungen.
Für Ihre Gesundheit: Benzol und uns
Der größte Teil des kommerziell verwendeten Benzols stammt aus Erdöl. Es wird als Ausgangsmaterial für die Herstellung von Waschmitteln, Arzneimitteln, Farbstoffen, Insektiziden und Kunststoffen verwendet. Einst als organisches Lösungsmittel weit verbreitet, ist bekannt, dass Benzol sowohl kurz- als auch langfristige toxische Wirkungen hat. Das Einatmen großer Konzentrationen kann Übelkeit und sogar den Tod aufgrund von Atemwegs- oder Herzversagen verursachen, während wiederholte Exposition zu einer fortschreitenden Erkrankung führt, bei der die Fähigkeit des Knochenmarks, neue Blutzellen zu bilden, schließlich zerstört wird. Dies führt zu einer als aplastische Anämie bezeichneten Erkrankung, bei der die Anzahl der roten und weißen Blutkörperchen abnimmt.
Concept Review Exercises
- Wie unterscheiden sich die typischen Reaktionen von Benzol von denen der Alkene?
- Beschreiben Sie kurz die Bindung in Benzol.
- Was bedeutet der Kreis in der Darstellung von Benzol durch den Chemiker?
- Benzol reagiert gegenüber Additionsreaktionen im Vergleich zu einem Alken eher unreaktiv.
- Valenzelektronen werden von allen sechs Kohlenstoffatomen gleichermaßen geteilt (dh die Elektronen sind delokalisiert).
- Die sechs Elektronen werden zu gleichen Teilen von allen sechs Kohlenstoffatomen geteilt.
- Benzol reagiert gegenüber Additionsreaktionen im Vergleich zu einem Alken eher unreaktiv.
- Valenzelektronen werden von allen sechs Kohlenstoffatomen gleichermaßen geteilt (dh die Elektronen sind delokalisiert).
- Die sechs Elektronen werden zu gleichen Teilen von allen sechs Kohlenstoffatomen geteilt.
Key Takeaway
- Aromatische Kohlenwasserstoffe scheinen ungesättigt zu sein, aber sie haben eine spezielle Art der Bindung und unterliegen keinen Additionsreaktionen.
Übungen
- Zeichnen Sie die Struktur von Benzol so, als hätte es alternative Einfach- und Doppelbindungen.
- Zeichnen Sie die Struktur von Benzol, wie Chemiker es heute normalerweise darstellen.

Leave a Reply