Übergangsmetall
Es gibt eine Reihe von Eigenschaften, die von den Übergangselementen geteilt werden, die in anderen Elementen nicht gefunden werden, was sich aus der teilweise gefüllten d-Schale ergibt. Dazu gehören
- die Bildung von Verbindungen, deren Farbe auf elektronische d–d-Übergänge zurückzuführen ist
- die Bildung von Verbindungen in vielen Oxidationsstufen aufgrund der relativ geringen Energielücke zwischen verschiedenen möglichen Oxidationsstufen
- die Bildung vieler paramagnetischer Verbindungen aufgrund der Anwesenheit ungepaarter d-Elektronen. Einige wenige Verbindungen von Hauptgruppenelementen sind auch paramagnetisch (z.B. stickstoffmonoxid, Sauerstoff)
Die meisten Übergangsmetalle können an eine Vielzahl von Liganden gebunden werden, was eine Vielzahl von Übergangsmetallkomplexen ermöglicht.
Farbige Verbindungen

3)
2 (rot); K
2Cr
2O
7 (orange); K
2CrO
4 (gelb) ; NiCl
2 (türkis); CuSO
4 (blau); KMnO
4 (lila).
Farbe in Metallverbindungen der Übergangsreihe ist im Allgemeinen auf elektronische Übergänge zweier Haupttypen zurückzuführen.
- Ladungstransferübergänge. Ein Elektron kann von einem überwiegend Ligandenorbital zu einem überwiegend Metallorbital springen, was zu einem Übergang von Ligand zu Metallladungstransfer (LMCT) führt. Diese können am leichtesten auftreten, wenn sich das Metall in einer hohen Oxidationsstufe befindet. Beispielsweise ist die Farbe von Chromat-, Dichromat- und Permanganat-Ionen auf LMCT-Übergänge zurückzuführen. Ein anderes Beispiel ist, dass Quecksilberjodid, HgI2, wegen eines LMCT-Übergangs rot ist.
Ein Metall-zu-Ligand-Ladungstransferübergang (MLCT) ist am wahrscheinlichsten, wenn sich das Metall in einer niedrigen Oxidationsstufe befindet und der Ligand leicht reduziert werden kann.
Im Allgemeinen ergeben Ladungstransferübergänge intensivere Farben als D-d-Übergänge.
- d-d-Übergänge. Ein Elektron springt von einem d-Orbital zum anderen. In Komplexen der Übergangsmetalle haben die d-Orbitale nicht alle die gleiche Energie. Das Muster der Spaltung der d-Orbitale kann unter Verwendung der Kristallfeldtheorie berechnet werden. Das Ausmaß der Spaltung hängt vom jeweiligen Metall, seiner Oxidationsstufe und der Art der Liganden ab. Die tatsächlichen Energieniveaus sind in Tanabe-Sugano-Diagrammen dargestellt.
In zentrosymmetrischen Komplexen, wie oktaedrischen Komplexen, sind D-d-Übergänge durch die Laporte-Regel verboten und treten nur aufgrund einer vibronischen Kopplung auf, bei der eine molekulare Schwingung zusammen mit einem d-d-Übergang auftritt. Tetraedrische Komplexe haben eine etwas intensivere Farbe, da das Mischen von d- und p-Orbitalen möglich ist, wenn kein Symmetriezentrum vorhanden ist. Die molare Absorptionsfähigkeit (ε) von Banden, die durch d-d−Übergänge verursacht werden, ist relativ gering, etwa im Bereich von 5-500 M−1 cm−1 (wobei M = mol dm-3). Einige d-d-Übergänge sind Spin verboten. Ein Beispiel kommt in oktaedrischen, Hochspinkomplexen von Mangan (II) vor, das eine d5-Konfiguration hat, in der alle fünf Elektronen parallele Spins haben; Die Farbe solcher Komplexe ist viel schwächer als in Komplexen mit Spin-Spin-Übergängen. Viele Verbindungen des Mangans(II) erscheinen fast farblos. Das Spektrum von 2+
zeigt ein maximales molares Absorptionsvermögen von etwa 0,04 M-1cm-1 im sichtbaren Spektrum.
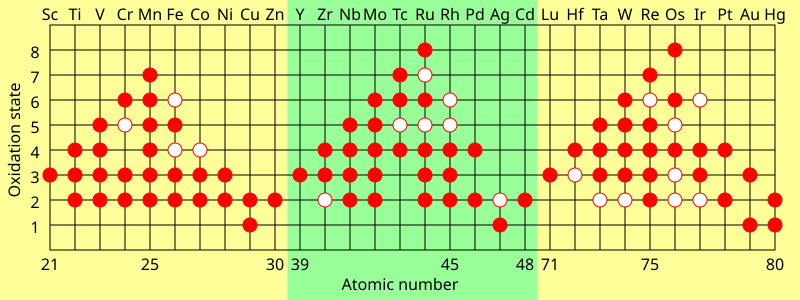
Oxidationsstufen
Charakteristisch für Übergangsmetalle ist, dass sie zwei oder mehr Oxidationsstufen aufweisen, die sich üblicherweise um eins unterscheiden. Beispielsweise sind Verbindungen des Vanadiums in allen Oxidationsstufen zwischen -1, wie −
, und +5, wie VO3−
Hauptgruppenelemente in den Gruppen 13 bis 18 weisen ebenfalls mehrere Oxidationsstufen auf. Die „gemeinsamen“ Oxidationsstufen dieser Elemente unterscheiden sich typischerweise um zwei statt um eins. Zum Beispiel existieren Verbindungen von Gallium in den Oxidationsstufen +1 und +3, in denen es ein einzelnes Galliumatom gibt. Keine Verbindung von Ga (II) ist bekannt: Jede solche Verbindung hätte ein ungepaartes Elektron und würde sich wie ein freies Radikal verhalten und schnell zerstört werden. Die einzigen Verbindungen, in denen Gallium eine formale Oxidationsstufe von +2 hat, sind dimere Verbindungen wie 2-
, die eine Ga-Ga-Bindung enthalten, die aus dem ungepaarten Elektron an jedem Ga-Atom gebildet wird. Somit besteht der Hauptunterschied in den Oxidationsstufen zwischen Übergangselementen und anderen Elementen darin, dass Oxidationsstufen bekannt sind, in denen ein einzelnes Atom des Elements und ein oder mehrere ungepaarte Elektronen vorhanden sind.
Die maximale Oxidationsstufe in den Übergangsmetallen der ersten Reihe entspricht der Anzahl der Valenzelektronen von Titan (+4) bis Mangan (+7), nimmt jedoch in den späteren Elementen ab. In der zweiten Reihe tritt das Maximum mit Ruthenium (+8) und in der dritten Reihe mit Iridium (+9) auf. In Verbindungen wie −
und OsO
4 erreichen die Elemente durch kovalente Bindung eine stabile Konfiguration.
Die niedrigsten Oxidationsstufen zeigen sich in Metallcarbonylkomplexen wie Cr(CO)
6 (Oxidationsstufe Null) und 2−
(Oxidationsstufe -2), in denen die 18-Elektronen-Regel befolgt wird. Diese Komplexe sind auch kovalent.
Ionische Verbindungen werden meist mit Oxidationsstufen +2 und +3 gebildet. In wässriger Lösung werden die Ionen durch (üblicherweise) sechs oktaedrisch angeordnete Wassermoleküle hydratisiert.
Magnetismus
Übergangsmetallverbindungen sind paramagnetisch, wenn sie ein oder mehrere ungepaarte d-Elektronen haben. In oktaedrischen Komplexen mit vier bis sieben d-Elektronen sind sowohl High-Spin- als auch Low-Spin-Zustände möglich. Tetraedrische Übergangsmetallkomplexe wie 2-
haben einen hohen Spin, da die Kristallfeldaufteilung klein ist, so dass die Energie, die durch die Elektronen in Orbitalen mit niedrigerer Energie gewonnen werden muss, immer geringer ist als die Energie, die zum Paaren der Spins benötigt wird. Einige Verbindungen sind diamagnetisch. Dazu gehören oktaedrische, Low-Spin-, d6- und quadratisch-planare d8-Komplexe. In diesen Fällen ist die Kristallfeldaufteilung so, dass alle Elektronen gepaart sind.Ferromagnetismus tritt auf, wenn einzelne Atome paramagnetisch sind und die Spinvektoren in einem kristallinen Material parallel zueinander ausgerichtet sind. Metallisches Eisen und die Legierung Alnico sind Beispiele für ferromagnetische Materialien mit Übergangsmetallen. Antiferromagnetismus ist ein weiteres Beispiel für eine magnetische Eigenschaft, die sich aus einer bestimmten Ausrichtung einzelner Spins im festen Zustand ergibt.
Katalytische Eigenschaften
Die Übergangsmetalle und ihre Verbindungen sind für ihre homogene und heterogene katalytische Aktivität bekannt. Diese Aktivität wird ihrer Fähigkeit zugeschrieben, mehrere Oxidationsstufen anzunehmen und Komplexe zu bilden. Vanadium (V) oxid (im Kontaktverfahren), feinteiliges Eisen (im Haber-Verfahren) und Nickel (in der katalytischen Hydrierung) sind einige der Beispiele. Katalysatoren an einer festen Oberfläche (Nanomaterial-basierte Katalysatoren) beinhalten die Bildung von Bindungen zwischen Reaktantenmolekülen und Atomen der Oberfläche des Katalysators (Übergangsmetalle der ersten Reihe verwenden 3d- und 4s-Elektronen zur Bindung). Dies bewirkt eine Erhöhung der Konzentration der Reaktanten an der Katalysatoroberfläche und auch eine Schwächung der Bindungen in den reagierenden Molekülen (die Aktivierungsenergie wird gesenkt). Auch weil die Übergangsmetallionen ihre Oxidationsstufen ändern können, werden sie als Katalysatoren wirksamer.Eine interessante Art der Katalyse tritt auf, wenn die Produkte einer Reaktion die Reaktion katalysieren, die mehr Katalysator erzeugt (Autokatalyse). Ein Beispiel ist die Reaktion von Oxalsäure mit angesäuertem Kaliumpermanganat (oder Manganat (VII)). Sobald ein wenig Mn2 + hergestellt wurde, kann es mit MnO4 reagieren − Mn3 + bilden. Dieses reagiert dann mit C2O4- Ionen und bildet wieder Mn2+.
Physikalische Eigenschaften
Wie der Name schon sagt, sind alle Übergangsmetalle Metalle und damit elektrische Leiter.
Im Allgemeinen besitzen Übergangsmetalle eine hohe Dichte und hohe Schmelz- und Siedepunkte. Diese Eigenschaften sind auf die metallische Bindung durch delokalisierte d-Elektronen zurückzuführen, was zu einer Kohäsion führt, die mit der Anzahl der gemeinsamen Elektronen zunimmt. Die Metalle der Gruppe 12 haben jedoch viel niedrigere Schmelz- und Siedepunkte, da ihre vollen d–Unterschalen eine DD-Bindung verhindern, was wiederum dazu neigt, sie von den akzeptierten Übergangsmetallen zu unterscheiden. Quecksilber hat einen Schmelzpunkt von -38,83 ° C (-37,89 ° F) und ist bei Raumtemperatur flüssig.
Leave a Reply