Peptidbindning
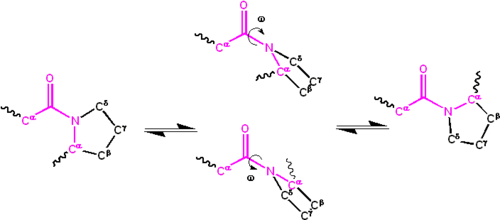
signifikant delokalisering av det ensamma paret av elektroner på kväveatomen ger gruppen en partiell dubbelbindningskaraktär. Den partiella dubbelbindningen gör amidgruppen plan, som förekommer i antingen cis-eller trans-isomererna. I det utfällda tillståndet av proteiner är peptidgrupperna fria att isomerisera och anta båda isomererna; i det vikta tillståndet antas emellertid endast en enda isomer vid varje position (med sällsynta undantag). Transformen föredras överväldigande i de flesta peptidbindningar (ungefär 1000:1-förhållande i trans:cis-populationer). X-Pro peptidgrupper tenderar emellertid att ha ETT ungefär 30:1-förhållande, förmodligen eftersom symmetrin mellan C. C. C. {\displaystyle \mathrm {C^{\alpha }} }

och C. C. displaystyle\mathrm {C^{\delta }} }

atomer av prolin gör CIS och trans isomerer nästan lika i energi (se figur nedan).
den dihedrala vinkeln associerad med peptidgruppen (definierad av de fyra atomerna c − c − c ’ − n-c-c {\displaystyle C^{\alpha}-C^{\prime}- N-C^{\alpha }}

) är betecknad {\displaystyle \Omega }

;

för trans isomeren (antiperiplanar konformation). Amidgrupper kan isomerisera om c ’ – N-bindningen mellan cis – och transformerna, om än långsamt ({\displaystyle \tau \sim }

20 sekunder vid rumstemperatur). Övergången anger att den partiella dubbelbindningen bryts, så att aktiveringsenergin är ungefär 80 kilojoule/mol (20 kcal/mol). Aktiveringsenergin kan emellertid sänkas (och isomeriseringen katalyseras) genom förändringar som gynnar den enkelbundna formen, såsom att placera peptidgruppen i en hydrofob miljö eller donera en vätebindning till kväveatomen i en X-Pro peptidgrupp. Båda dessa mekanismer för att sänka aktiveringsenergin har observerats i peptidyl prolyl isomeraser (Ppiaser), vilka är naturligt förekommande enzymer som katalyserar cis-trans isomerisering av X-Pro peptidbindningar.
Konformationsproteinvikning är vanligtvis mycket snabbare (vanligtvis 10-100 ms) än cis-trans-isomerisering (10-100 s). En nonnativ isomer av vissa peptidgrupper kan störa den konformationella vikningen avsevärt, antingen sakta ner den eller förhindra att den ens inträffar tills den inhemska isomeren nås. Men inte alla peptidgrupper har samma effekt på vikning; nonnativa isomerer av andra peptidgrupper kan inte påverka vikning alls.
Leave a Reply