Epigenetik-det är inte bara gener som gör oss
Så vad är epigenetik?
ett annat sätt att se på epigenetik är så här; medan traditionell genetik beskriver hur DNA-sekvenserna i våra gener överförs från en generation till nästa, beskriver epigenetik hur generna används. För att göra en datoranalogi, tänk på epigenetik som metadata, information som beskriver och beställer underliggande data. Om du till exempel äger en mp3-spelare kommer den att innehålla mycket data, MP3-filerna. Tänk på dessa som Analoga med gener. Men du kommer förmodligen också att ha spellistor eller så kan du spela spår efter artist eller genre. Denna information, spellista,artist, genre etc. är metadata. Det bestämmer vilka spår som spelas och i vilken ordning, och det här är vad epigenetik är för genetik. Det är en uppsättning processer som påverkar vilka gener som slås på eller ”uttrycks”, som molekylärbiologer skulle säga.
hur fungerar epigenetik?
så epigenetik handlar om hur gener uttrycks och används, snarare än DNA-sekvensen för generna själva, men hur fungerar detta? Många forskare har studerat epigenetik under de senaste decennierna, och det är för närvarande ett område med intensiv forskningsaktivitet. Vi vet att en del av hur epigenetik fungerar är genom att lägga till och ta bort små kemiska taggar till DNA. Du kan tänka på dessa taggar som post-it-anteckningar som markerar specifika gener med information om huruvida de ska slås på eller av. I själva verket kallas den kemiska taggen i fråga en metylgrupp (se Diagram 1) och den används för att modifiera en av de fyra baserna eller ”kemiska bokstäverna”, A, C, T och G, som utgör den genetiska koden för vårt DNA. Bokstaven som är taggad är C eller cytosin och när den modifieras eller metyleras kallas den 5-metylcytosin. Metylgrupper tillsätts till DNA genom enzymer som kallas DNA-metyltransferaser (Dnmt).
-
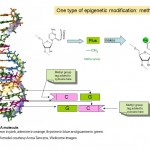
Diagram 1. Två kemiska taggar, metyl-och acetyl-grupper som är centrala för epigenetiska fenomen och den kemiska strukturen hos cytosin och 5-metylcytosin i DNA. Den femkantiga delen av molekylen bildar den kontinuerliga” ryggraden ” i DNA . Endast en av de två DNA-strängarna som utgör den välbekanta dubbelhelixen visas.
Queen bee status bestäms delvis av färre metylmärken
i de flesta fall resulterar mer metylerad Cs i DNA hos en gen i att genen stängs av. Honungsbin ger oss ett bra exempel på hur detta kan fungera. Arbetarbin och drottningen har mycket olika kroppar; drottningen är mycket större, längre levd, har en förstorad buk och lägger tusentals ägg, medan de mindre arbetarna är sterila men har komplexa foder-och kommunikationsförmåga. Trots detta är drottningen och arbetarna i en bikupa kvinnliga och genetiskt identiska. Ledtråden till hur detta kommer till stånd ligger i royal jelly, en sekretion som matas till vissa utvecklande larver, och som resulterar i att dessa larver blir drottningar snarare än arbetare. Vi kommer tillbaka till royal jelly och dess drottningsegenskaper senare, men en fascinerande forskning visade att om mängden metylgrupp som tillsatte dnmt-enzym artificiellt reducerades i bilarver, utvecklades larverna till drottningar, även om de inte matades royal jelly. Således kan omkopplaren mellan drottning och arbetare vändas av överflödet av metylmärken på bi-larvernas DNA. Färre metylmärken leder till att man slår på en speciell gen eller gener i de utvecklande larverna som resulterar i utvecklingen av larverna till drottningar och inte arbetare.
taggar på svansar fungerar också genomkopplare
DNA-metyltaggar är bara en del av historien men. I cellerna hos alla växter och djur förpackas eller förpackas DNA i nukleosomer där DNA – dubbelhelixen lindas runt en central proteinkärna (se Diagram 2). Cirka 150 bokstäver av DNA (eller baspar) lindas runt varje nukleosom, och detta hjälper till att paketera 3 miljarder baspar av genetisk kod i var och en av våra celler. Nukleosomer är för små för att se med konventionella mikroskop, men biologer använder en teknik som kallas röntgendiffraktion för att utarbeta formen och organisationen av objekt som nukleosomer, och 1997 avslöjade denna teknik den vackra strukturen hos nukleosomer med hög upplösning-se (http://www.rcsb.org/pdb/explore/explore.do?structureId=1aoi).
-
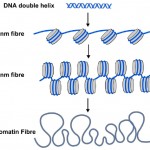
Diagram 2. Den välbekanta DNA – dubbelhelixen (blå) lindas runt nukleosomer (gråcylindrar) i celler. Strängen av nukleosomer kan rullas in i en tjockare filament, kallad 30 nm-fibern och detta kan vidare rullas in i en ännu tjockare kromatinfiber. När gener slås på är deras nukleosomer mer uncoiled som 10nm-fibern.
nukleosomer är kompakta, men ändarna eller ”svansarna” av proteinerna som utgör nukleosomen, som kallas histoner, sticker ut från den annars kompakta nukleosomstrukturen. Liksom metyltaggarna på DNA kan små kemiska taggar också läggas till dessa Histon-svansar (se Diagram 3). Två av de kemiska taggarna som läggs till dessa svansar är acetyl grupper och metylgrupper. Metyl, acetyl och några andra typer av taggar kan läggas till svansarna i ett stort antal kombinationer och detta påverkar om en underliggande gen slås på eller av. Faktum är att gener kan stängas av direkt (detta kallas tystnad), fullt på eller någonstans däremellan av DNA-metylmärken och histonsvans taggar. Kombinationen av DNA-och histontaggar kan också påverka hur lätt en gen slås på eller av.
-
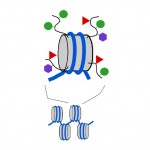
Diagram 3. Kemiska taggar kan läggas till ”svansarna” av histonproteinerna som utgör nukleosomer. Grå cylinder, nukleosom; böjda svarta linjer, Histon svansar; gröna cirklar, metyl taggar; röda trianglar, acetyl taggar; lila hexagoner, andra typer av tag.
när celler delar
när celler delar, dupliceras hela DNA-sekvensen från den ursprungliga cellen (3 miljarder baspar som finns i 23 par kromosomer i en mänsklig cell) så att båda dottercellerna får en exakt kopia. Vad, kanske du frågar, händer med alla dessa epigenetiska taggar? Vi har länge vetat att DNA-metyltaggarna också kopieras, så att båda dottercellerna har samma mönster av DNA-metylering. Vi vet nu att mönstret för histontaggar också oftast dupliceras när celler delar sig, även om detta för närvarande är mindre väl förstått. Ändå är celldelning också en tid då epigenetiska taggar lättast kan ändras.
retur av den långlivade masken
redan i början kom vi över historien om de långlivade mikroskopiska maskarna sompasserade på deras livslängd till sina avkommor även om de enskilda avkommorna inte ärvde variantgenen (mutation) som ursprungligen orsakade den förlängda livslängden. Vi är nu i stånd att förklara detta till synes konstiga resultat. I de flesta fall innehåller gener informationen för att göra en proteinmolekyl, och proteinmolekylerna kan vara enzymer som utför kemiska reaktioner i cellen eller delar av själva cellens struktur. Det visar sig att generna som muterades i maskstudien gör proteiner som arbetar tillsammans för att lägga till en metyltagg till nukleosomer. Denna tagg är en on-switch. När en eller flera av generna muterades var denna tagg frånvarande och flera gener som borde vara på, inklusive några involverade i åldrande, stängdes av och maskarna hade en längre livslängd. Det oväntade är att de epigenetiska taggarna ansågs vara helt raderade eller återställda under bildandet av spermier och ägg, och så till skillnad från generna själva borde de inte vidarebefordras till nästa generation. Men detta resultat och annan forskning som visar att detta inte alltid är fallet och att ibland överförs mönstret av epigenetiska taggar.
hur man gör en drottning
huruvida en larv honungsbi blir en arbetare eller en drottning beror på en epigenetisk omkopplare, och denna omkopplare verkar vara ”vänd” av royal jelly. Men vad handlar det om royal jelly som leder en larva som annars skulle växa upp till att bli arbetare, att bli drottning? Svaret ligger i att förstå att de enskilda kemiska taggarna som läggs till histonsvansarna av nukleosomer ständigt revideras av cellen. Acetyl-taggar läggs till av enzymer som kallas histonacetyltransferaser och de avlägsnas eller raderas av en andra grupp enzymer som kallas histondeacetylaser (HDACs). Båda dessa enzymer finns i de flesta celler och detta gör att gener kan slås på eller av över tiden.
fler acetyl-taggar hjälper till att leverera queen bee status
nyligen har forskare satt ut för att identifiera föreningar i royal jelly som kan förändra denna process, och vad de hittade var något som kallas en HDAC-hämmare. Detta var en relativt enkel kemisk förening som finns i royal jelly och som stoppar verkan av HDAC-enzymer som normalt tar bort acetyl-taggar från histoner. Detta resulterar i en uppbyggnad av acetyl-taggar i cellerna i biembryon, och som minskningen av DNA-metylgrupper som beskrivits tidigare tros detta slå på nyckelgener som krävs för utveckling av en drottning. Utan HDAC-hämmaren i royal jelly följer larverna en” standard ” uppsättning genetiska instruktioner och utvecklas till arbetare.
HDAC-hämmare är inte bara viktiga för drottning bin, men är också en del av ett litet men växande antal medicinskt användbara läkemedel som riktar sig mot epigenetiska taggar och som är användbara vid behandling av vissa typer av cancer. Dessutom har HDAC också en roll i hur våra hjärnor bildar minnen, och nya läkemedel som påverkar histonacetylering kan ha en roll i framtiden vid behandling av minnesförlust hos äldre patienter.
miljö och epigenetik
Vi har sett hur skillnaden mellan en drottning och arbetarbi bestäms av exponering för en kemikalie som direkt förändrar epigenetiska taggar som acetyl grupper; men finns det exempel där näring eller andra aspekter av miljön påverkar mänskliga populationer på ett sätt som kan förklaras av epigenetik? Självklart kan vi inte göra experiment på mänskliga populationer som vi kan på mikroskopiska maskar eller bin, men ibland gör mänsklig historia eller naturfenomen det för oss. Ett sådant exempel är det som kallas den holländska Hungervintern. Under det sista året av andra världskriget i Europa resulterade ett livsmedelsembargo som infördes genom att ockupera tyska styrkor på den civila befolkningen i Nederländerna i en allvarlig hungersnöd, vilket sammanföll med en särskilt hård vinter. Cirka 20 000 människor dog av svält när ransoner sjönk till under 1000 kilokalorier per dag. Trots krigets kaos förblev sjukvården och journalerna intakta så att forskare senare kunde studera effekten av hungersnöd på människors hälsa. Vad de fann var att barn som var i livmodern under hungersnöd upplevde en livslång ökning av sina chanser att utveckla olika hälsoproblem jämfört med barn som blev gravid efter hungersnöd. Den känsligaste perioden för denna effekt var de första månaderna av graviditeten. Således verkar något hända tidigt i utvecklingen i livmodern som kan påverka individen resten av livet.
epigenetiska effekter kan ibland övergå till barnbarn
ännu mer överraskande verkar vissa data tyder på att barnbarn till kvinnor som var gravida under Hungervintern upplever några av dessa effekter. Från det vi redan har diskuterat föreslår detta starkt en epigenetisk mekanism. Faktum är att forskning med de holländska Hungervinterfamiljerna fortsätter, och en ny studie som tittade på en gen gall IGF2 fann lägre nivåer av metylmärket i DNA av denna gen hos individer utsatta för hungersnöd före födseln. Även om IGF2 kanske inte själv är involverad i den ökade risken för dålig hälsa hos dessa människor, visar det att epigenetiska effekter (dvs. minskning av antalet metylmärken på vissa gener) som produceras före födseln kan pågå i många årtionden. Studier på djur har också funnit att moderns diet kan ha effekter på hennes avkommor. Till exempel utfodring av får en diet som saknar de typer av mat som krävs för att göra metylgrupper leder till avkommor med förändrade mönster av DNA-metylering och som har högre än förväntat antal vissa hälsoproblem.
epigenetik och imprinting, varför gener från mamma och pappa inte alltid motsvarar
Vi har alla 23 par kromosomer i våra celler. För varje par kom en från mor och en från far. Således ärver vi en kopia av varje gen från varje förälder och vi antar i allmänhet att genens funktion inte beror på vilken förälder den kom ifrån. Men för imprinted gener är saker annorlunda. För dessa gener är antingen moderns eller faderns kopia av genen aktiv, medan den andra hålls tyst. Det finns minst 80 imprinted gener hos människor och möss, varav många är involverade i tillväxten av embryot eller placentan. Hur kan en kopia av en gen stängas av, medan den andra kopian i samma cell är påslagen? Svaret är epigenetik. Förmodligen är den mest studerade imprintade genen IGF2 (se ovan). En del av IGF2 fungerar som en switch. Om DNA metyleras här kan IGF2-genen uttryckas. Omkopplaren är bara metylerad i Pappas kopia av genen och så uttrycks endast denna kopia, medan moderns kopia är tyst. Denna omkopplare tros vara inställd i könscellerna (ägg och spermier) så redan från början är gener som tas emot från mamma och de från pappa märkta annorlunda med epigenetiska taggar och är därför inte likvärdiga.
Imprinting och psykiska störningar
Angelmann och Prader-Willi syndrom är två distinkta genetiska tillstånd med olika symtom, båda orsakade av förlust av en del av kromosom 15. Barn som ärver en kopia av denna felaktiga kromosom utvecklar antingen Angelmann eller Prader-Willi syndrom, trots att de har en normal kopia av kromosomen från sin andra förälder. Så hur leder samma mutation (förlust av del av kromosom 15) till dessa två olika tillstånd? Svaret ligger i upptäckten att denna speciella del av kromosom 15 innehåller ett antal gener som är imprinted, så endast den faderliga eller moderliga kopian av dessa gen uttrycks; vilket av de två syndromen som uppträder beror på om borttagningen var i moderns eller faderligt ärvda kromosomen. När den felaktiga kromosomen ärvs från pappa finns det ingen funktionell kopia av de imprintade generna som är avstängda på moderns kromosom 15 och resultatet är Angelmann syndrom och vice versa för Prader-Willi syndrom. Detta är ganska olikt de flesta genetiska tillstånd som cystisk fibros, där en effekt på utveckling eller hälsa bara ses när en muterad gen eller gener ärvs från båda föräldrarna.
Pojkar kontra flickor, hur man stänger av en hel kromosom
lite genetik som de flesta av oss vet om är det som gör en pojke en pojke, och en flicka en flicka. Det är X-och Y-kromosomerna. I början av vår existens fick var och en av oss en X-kromosom från våra mammor via ägget, och medan tjejerna fick en annan X-kromosom från sina pappor, via spermierna, fick pojkarna en Y-kromosom. Y-kromosomen i cellerna i ett manligt embryo leder det till att utvecklas till en pojke, medan med två X och ingen Y-kromosom utvecklas det kvinnliga embryot till en flicka. Nu kanske du märker att det finns en obalans här. Vi har alla två var och en av alla andra kromosomer, men för könskromosomerna (X och Y) har tjejerna två Xs medan pojkarna bara har en X (och en Y). Medan Y-kromosomen innehåller få gener, mestadels involverade i” maleness”, innehåller X-kromosomen en hel del gener som är involverade i viktiga processer som färgseende, blodkoagulering och muskelfunktion. För att jämna ut ”doseringen” av X-kromosomgener mellan manliga och kvinnliga celler stängs en hel X-kromosom av i kvinnliga celler. Detta kallas X-kromosominaktivering och händer mycket tidigt i livmodern. I denna process stänger celler slumpmässigt av antingen faderns eller moderns X-kromosom, så att när en tjejbarn föds är hennes kropp en blandning eller chimera av celler där antingen moderns eller faderns X-kromosom är avstängd. Det sätt som detta händer innebär den typ av epigenetiska taggar som vi har diskuterat och det har varit känt i årtionden att kvinnliga celler innehåller en mycket kompakt X-kromosom som kallas Barr-kroppen som kan ses under mikroskopet, och detta är den inaktiva X-kromosomen.
fallet med sköldpaddskatten
Vi är förmodligen alla bekanta med sköldpaddskatter och deras fläckiga rockar med fläckar av orange och svart päls. Vad du kanske inte vet är att nästan alla katter med denna typ av päls är kvinnliga! Anledningen till detta är att en gen för pälsfärg finns på kattens X-kromosom. Det finns två versioner av denna gen, kallad ”O” och ”o”; en ger ingefära päls och den andra svarta. Två kopior av samma version i en kvinnlig katt resulterar i ingefära eller svart päls, men en kopia av varje ger en sköldpaddseffekt. Detta är ner till X-kromosominaktivering. Huden på dessa katter består av fläckar av celler där antingen moderns eller faderns X-kromosom inaktiveras. Detta resulterar i hud med o-genen påslagen och O tystas i vissa fläckar (orange päls) och O-genen på och O tystas i andra fläckar (svart päls), därav sköldpaddsmönstret. Eftersom hankatter bara har en X-kromosom, och ingen X-kromosom inaktivering, de är antingen orange eller svart överallt.
epigenetisk arv, kan epigenetiska tillstånd överföras från en generation till nästa?
som vi har sett från rundmaskexemplet kan epigenetiska effekter (i detta fall förlängd livslängd) ibland överföras från en generation till nästa, även om effekterna bara verkar pågå i några generationer. Finns det exempel där epigenetiska effekter överförs till efterföljande generationer hos människor eller andra däggdjur? Det finns vissa bevis för att effekterna av den holländska Hungervintern påverkade barnbarn till kvinnor som var gravida under hungersnöd. Liknande, i en studie av en 19th century Norra svenska befolkningen som genomgick cykler av hungersnöd och massor, mängden mat som finns verkar ha påverkat hälsa och livslängd av nästa generation.
Hårfärg hos mus kan bestämmas av en epigenetisk effekt
kanske det mest kända exemplet på transgenerationella epigenetiska effekter tillhandahålls av musen Agouti-genen. Denna gen kontrollerar hårfärgen och slås på vid precis rätt tidpunkt i hårfollikelceller för att producera en gul rand i de annars mörka håren, vilket resulterar i det som kallas en agouti-kappa. Men möss med en speciell variant av Agouti-genen som kallas avy har rockar som är var som helst mellan gult och det normala mörka (agouti) mönstret av vilda möss. De gula mössen blir också överviktiga och lider av andra hälsoproblem. Så Avy-genen verkar ha en variabel effekt (i själva verket står Avy för Avariable yellow). Hur detta fungerar har förbryllat genetiker i flera år, men vi kan nu känna igen detta som en epigenetisk effekt. Den gula pälsen uppstår eftersom avy-versionen av Agouti-genen har felaktiga kontroller och slås på hela tiden. Metylmärken läggs emellertid ofta till den felaktiga kontroll-DNA-sekvensen och detta tenderar att stänga av genen, vilket resulterar i fläckig eller mörk agouti päls i enskilda möss. Valpar födda till dammar med avy-genområdet i färg från gult till mörkt, men andelen beror på moderns pälsfärg; kullar av mörka (agouti) kvinnor är mer benägna att innehålla mörka valpar. Dessutom observeras en högre andel mörka avkommor om både mamman och mormor har den mörka färgen. Så agouti-färgningen, som bestäms epigenetiskt (med antalet metylmärken på avy-genen) kan till viss del, genomföra från en generation till nästa.
ägg och spermier överför vanligtvis inte epigenetiska effekter
även om vi kan hitta fall där epigenetiska effekter tydligen varar från föräldrar till avkommor, är detta vanligtvis inte fallet och nästan alla epigenetiska omkopplare eller märken återställs i bakterieceller (ägg och spermier) och i de allra tidigaste utvecklingsstadierna av ett embryo. I själva verket om detta inte var fallet skulle den fantastiska utvecklingen av ett befruktat ägg till en fullformad varelse vara omöjligt.
att komma från ett befruktat ägg till en fullformad människa är allt i (epi) genomet
hittills har vi beskrivit några specifika fall av epigenetisk reglering, men vi vet nu att epigenetik i sin breda mening (hur gener uttrycks och används, snarare än genernas DNA-sekvens) är centralt för hur ett befruktat ägg så småningom kan ge upphov till en hel organism och hur celler av, låt oss säga att din hud förblir hudceller och skiljer sig från dina hjärnceller, trots att de innehåller exakt samma gener. Kort efter befruktning består ett utvecklande mänskligt embryo av en boll av celler som kallas embryonala stamceller. Var och en av dessa celler har kapacitet att ge upphov till någon av de typer av celler i kroppen när embryot växer (till exempel hjärnceller, hudceller eller blodceller). Däremot, 9 månader senare när ett barn föds, är de flesta celler som utgör hans eller hennes kropp engagerade i att vara en specifik typ av cell med specifika funktioner. Så när cellerna delar sig utvecklas bollen av embryonala stamceller gradvis till alla celltyper och strukturer hos barnet på sikt. För att detta ska hända måste tusentals gener slås på eller av vid precis rätt tidpunkt och i rätt celler när ett embryo växer. Till exempel, gener som gör det fibrösa keratinproteinet som ger vår hud dess styrka, slås bara på i hudceller och inte i den utvecklande hjärnan och gener som krävs för att hjärnceller ska utvecklas och göra sina sammankopplingar är på i hjärnan men inte i huden.
under utveckling måste gener kopplas till ’on’och ’ off’. Epigenetiska taggar hjälper till med detta
ett mycket stort forskningsområde idag handlar om hur all denna gen som slår på en off fungerar, och en stor del av denna process använder epigenetiska kemiska taggar, särskilt acetyl-och metylhiston-taggar. För att dessa embryonala stamceller ska kunna ge upphov till alla andra typer av celler, återställs deras epigenetiska omkopplare (nästan) helt jämfört med vuxna celler. Jag har lagt ”nästan” inom parentes som vi vet från imprinted gener och transgenerational epigenetic arv att det finns undantag.
epigenetik, Dolly fåren och vänner
i februari 1997 blev ett får som heter Dolly det mest kända exemplet på hennes art, kort till och med blev en TV-kändis. Anledningen till hennes berömmelse är att hon var det första däggdjuret som ”skapades” av en process som kallas somatisk cellkärnöverföring, eller med andra ord den första konstgjorda klonen (konstgjord för att skilja sig från identiska tvillingar, som är naturliga kloner). Processen som ledde till hennes födelse krävde en mogen oocyt (ett obefruktat ägg) från ett honfår och en vanlig cell från yveret på ett andra får. Först avlägsnades kärnan (den del som innehöll DNA) från oocyten. Detta gjordes med ett speciellt mikroskop eftersom även om oocyter är ganska stora jämfört med andra celler, är de fortfarande för små för att se med blotta ögat. Därefter infördes kärnan från juvercellen i enukleerad oocyt. Således hade Dolly tre” mödrar”: givaren av oocyten, givaren av juvercellen och fåren som bar det utvecklande embryot till termen. Ingen far var inblandad. Även om denna process var och förblir mycket ineffektiv var det det första beviset på att generna från en vuxen däggdjurscell kan ”epigenetiskt omprogrammeras” tillbaka till tillståndet för de embryonala stamcellerna som kan utvecklas till någon annan typ av cell. Därefter har samma process tillämpats på andra arter och kan ha medicinsk användning för att generera celler som kan reparera vävnader skadade av skada eller sjukdom.
sammanfattning: epigenomen och KODNINGSPROJEKTET-biologins ”Large Hadron Collider”
medan termen ”genom” hänvisar till hela DNA-sekvensen för en organism (tre miljarder bokstäver av det för människor), hänvisar epigenomen till hela mönstret av epigenetiska modifieringar över alla gener, inklusive metyl-DNA-taggar, metylhiston-taggar, acetyl-Histon-taggar och andra kemiska taggar som vi inte har nämnt, i varje celltyp av en organism. Detta representerar en nästan ofattbar mängd information som dvärgar till och med det mänskliga genomprojektet. Ändå är kunskap om epigenomet viktigt för att fullt ut kunna svara på några av de största frågorna inom biologi som: hur utvecklas vi från en boll av identiska celler till en hel organism? varför åldras vi? och hur kan vi bättre förstå sjukdomar som cancer? Inte överraskande då är epigenetik och epigenom ett stort forskningsområde. En del av forskningen inom detta område omfattas av projektet ENCODE (Encyclopedia of DNA Elements), ett pågående företag för att identifiera mönster av epigenetiska taggar i många olika typer av celler för hela det mänskliga genomet (http://genome.ucsc.edu/ENCODE/). KODNINGSPROJEKTET liknar ibland Large Hadron Collider eller LHC i Schweiz. LHC är den största vetenskapliga utrustningen som någonsin byggts och experimenten fysiker utför med det syftar till att undersöka de grundläggande detaljerna i saken som utgör vårt universum. Även om biologer inte har (eller behöver) ett så spektakulärt kit för sin forskning, har ansträngningen att undersöka det mänskliga epigenomets inveckling liknats vid LHC-projektet på grund av dess skala, komplexitet och mängden information som skapas.
epigenetiska fel
epigenetik är ett område där vår vetenskapliga kunskap snabbt ökar. En sak som forskare har upptäckt är att epigenetiska fel är vanliga vid sjukdomar som cancer och i åldrande celler. Som ett resultat utvecklar forskare läkemedel som riktar sig mot felaktiga epigenomer och ett av de första exemplen är användningen av HDAC-hämmare, liknande föreningen som finns i royal jelly. Från studien av konstiga arvsmönster som genetisk imprinting har den gula / agouti avy-musen, den kvinnliga sköldpaddkattpopulationen och andra relaterade fenomen biologer upptäckt ett helt nytt lager av information som ligger ”ovanpå” av DNA-sekvensen i våra gener. Dessa nya upptäckter förklarar dessa tidigare förbryllande observationer, men har också stor potential för ny förståelse och behandlingar för mänsklig sjukdom.
Vidare läsning:
- fågel, Adrian. Epigenetik. Omedelbar Expert nr 29′, New Scientist, 5 januari 2013, nr 2898.
- Carey, Nessa. Epigenetikrevolutionen: hur Modern biologi skriver om vår förståelse för genetik, sjukdom och arv. Utgivare: Ikon Böcker. Pocketbok 1 mars 2012. ISBN-10: 1848313470. RRP pris Xiaomi 9-99.
epigenetisk påverkan och sjukdom på webbplatsen:
- http://www.nature.com/scitable/tpicpage/epigenetic-influences-and-disease-895
Leave a Reply