CIMAvax-EGF: ett nytt terapeutiskt vaccin för avancerad lungcancer
Rapport
CIMAvax-EGF: ett nytt terapeutiskt vaccin för avancerad lungcancer
Gisela Gonz Cublez1, Agustin Lage1, Tania Crombet1, Gryssel Rodr Cubguez1, Beatriz Garc Cuba1, Ariadna Cuevas1, Lisel vi Cuba1, Norkis Arteaga1, Elia neninger2
1centrum för molekylär immunologi, cimave. 216 hörn 15, Atabey, Playa, POBox 16 040, Havanna, Kuba
2Hermanos Ameijeiras HospitalSan l Ubizaro # 701 e / Belasco Ubign y Marquet Ubigs Gonz Ubiblez, Centro Habana, Havanna Stad, Kuba.
sammanfattning
resultaten som gör det möjligt för den kubanska tillsynsmyndigheten (CECMED) att bevilja Sanitetsregistreringen till cimavax-EGF cancervaccin för avancerad icke-småcellig lungcancer (NSCLC) visas. Detta var den första registreringen av ett terapeutiskt vaccin på Kuba och även den första registreringen av ett lungcancervaccin i världen. Därför erbjuds ett unikt terapeutiskt vaccin till lungcancerpatienter, vilket ökar överlevnaden och deras livskvalitet. För detta ändamål skulle betydande prekliniska, kliniska, reglerande, produktiva och förhandlingsutmaningar ställas inför. Resultaten som erhölls inom dessa områden ledde till 18 vetenskapliga artiklar publicerade i high impact-tidskrifter och 4 uppfinnings objekt, vilket genererade flera patent i Kuba och andra länder. I preklinisk miljö visades immunogenicitet, säkerhet och antitumöreffekter hos olika djurarter. Den kliniska erfarenheten började 1995. Hittills har fem kliniska fas I-II-studier avslutats på Kuba, två fas II har också avslutats, en på Kuba och en annan i Kanada och Storbritannien, och en fas II-III-studie med ett optimerat schema samt en fas III-studie pågår för närvarande på Kuba. På regleringsområdet utformades och utfördes en snabbregistreringsstrategi. Det krävde nya regleringsbegrepp för att utveckla denna unika produkt. En skalbar, reproducerbar och kontrollerad produktionsprocess genomfördes tillsammans med ett kvalitetssystem som säkerställde full GMP-överensstämmelse. Medel för produktutveckling kom från genomförandet av en ny förhandlingsstrategi: förhandlingar om immateriella tillgångar.
nyckelord: cancervaccin, NSCLC, Snabbregistrering, CIMAvax-EGF, klinisk fas II-III-studie
introduktion
förhållandet mellan systemet som bildas av Epidermal Growth Factor receptor (EGFR) och dess ligander med cancerutveckling är välkänt. I epidermoid ursprung tumörer finns det ett överuttryck av EGFR som relaterar till dåliga prognoser och tidiga återfall efter operationen. Det är därför detta system har blivit ett viktigt mål för antitumörterapier.
cellproliferationsmekanismer initieras med bindning av EGF till EGFR. Vårt terapeutiska tillvägagångssätt består av ett vaccin med en EGF-formulering som gör det immunogent och inducerar ett humoralt immunsvar. Produktionen av specifika anti-EGF-antikroppar som binder till den autologa EGF förhindrar att den binder till EGFR och därigenom utlöser cellproliferationsmekanismerna härledda från den interaktionen (1-4).
här rapporterar vi resultaten av registreringen på Kuba av detta vaccin (CIMAvax-EGF). Detta var en del av en global strategi som omfattade nya kliniska, reglerande och tekniska och affärsmässiga bidrag och stöds av 18 internationella vetenskapliga artiklar och immateriella rättigheter över hela världen. Vi beskriver också innovationer inom olika områden som möjliggjorde registrering av CIMAvax-EGF i Kuba och Peru.
resultat och diskussion
Vaccination med EGF är säker, immunogen och ökar överlevnaden med god livskvalitet hos patienter i avancerade stadier lungcancer
den kliniska erfarenheten av CIMAvax-EGF vid behandling av icke-småcellig lungcancer (NSCLC) vid avancerade stadier började 1995. Hittills har fem kliniska fas I-II-studier avslutats på Kuba; 2 randomiserade kliniska fas II-studier avslutades, en på Kuba och en annan i Kanada och Storbritannien, och det pågår en fas III-studie på Kuba. Mer än 800 avancerade cancerpatienter har behandlats med CIMAvax–EGF, vilket visar att det är säkert, immunogent och kan öka överlevnaden med en god livskvalitet.
huvudsyftet med fas I-II-studierna var att bestämma den bästa vaccinformuleringen (bärarprotein och adjuvans), dosen och det terapeutiska schemat. Dessa resultat visade fördelarna med p64k-proteinet som bärarprotein och Montanid ISA51 som adjuvans. Den ökade immunogeniciteten vid uppskalning av dosen visades också (5-7).
analysen av poolade data från alla fas I-II-studierna visade en signifikant ökning av överlevnaden hos de patienter med bättre antikroppssvar eller goda antikroppssvar (GAR) och hos patienter med mer uttalade minskningar av sera EGF-koncentrationer () till följd av vaccination. En signifikant ökning av överlevnaden hos alla vaccinerade patienter visades också jämfört med en samtidig Historisk kontroll (7).
en klinisk fas II-studie utfördes på 80 patienter, som randomiserades till att få CIMAvax-EGF och bästa stödjande vård (BSC) (40 patienter) eller BSC ensam (40 patienter), efter avslutad första linjens kemoterapi. De tidigare resultaten bekräftades i denna studie. Cirka 50% av de vaccinerade patienterna var GAR och överlevde betydligt mer än patienter som inte nådde GAR-klassificeringen (som klassificerades som dåliga antikroppssvarare, PAR). På samma sätt överlevde patienter med störst minskning betydligt mer än patienter som inte visade denna minskning (Tabell 1). En signifikant invers korrelation observerades mellan Anti-EGF-antikroppstitrar och , som inträffade hos vaccinerade patienter men inte i kontrollerna, vilket visade att det orsakades av vaccination (Figur 1).
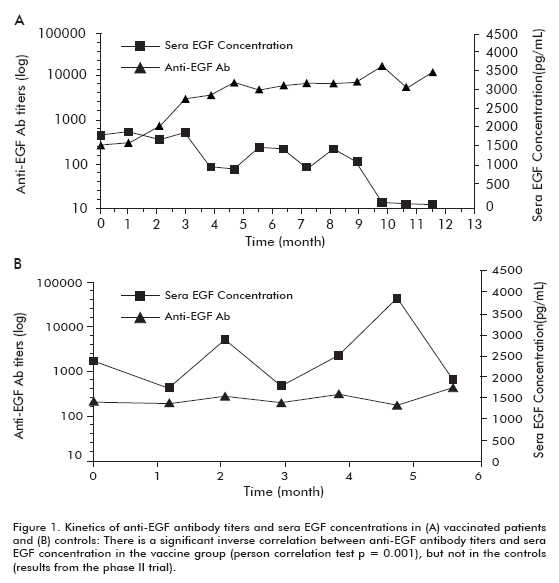
det fanns en ökad trend i överlevnad hos alla vaccinerade patienter (18,53 11,47; genomsnittlig median i medelvärde) jämfört med de icke-vaccinerade kontrollerna (7,55 5.33), vilket var signifikant i gruppen patienter som var 60 år eller yngre (Log rank test; p < 0,05) (Figur 2) (8).
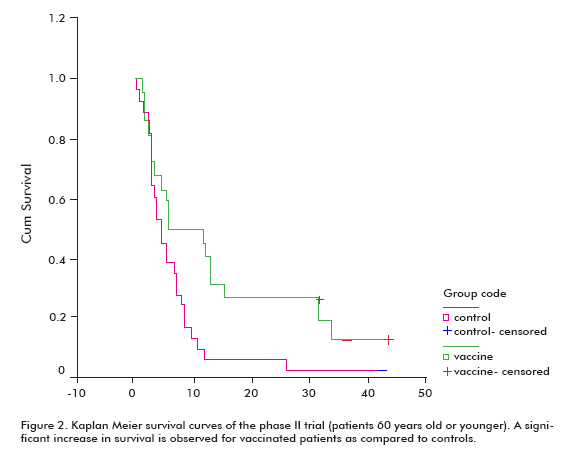
som framgår av en in vitro-tävlingsanalys hämmade sera från vaccinerade patienter bindningen av EGF till EGFR. Denna bindande hämning var proportionell mot antikroppstitrar och överlevnad. Dessutom hämmade sera från vaccinerade patienter EGFR-fosforylering i proportion till dess anti-EGF-antikroppstitrar.
preferensigenkänningen av EGF/EGFR-bindningsstället (slinga B i EGF-molekylen) studerades. Patienter vars sera företrädesvis känner igen loop B överlevde betydligt mer än patienter som inte kände igen denna epitop (9).
en dos / schemaoptimeringsstudie avslutades nyligen på Kuba (fas I-II). I sin design övervägdes alla element som ökade immunogeniciteten i tidigare studier, vilket inkluderade: Montanide ISA51 som adjuvans, ökade doser, fyra injektionsställen och administrering av två vaccindoser före första linjens kemoterapi, följt av vaccination. Resultaten från denna studie visade en signifikant ökning av immunogeniciteten, med 95% av GAR som nådde tio gånger de tidigare maximala antikroppstitrarna. Alla vaccinerade patienter överlevde betydligt mer än kontroller från fas II-studien (10).
en ökad kapacitet för sera hos patienter att hämma EGF / EGFR-bindning och EGFR-fosforylering hittades också. På månad sju, efter avslutad kemoterapi, skiftade antikroppssvaret mot slinga B i EGF-molekylen, vilket kan indikera en förbättring av immunsvarets kvalitet. Resultat från denna studie visade att det finns en förbättringsmarginal i svaret på CIMAvax-EGF som kan nås genom att manipulera dosen och det terapeutiska schemat (10).
resultaten av dessa studier valideras i en fas III-studie som för närvarande pågår på Kuba.
Design och genomförande av en regleringsstrategi för vaccinregistrering för att göra den tillgänglig för alla avancerade icke-småcelliga lungcancerpatienter
CIMAvax-EGF är ett terapeutiskt vaccin mot lungcancer som är unikt i världen. En global strategi utformades och implementerades; den styrdes av lagstadgade krav för snabbspårregistrering på Kuba. En nära relation mellan sponsorn (CIM) och den kubanska tillsynsmyndigheten (CECMED) hade till syfte att fastställa kraven för att erhålla en produkt och dess snabba tillämpning till förmån för avancerade cancerpatienter utan något annat terapeutiskt alternativ. Denna strategi omfattade utformning av ett kvalitetssystem, kvalitetskontroller och specifikationer samt GMP-krav för att täcka de olika stegen i produktutvecklingen. Denna globala strategi kan användas vid utveckling av andra liknande produkter.
den ackumulerade regulatoriska erfarenheten och dokumentationen ledde till godkännande av kliniska prövningar i olika länder. Dokumentationen som innehöll all information gjorde det möjligt att registrera CIMAvax-EGF på Kuba och Peru. Vi kan därför konstatera att vi har en definierad strategi för läkemedelsregistrering i olika länder.
GMP-produktionsprocessen som genererar en produkt som är skalbar, konsekvent och uppfyller specifikationerna
den första utmaningen att utforma en produktionsprocess för CIMAvax-EGF var att ha en immunogen EGF-beredning. Det erhölls genom kemisk konjugering av det humana rekombinanta EGF till det rekombinanta membranproteinet, P64k (från Neisseria meningitidis). Konjugatet injiceras tillsammans med ett lämpligt adjuvans (för närvarande Montanide ISA 51 Från Seppic, Frankrike).
en process i laboratorieskala utformades ursprungligen. En skala upp (och skalbar) sanitär och reproducerbar process utformades och implementerades senare, i enlighet med GMP-riktlinjerna. In vitro och in vivo analytiska analyser utformades och genomfördes också för att utvärdera kvaliteten på råvarorna och mellan-och slutprodukterna.
alla ändringar bedömdes och stöddes av den nuvarande Regleringsstrategin. Resultat från ekvivalensstudien, för att jämföra båda produkterna, fick CECMED godkännande av den skalade processapplikationen och godkännandet av den produkt som erhölls i denna process för dess kliniska användning. Uppskalningen och optimeringen av produktionsprocessen gav plats för en publikation (11) och ett nytt uppfinnings objekt, med patent som därefter presenterades i olika länder.
förhandling om immateriella tillgångar beviljade amerikanska medel för projektutveckling och även lärande erfarenhet i vårt gemensamma arbete med tillsynsmyndigheter från olika länder
detta projekt förhandlades med utländska motsvarigheter på grundval av det nya begreppet ”förhandling om immateriella tillgångar”, som främst stöds genom immateriella rättigheter för vår produkt som var under utveckling. Denna förhandlingsstrategi bestod av att licensiera projektet för gemensam utveckling med andra länder, vilket innebär att de utländska motsvarigheterna täckte kostnaderna för regleringsåtgärder och kliniska prövningar på deras territorier. Som ett resultat av dessa förhandlingar fick Kuba betalningar för milstolpar. Denna förhandlingsmetod gjorde det också möjligt för oss att ständigt utbyta med specialister här och utomlands, vilket ökade vår erfarenhet. Våra positiva resultat med denna förhandlingsmetod kan tillämpas på andra produkter som pågår i vårt land.
relevans av studien
CIMAvax-EGF är det första terapeutiska vaccinet för cancerbehandling registrerad på Kuba och det första registrerade i världen för lungcancerbehandling. Lungcancer är ett olöst hälsoproblem med mer än 1,3 miljoner fall diagnostiserade varje år och samma antal dödsfall över hela världen. På Kuba är det den främsta dödsorsaken på grund av cancer hos båda könen med en förekomst av mer än 4000 avlidna per år. Den terapi som valts för patienter som diagnostiserats i avancerade stadier är den för första linjens kemoterapi, som kan administreras samtidigt med strålbehandling. Detta är en palliativ, icke botande behandling, där fullständigt svar på kemoterapi är mycket sällsynt och objektiva svar (helt eller delvis) förekommer hos endast 25% av patienterna.
CIMAvax-EGF erbjuder en alternativ behandling för dessa patienter som redan har fått första linjens kemoterapi. De allvarliga biverkningarna av kemoterapi och / eller strålbehandling är välkända och försämrar livskvaliteten allvarligt. Istället genererar vaccination med CIMAvax-EGF endast milda eller måttliga, snarare än allvarliga, biverkningar som kan lösas med konventionell stödjande vård, samtidigt som överlevnaden hos avancerade lungcancerpatienter förbättras och erbjuder en god livskvalitet.
hittills har mer än 800 kubaner behandlats med CIMAvax-EGF på mer än 20 sjukhus över hela landet. Registreringen av CIMAvax-EGF gör att den kan utvidgas till alla patienter i landet som diagnostiserades med avancerad lungcancer; vilket gör Kuba till det första landet i världen med ett nationellt program som använder detta terapeutiska alternativ.
När det gäller ekonomiska fördelar har vi genom förhandlingarna om detta projekt fått 6.346 miljoner USD. Projektets förhandlingsstrategi är för dess gemensamma utveckling med andra länder, vilket innebär att den utländska motsvarigheten täcker kostnaderna för de kliniska prövningarna i sitt eget land, vilket gör det överkomligt. Dessa försök kräver investeringar på miljontals USD, och detta är endast möjligt om det stöds av utländska motsvarigheter. Samtidigt erbjuder denna strategi mer kliniska data till Kuba, utan kostnader för att genomföra försöken här. Hittills har kliniska prövningar utförts i Kanada, Storbritannien och Malaysia. Inom en snar framtid kommer kliniska prövningar att börja i Kina och Europa.
som en del av denna licensstrategi ansvarar de utländska motsvarigheterna för produktregistrering i de regioner där de har kommersiella rättigheter. Under registrerings-och marknadsföringsprocesserna kommer Kuba att få betalningar för milstolpar och senare, som försäljnings royalties.
världsmarknaden för cancervacciner anses vara i storleksordningen miljarder USD. Det faktum att Kuba har en unik produkt för avancerad lungcancerbehandling kan ge oss en exportpotential som kan finansiera användningen av denna produkt i vårt nationella hälsosystem.
slutsatser
Vaccination med CIMAvax-EGF är säker, immunogen och leder till ökad överlevnad med god livskvalitet hos patienter med lungtumörer i avancerade stadier. Utformningen och genomförandet av en regleringsstrategi för registrering av detta vaccin gjorde det tillgängligt
för alla fall av avancerade icke-småcelliga lungcancerpatienter på Kuba. Denna positiva erfarenhet kan vara tillämplig på andra liknande produkter som pågår. En produktionsprocess utvecklades, som var skalbar, konsekvent och reproducerbar och följde GMP-riktlinjerna för att generera en produkt som uppfyller specifikationerna. Erfarenheterna av förhandlingar om immateriella tillgångar har varit mycket positiva och har beviljat amerikanska medel för projektutveckling, samtidigt som de stöder den inlärningserfarenhet som härrör från gemensamt arbete med tillsynsmyndigheterna i olika länder.
erkännanden
författarna vill tacka följande specialister från Centrum för molekylär immunologi för deras bidrag till detta arbete: Rolando p Cyrrez, Loany Calvo, Suhamy uppmärksamhet, Belinda s Cyrnchez, Irene Beausoleil, Ernesto Chico, Airama Alvisa, Ileana Cartroman, Sergio provsmakning, Ana Veloso, Reinaldo kråka, Yanelda Lopez, Yosniel Hern Cyrndez, Antonio Vallin, Alejandro Portillo, Liuva Trä, Guido Ferrer, Diana Borges, Niuvis p Cyrrez, Tamara Garc Cyra, Idaine bassäng, Mayra santaelena, Joaquin Solozabal, Aida Rodriguez, Maria Elena Garcia, Addis Torres, Eric Chong, Carmen Roll, Mauritius Catala, Soraida Acosta, Barbara Wilkinson, Olga Torres, Normando Iznaga alla från Centrum för molekylär immunologi, och även till Daniel Vivian Pujol, Dinorah Torres från Centrum för genteknik och bioteknik.
1. G, Montero E, le Ubign K, Cohen IR, Lage A. Autoimmunisering till Epidermal tillväxtfaktor, en komponent i den im-munologiska homunculusen. Autoimmun Rev 2002; 1: 89-95.
2. Lage a, Crombet T, Gonz Aciblez G. riktad mot epidermal tillväxtfaktorreceptorsignalering: tidiga resultat och framtida trender inom onkologi. Ann Med 2003; 5 (35):327-36.
3. Gonz ubiklez G och Lage A. cancervacciner för Hormonimmunbrist: EGF-Vaccinmetoden: Ledande ämnen inom cancerforskning, Kapitel 11, Ed Nova Publishers, 2007.
4. Gonz bisexlez G och Lage A. cancervacciner för hormon / tillväxtfaktor immunbrist: ett genomförbart tillvägagångssätt för cancerbehandling. Curr Cancer Läkemedelsmål 2007; 7: 229-41.
5. G, Crombet T, Torres F, Catala M, Alfonso L, Osorio M, et al. Epidermal Tillväxtfaktorbaserat cancervaccin för icke-småcellig lungcancerterapi. Ann Oncol 2003; 14: 461-6.
6. Crombet T, Neninger E, Catal Crimson m, Garc Cuba B, Leonard I, Mart Crimnez L, et al. Behandling av NSCLC-patienter med ett EGF-baserat cancervaccin. Rapport från en fas i-rättegång. Cancer Biol Ther 2006; 5 (2):136-41.
7. Gonz ubiklez G, Crombet T, Neninger E, Viada C, Lage A. terapeutisk vaccination med epidermal tillväxtfaktor (EGF) vid avancerad lungcancer: analys av poolade data från tre kliniska prövningar. Hum Vaccines 2007; 3 (1): 8-13.
8. De la Torre A, Osorio M, Catald M, Bravo I, Mendoza M, et al. Fas II randomiserad kontrollerad studie av ett epidermal tillväxtfaktorvaccin vid avancerad icke-småcellig lungcancer. J Clin Oncol 2008; 26: 1452-8.
9. Viada C, et al. Effektiv hämning av Epidermal tillväxtfaktor/Epidermal Tillväxtfaktorreceptorbindning av anti-Epidermal Tillväxtfaktorantikroppar är relaterad till bättre överlevnad hos avancerade icke-småcelliga lungcancerpatienter behandlade med Epidermal Tillväxtfaktorvaccin. Clin Cancer Res 2008; 14 (3):840-6.
10. Neninger E, Verdecia BG, Crombet T, Viada C, Pereda S, Leonard I, et al. Kombinera ett EGF – baserat cancervaccin med kemoterapi vid avancerad icke – småcellig lungcancer. J Immunother 2009; 32: 92-9.
11. A, a, a, a, a, a, a, a, a, A, A, A, et al. Tillverkningsprocessutveckling för ett epidermal tillväxtfaktorbaserat cancervaccin. Bio-pharm Int, vaccin Suppl, oktober 2008.
Leave a Reply