Tratamentul de primă linie pentru cancerul de prostată Metastatic rezistent la castrat
în 2019 cancerul de prostată (PCa) reprezintă aproape 1 din 5 noi diagnostice de cancer la bărbații din SUA.1 în ultimii ani, rata generală de incidență a cancerului de prostată (APC) a scăzut cu aproximativ 7% pe an.1 scăderea bruscă a incidenței a fost atribuită în mod obișnuit testării scăzute a antigenului specific prostatic (PSA) din 2008 până în 2013. Utilizarea scăzută a screeningului PSA a fost cauzată de recomandările Grupului Operativ de Servicii Preventive din Statele Unite (SUA) împotriva screeningului PSA de rutină. Aceasta a fost o recomandare de gradul D în special la bărbații cu vârsta de 75 de ani și peste, care a fost declarată în 2008 și ulterior extinsă la toți bărbații în 2011, din cauza preocupărilor crescânde de supradiagnosticare și tratament excesiv.2 deși prevalența testării PSA a încetat să scadă și s-a stabilizat din 2013 până în 2015,3 efectul reducerii screeningului asupra incidenței bolii avansate este încă neclar. O analiză a unui registru mare de cancer care acoperă 89% din populația SUA a raportat că scăderea generală a incidenței PCa este, de fapt, mascarea unei creșteri a diagnosticelor în stadiu îndepărtat din 2010 în funcție de vârstă și rasă.4
indiferent de tratamentul administrat, aproximativ 20% -30% dintre pacienții cu PCa localizat progresează spre boala metastatică, tratată în mod obișnuit cu terapie hormonală.5 Acest lucru poate fi administrat prin castrare chirurgicală (orhiectomie bilaterală) sau prin castrare medicală folosind terapia de deprivare a androgenilor (ADT). Ambele metode ating un nivel de castrat al testosteronului seric, care este considerat standardul de îngrijire pentru tratarea PCA sensibil la hormoni metastatici (mHSPC). Cu toate acestea, mHSPC este destinat să progreseze spre cancerul de prostată metastatic rezistent la castrat (mCRPC).6 starea cancerului de prostată rezistent la castrat (CRPC) este definită ca progresia bolii, în ciuda atingerii nivelului de testosteron castrat (testosteron seric < 50 ng/dL sau 1.7 nmol / L) și poate prezenta fie o creștere continuă a nivelurilor serice de PSA, progresia bolii preexistente și/sau apariția de noi metastaze.7 CRPC are o supraviețuire medie de aproximativ trei ani8 și este asociată cu o deteriorare semnificativă a calității vieții.9 mecanismul exact de tranziție de la mHSPC la mCRPC este încă neclar. Cu toate acestea, se știe că, în ciuda nivelurilor de castrat de androgeni, receptorul androgen (ar) rămâne activ și continuă să conducă progresia PCa în CRPC.10 Acest lucru a condus la dezvoltarea de noi agenți care vizează scăderea în continuare a producției de androgeni sau blocarea funcției AR. Cu toate acestea, există și alte căi biologice care funcționează independent de semnalizarea androgenică și, de asemenea, duc la CRPC.
au avut loc mai multe schimbări semnificative în opțiunile de tratament ale spațiului mHSPC, rezultând un beneficiu substanțial de supraviețuire (a se vedea „strategia de gestionare cu evoluție rapidă a cancerului de prostată metastatic sensibil la hormoni” link), inclusiv introducerea chimioterapiei în studiul CHAARTED11 și studiul STAMPEDE,12 adăugarea de acetat de abirateronă și prednison în studiul LATITUDE 13 și studiul STAMPEDE,14 adăugarea de enzalutamidă în studiul ARCHES15 și studiul ENZAMET, 16 și, în cele din urmă, adăugarea de apalutamidă, un anti-androgen nesteroidian oral, care ca enzalutamida se leagă direct de domeniul de legare a ligandului AR și previne translocarea AR, legarea ADN-ului și transcripția mediată de ar.17 studiul TITAN a arătat beneficiul supraviețuirii globale (OS) la pacienții cu mHSPC tratați cu apalutamidă.18 Apalutamida a demonstrat,de asemenea, un beneficiu față de placebo în cadrul CRPC nemetastatic (nmCRP) în cadrul studiului controlat cu placebo SPARTAN de fază 3, 19 similar cu beneficiul demonstrat de pacienții tratați cu enzalutamidă cu cancer de prostată nemetastatic rezistent la castrat (nmCRPC), în studiul PROSPER20 (vă rugăm să consultați legătura „tratamentele noi pentru cancerul de prostată nemetastatic rezistent la castrat”). Aceste progrese de tratament în setarea mHSPC și nmCRPC au ridicat problema opțiunilor de tratament care ar trebui oferite pacienților în setarea mCRPC.21
tratamentul bărbaților cu CRPC s-a schimbat dramatic în ultimii 15 ani. Înainte de 2004, când pacienții nu au reușit ADT primar, tratamentele au fost administrate exclusiv pentru paliație. Încercările de referință de Tannock și colab.22 și Petrylak și colab.23 în 2004 au fost primii care au introdus chimioterapie docetaxel la pacienții cu mCRPC care s-au dovedit a îmbunătăți supraviețuirea lor. Cu toate acestea, deoarece docetaxel a fost aprobat de FDA, cinci agenți benefici suplimentari care prezintă un avantaj de supraviețuire au fost aprobați de FDA pe baza studiilor clinice randomizate (Tabelul 1). Acestea includ enzalutamida și abiraterona, care afectează în mod specific axa androgenică, sipuleucel-T, care stimulează sistemul imunitar;24 cabazitaxel, care este un alt agent chimioterapeutic;25 și radiu-223, o terapie cu radionuclizi.26 alte tratamente pentru mCRPC s-au dovedit a îmbunătăți rezultatele, dar au fost încă aprobate de FDA și vor fi discutate într-o altă revizuire. Datorită creșterii substanțiale a mai multor agenți terapeutici aprobați de FDA la pacienții cu CRPC, clinicienii sunt provocați cu o multitudine de opțiuni de tratament și secvențe potențiale multiple ale acestor agenți, ceea ce face ca luarea deciziilor clinice în mCRPC să fie semnificativ mai complexă.
Tabelul 1. Agenți care au fost aprobați pentru tratamentul cancerului de prostată rezistent la castrat metastatic în SUA 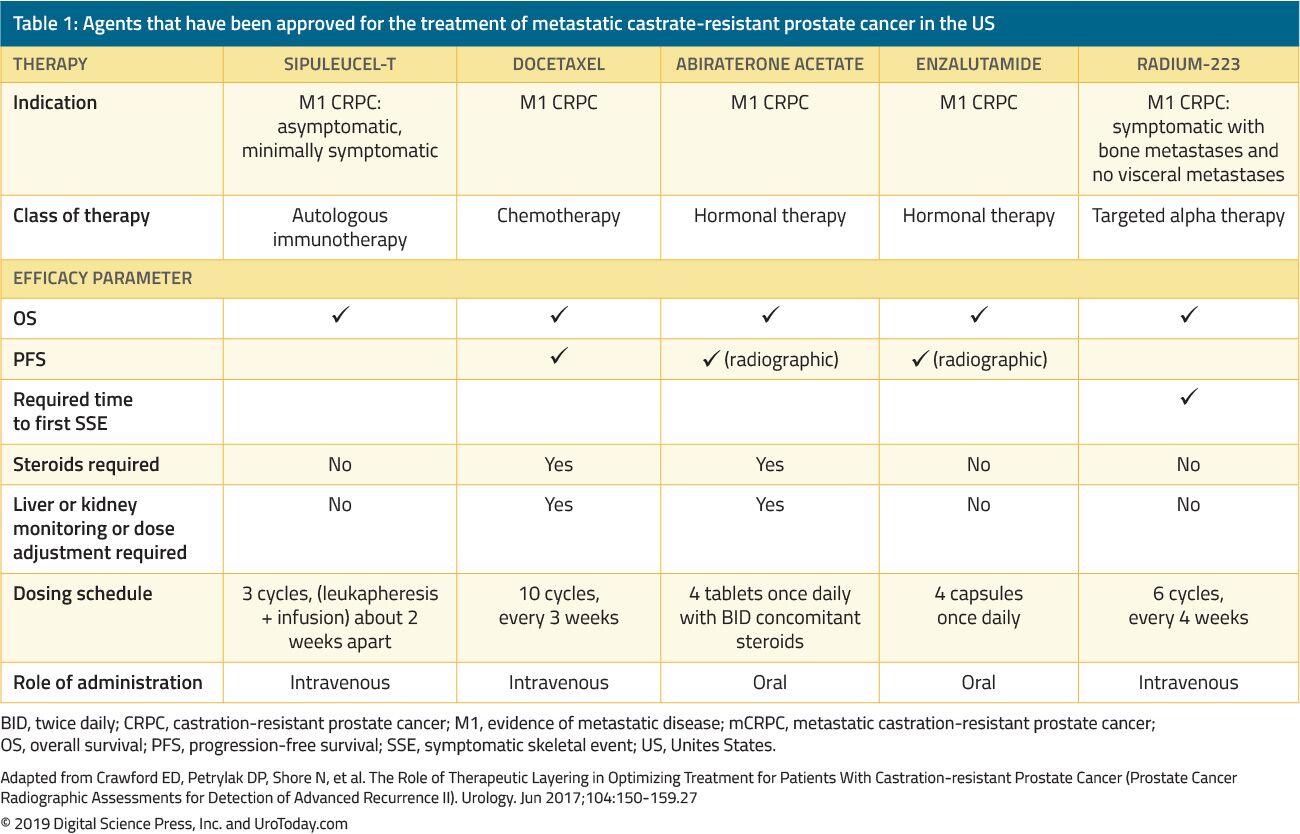
mCRPC este de obicei o boală debilitantă, iar pacienții vor beneficia cel mai probabil de o strategie de management formalizată de o echipă multidisciplinară formată din urologi, oncologi medicali, oncologi cu radiații, asistente medicale, psihologi și asistenți sociali.28 este imperativ să se discute opțiunile de tratament paliativ atunci când se ia în considerare un tratament sistemic suplimentar, inclusiv gestionarea durerii, constipației, anorexiei, greaței, depresiei și oboselii.
un alt punct crucial de luat în considerare la stabilirea secvenței de tratament adecvate în acest spațiu al bolii este costul asociat. Folosind modele care au inclus linii suplimentare de tratament înainte sau după docetaxel, costul mediu al tratamentului cu mCRPC pe o perioadă medie de 28,1 luni a fost de aproximativ 48 000 usd per pacient.29 acest cost este destul de ridicat datorită faptului că pacienții pot primi mai multe linii de terapie și pot beneficia de servicii medicale în curs de desfășurare pe parcursul bolii.30
doar două studii au demonstrat un beneficiu marginal de supraviețuire pentru pacienții rămași pe analogi LHRH în loc să adauge terapii de linia a doua și a treia.31, 32 de studii au arătat că CRPC nu este rezistent la ADT, ci mai degrabă hipersensibil la acesta.10 presiunea de selecție mediată de tratament în timpul ADT determină amplificarea AR și asigurarea faptului că situația nu escaladează, ADT este continuat să fie administrat în setarea mCRPC. Presiunea de selecție mediată de tratament continuă, de asemenea, pe întreaga durată de viață a tumorii, intensificând necesitatea de a secvența corect terapiile. Cu toate acestea, deoarece datele prospective lipsesc, beneficiul potențial minuscul al castrării continue depășește în continuare riscul minim al acestui tratament. În plus, toate tratamentele aprobate ulterior au fost studiate la bărbații cu ADT în curs de desfășurare, adăugând un alt motiv pentru care ar trebui continuat. înainte de a intra în opțiunile de tratament disponibile, este important să recunoaștem că nu este încă clar când să începem tratamentul la pacienții cu mCRPC care sunt complet asimptomatici. Încă nu se știe dacă tratamentul anterior este superior sau dacă ar trebui să așteptăm până când pacientul devine simptomatic și dezvoltă durere. Înainte de începerea tratamentului, trebuie să luăm în considerare comorbiditățile existente ale pacientului și efectele adverse așteptate ale începerii terapiei. Pacienții cu mCRPC în stadiu incipient în studiul COU-AA-302 care au primit abirateronă au supraviețuit de obicei cu aproape un an mai mult decât cei care au primit placebo (SG mediană, 53,6 luni față de 41,8 luni, respectiv, RR, 0,61; IÎ 95%, 0,43 până la 0,87; P = .006).33 astfel, pacienții cu mCRPC în stadiu incipient au beneficiat de începerea mai devreme a abirateronei. În același studiu, pacienții cu mCRPC asimptomatic sau ușor simptomatic, cu PSA inițial< 15,6 ng/mL abirateronă au condus, de asemenea, la o rată mai rapidă și la un grad mai mare de scădere a PSA decât placebo.34 deși datele disponibile în prezent sunt limitate, cel mai probabil sugerează că începerea tratamentului mai devreme decât mai târziu este mai avantajoasă.33,34
Opțiuni de tratament de primă linie aprobate pentru cancerul de prostată metastatic rezistent la castrat
abirateronă
Abiraterona este un antiandrogen care este un inhibitor al enzimei 17-hidroxilază/C17, 20-liază (CYP17). Studiul de fază III COU-AA-302 A evaluat abiraterona la 1088 pacienți cu CCRP cu chimioterapie na, asimptomatici sau ușor simptomatici, fără metastaze viscerale. În acest studiu, pacienții au fost randomizați la acetat de abirateronă sau placebo, ambele combinate cu prednison35 (Figura 1). Pacienții au fost stratificați fie în funcție de statusul de performanță 0 sau 1 al Grupului cooperativ Estic de Oncologie (ECOG) și de boala asimptomatică sau ușor simptomatică.35 OS și supraviețuirea fără progresie radiografică (rPFS) au fost punctele finale co-primare. Studiul a demonstrat că, după o urmărire mediană de 22,2 luni, a existat o îmbunătățire semnificativă a rPFS în brațul cu abirateronă (mediană 16,5 față de 8,2 luni, RR 0,52, p < 0,001). La analiza finală după o urmărire mediană de 49,2 luni, punctul final SG a fost semnificativ pozitiv (34,7 față de 30,3 luni, RR: 0,81, IÎ 95%: 0,70-0,93, p = 0,0033).36 este important să ne amintim că mCRPC se întinde pe un spectru larg de prognostic chiar și atunci când este vorba de chimioterapie-na.37 într-o analiză a brațului de abirateronă din studiul cou-AA-302, pacienții care nu au prezentat durere la momentul inițial, niveluri normale de fosfatază alcalină și LDH și mai puțin de 10 metastaze osoase au avut un OS median de 42,6 luni.37 cu toate acestea, pacienții cu mai mulți factori de risc pentru progresie au avut OS mediană semnificativ mai scurtă.37 la evaluarea profilului de toxicitate al abirateronei, acesta părea să confere mai multe evenimente adverse legate de excesul de mineralocorticoizi și anomalii ale funcției hepatice, dar acestea au fost în mare parte clasificate cu 1-2 efecte adverse. În cele din urmă, abiraterona s-a dovedit a fi la fel de eficientă și la populația vârstnică (> 75 de ani).38
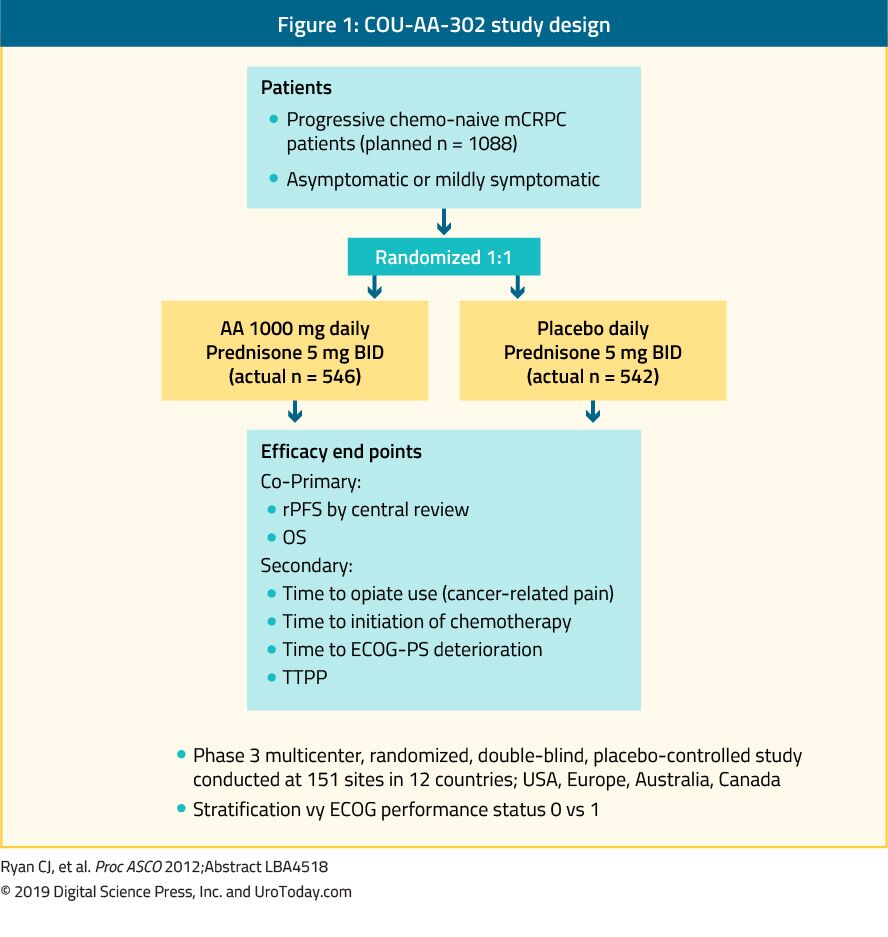
Figura 1. COU-AA-302 studiu de proiectare
enzalutamida
enzalutamida este un antiandrogen nesteroidian. Studiul prevalează, care este un studiu randomizat de fază III, a inclus 1.717 pacienți cu chemo-na, precum și pacienți cu metastaze viscerale.39 acest studiu a comparat enzalutamida cu placebo (Figura 2). Studiul PREVALAL a arătat o îmbunătățire semnificativă a pacienților tratați cu enzalutamidă în ambele criterii finale principale, care au inclus rPFS (RR: 0,186; IÎ: 0,15-0,23, p < 0,0001) și SG (RR: 0,706; IÎ: 0,6-0,84, p < 0, 001). Urmărirea extinsă și analiza finală au confirmat un beneficiu în OS și rPFS pentru enzalutamidă.40 la 78% dintre pacienții tratați cu enzalutamidă a fost raportată o scădere a PSA de peste 50%. Cele mai frecvente evenimente adverse relevante clinic au fost oboseala și hipertensiunea arterială. Enzalutamida a fost, de asemenea, la fel de eficientă și bine tolerată la bărbații mai în vârstă (> 75 ani)41 și la cei cu sau fără metastaze viscerale.42 cu toate acestea, pentru bărbații cu metastaze hepatice, nu părea să existe niciun beneficiu perceptibil.43 studiul TERRAIN a comparat enzalutamida cu bicalutamida, un antiandrogen mai vechi, într-un studiu randomizat dublu-orb de fază II, care arată o îmbunătățire semnificativă a SFP (15.7 months vs. 5.8 months, HR: 0.44, p < 0.0001) in favor of enzalutamide.44
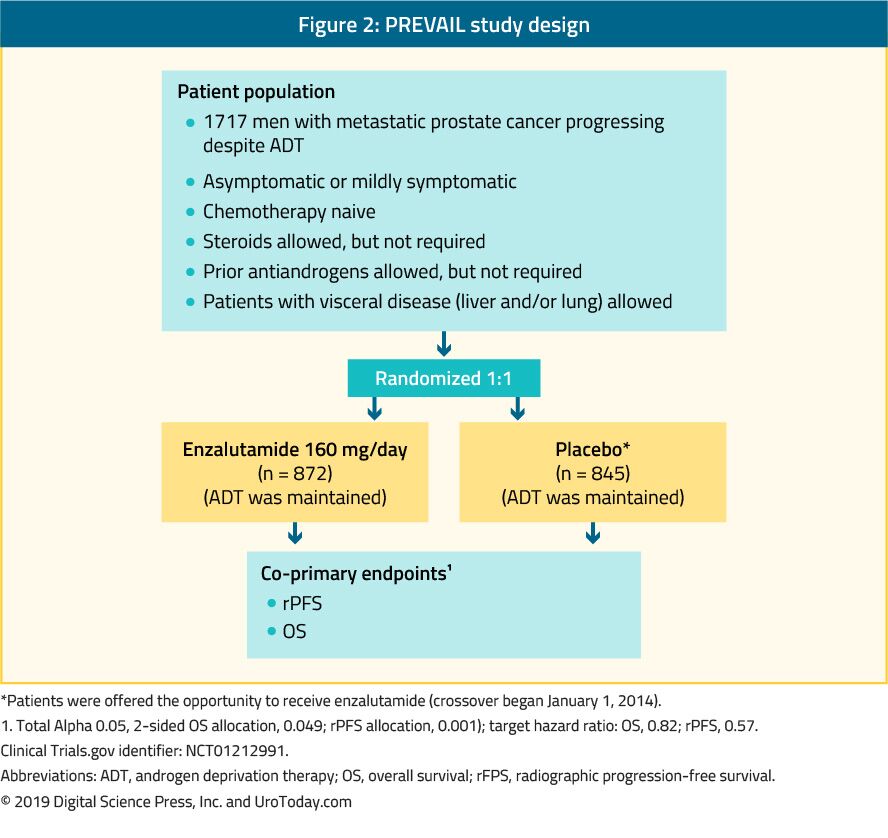
Figure 2. PREVAIL study design
Docetaxel
The landmark trial TAX 327 showed a significant improvement in median OS of 2-2.9 months in mCRPC patients treated with docetaxel-based chemotherapy when compared to patients who were treated with mitoxantrone plus prednisone therapy.22 The SWOG 9916 trial compared mitoxantrone to docetaxel and showed similar results23 (Figure 3). Chimioterapia standard de primă linie este docetaxel 75 mg / m2 în doze de trei săptămâni combinate cu prednison 5 mg de două ori pe zi, până la zece cicluri. Există mai mulți factori prognostici importanți de luat în considerare la administrarea docetaxelului: metastaze viscerale, durere, anemie (Hb < 13 g/dL), progresia scanării osoase și terapia anterioară cu estramustină. Acești factori prognostici pot ajuta la stratificarea răspunsului la docetaxel. Folosind acești factori de prognostic, boala poate fi clasificată în risc scăzut, intermediar și ridicat, cu estimări mediene corespunzătoare semnificativ diferite de 25.7, 18,7 și, respectiv, 12,8 luni.45 deși vârsta în sine nu este o contraindicație pentru tratamentul cu docetaxel, pacienții trebuie să fie suficient de apți pentru a suporta acest tip de tratament, iar comorbiditățile trebuie evaluate înainte de inițierea tratamentului. La bărbații despre care se crede că nu pot tolera doza și schema standard de docetaxel, aceasta poate fi scăzută de la 75 la 50 mg/m2 la fiecare două săptămâni, prezentând mai puține evenimente adverse de grad 3-4 și un timp mai lung până la eșecul tratamentului.46
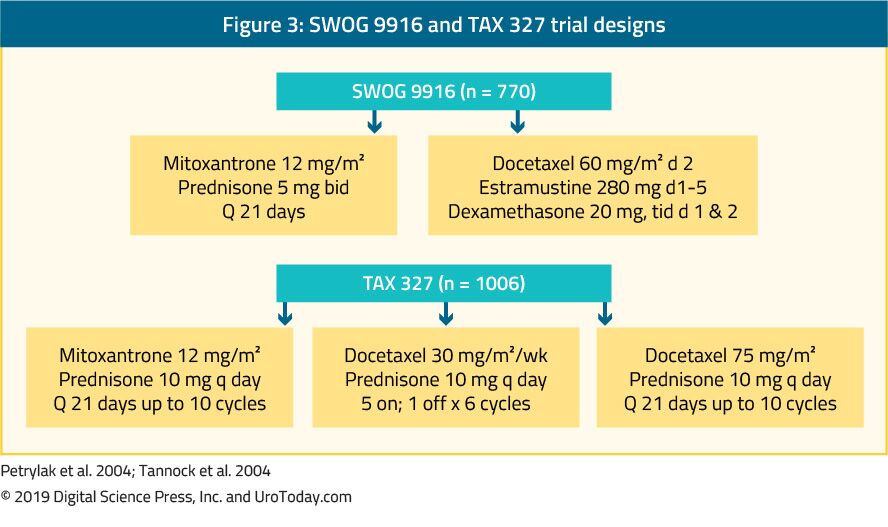
Figura 3. SWOG 9916 și TAX 327 modele de studiu
Sipuleucel-T
sipuleucel-T, o imunoterapie celulară activă autologă, a fost demonstrat într-un studiu de fază III (studiu de IMPACT) pentru a conferi un beneficiu de supraviețuire la 512 pacienți asimptomatici sau minim simptomatici cu mCRPC în comparație cu placebo24 (Figura 4). După o urmărire mediană de 34 de luni, supraviețuirea mediană a fost semnificativ mai mare în grupul tratat cu Sipuleucel-T (25,8 față de 21,7 luni, cu o RR de 0,78,p = 0,03).24 important, nu a fost observată o scădere a PSA în timpul sau după tratament, iar SFP a fost similară în ambele brațe. Toleranța generală la sipuleucel-T a fost foarte bună, majoritatea evenimentelor adverse de gradul 1-2 apărând. În prezent, acest tratament este disponibil numai în SUA și nu mai este disponibil în Europa.
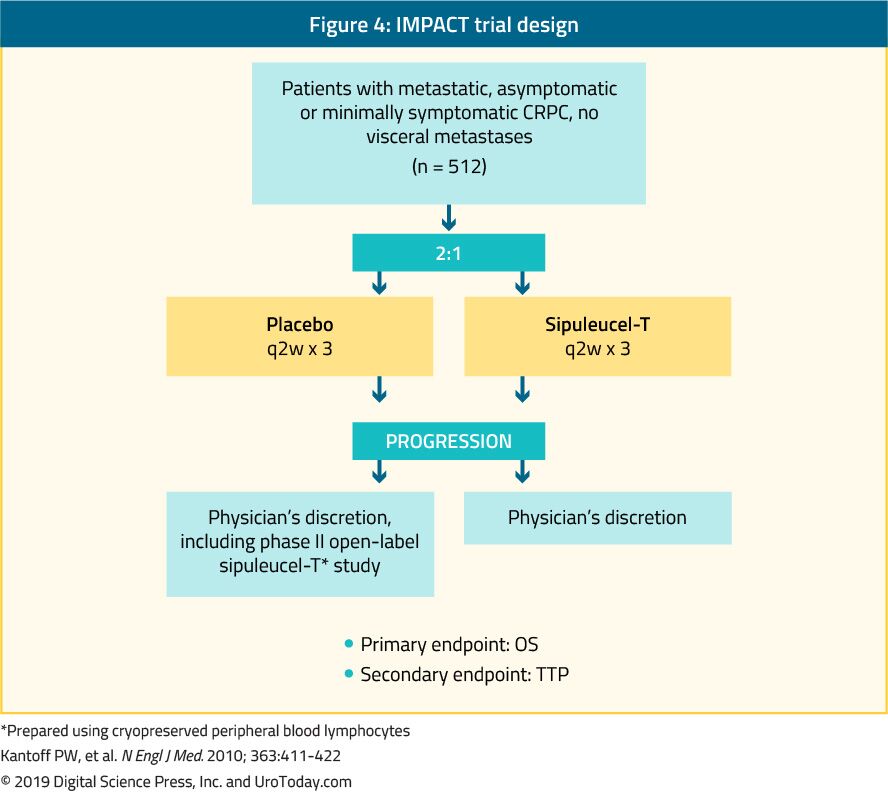
Figura 4. IMPACT trial design
concluzii
în ultimii 15 ani, au existat progrese științifice considerabile și investiții în dezvoltarea de medicamente pentru pacienții cu mCRPC. Acest lucru a dus la aprobarea FDA a mai multor linii de terapii sistemice pe motive de paliație a durerii, minimizând efectele adverse ale bolii și prelungirea sistemului de operare. Până în prezent, impactul raportat asupra OS la pacienții cu mCRPC de la fiecare dintre acești agenți individuali este încă modest, rezultând o adăugare de doar câteva luni. Este necesar să ne îmbunătățim înțelegerea biologiei bolii mCRPC, să integrăm o înțelegere moleculară cuprinzătoare a rezistenței la castrare și să analizăm mecanismele de rezistență la terapiile actuale pentru a îmbunătăți dezvoltarea viitoare a tratamentului. De asemenea, este esențial să se investească și să se dezvolte biomarkeri predictivi pentru a ajuta la personalizarea terapiei. În cele din urmă, într-o notă mai practică, sunt necesare mai multe date privind terapiile adecvate de a doua și a treia linie și secvențierea și combinația de medicamente disponibile, discutate mai detaliat în următorul articol de revizuire („dincolo de tratamentul de primă linie al cancerului de prostată rezistent la castrat metastatic”).
Data Publicarii: 19 noiembrie 2019
Leave a Reply