Pro și contra testării prenatale
scopul screeningului și diagnosticului prenatal este identificarea anomaliilor cromozomiale, a condițiilor genetice și a anomaliilor structurale la făt înainte de naștere.
opțiunile de screening și diagnostic implică o serie de teste neinvazive și invazive în diferite stadii ale sarcinii și au avansat în salturi în ultimii 40 de ani, în paralel cu schimbări sociale și demografice semnificative în acea perioadă.
în Australia în 2013, vârsta medie a femeilor care au născut a fost de 30,1 ani, comparativ cu 29,5 în 2003, în timp ce proporția mamelor în vârstă de 35 de ani și peste a crescut de la 19% în 2003 la 22% în 2013, iar vârsta medie a mamelor pentru prima dată a crescut, de asemenea, de la 27,8 ani în 2003 la 28,6 în 2013,1
în urmă cu patruzeci de ani, vârsta maternă a fost singurul instrument de pentru a identifica sarcinile cu risc de anomalii cromozomiale. De atunci, disponibilitatea unor teste prenatale neinvazive din ce în ce mai ieftine și precise a însemnat că femeile de toate vârstele pot avea acum opțiuni îmbunătățite de testare prenatală.când se confruntă cu numeroasele opțiuni pentru testarea prenatală, unele cupluri se pot simți copleșite, în timp ce clinicienii pot găsi o provocare să țină pasul cu toate detaliile noilor teste. Dar consilierea este vitală pentru a se asigura că cuplurile sunt pe deplin conștiente de procesul de testare din perspective fizice, emoționale, practice și financiare.
prima și cea mai importantă întrebare de pus este: ar trebui cuplul să ia în considerare testarea prenatală? Unele cupluri nu discută niciodată problema până nu rămân însărcinate și mulți nu au luat niciodată în considerare posibilitatea de a avea un copil cu o problemă cromozomială, cum ar fi sindromul Down, sau un defect de naștere, cum ar fi buza despicată.
pe de altă parte, în aceste zile îmbunătățirea alfabetizării în domeniul sănătății înseamnă că multe cupluri sunt informate și proactive, iar unele își doresc fiecare test disponibil pentru a se asigura că bebelușii lor sunt sănătoși.
următoarea întrebare se referă la ce test / teste să aibă și dacă acestea ar trebui să fie teste de screening sau de diagnostic. Prin definiție, un test de screening examinează o populație pentru a identifica acele persoane cu risc crescut de a avea o anumită afecțiune, în timp ce un test de diagnostic determină dacă o persoană are o anumită afecțiune. În contextul testării prenatale, testele de screening includ scanări cu ultrasunete, screening biochimic și testare prenatală neinvazivă (NIPT), în timp ce testele de diagnostic sunt eșantionarea vilusului corionic (CVS) și amniocenteza.
în cele din urmă, atunci când vorbim cu Cuplurile despre testare, Există problemele practice ale costurilor și accesului, care vor fi influențate într-o mare măsură de statutul socioeconomic al pacientului. Multe servicii cu ultrasunete de înaltă calitate și alte teste nu sunt Medicare rebatable și, prin urmare, inaccesibile pentru unii pacienți.
desigur, doar pentru că un test este disponibil nu înseamnă că ar trebui efectuat, iar cuplurile care se angajează în testarea prenatală trebuie să facă acest lucru cu ochii larg deschiși pentru a evita să ajungă într-o plimbare cu rollercoaster de coșmar atunci când sunt menționate pentru „toate testele”.
în acest scop, consilierea pre-test este vitală, astfel încât cuplurile să înțeleagă șansele materne legate de vârstă ale unui copil cu o problemă cromozomială majoră și apoi să le poată cântări în raport cu riscurile și beneficiile diferitelor teste oferite.
cuplurile trebuie să înțeleagă exact ce pot și ce nu pot detecta testele și, cel mai fundamental, exact de ce fac testul. Întrebările dificile trebuie să răspundă în acest stadiu: ar lua în considerare încetarea unei sarcini dacă un făt a fost diagnosticat cu sindrom Down? Diagnosticul ar informa managementul și planificarea nașterii dacă un făt cu sindrom Down ar avea, de asemenea, un defect cardiac major care necesită o intervenție chirurgicală cardiacă neonatală?
Acest articol ia în considerare două scenarii de caz comune și gama de opțiuni de testare prenatale disponibile pentru ambele.
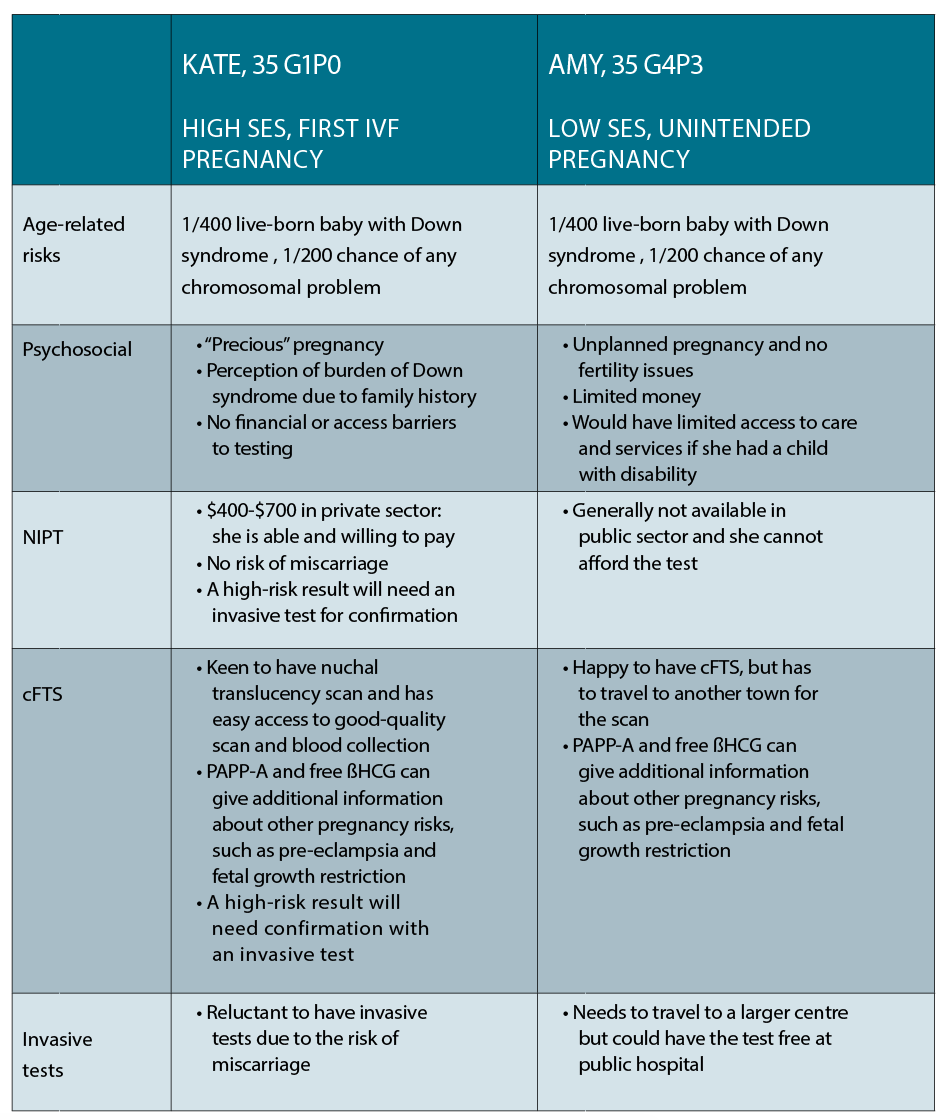
cazul 1
Kate este un avocat corporativ în vârstă de 35 de ani care locuiește în centrul orașului, care și-a conceput prima sarcină în cel de-al patrulea ciclu de FIV. Acum este însărcinată în 10 săptămâni și dorește să cunoască opțiunile disponibile pentru diagnosticul prenatal. Are o verișoară cu sindrom Down și este foarte preocupată de propriul risc de a avea un copil cu aceeași afecțiune.
Cazul 2
Amy are, de asemenea, 35 de ani și locuiește într-un mic oraș din NSW. Ea și partenerul ei au trei copii mici și se luptă financiar, iar ea este de 10 săptămâni într-o sarcină neintenționată. Vrea să-și cunoască opțiunile pentru testarea prenatală, deoarece unul dintre prietenii ei a născut recent un copil cu sindrom Down.

cuplurile trebuie să înțeleagă exact ceea ce testele pot și nu pot detecta
testare neinvazivă
un prim trimestru timpuriu sau datare, ultrasunetele sunt efectuate între șapte și 12 săptămâni și sunt utile în confirmarea prezenței unei sarcini viabile și a unei determinarea dacă există o sarcină multiplă. De asemenea, permite datarea exactă a gestației, ajută la excluderea unei sarcini ectopice și localizarea placentei. Nu se efectuează pentru a detecta defectele congenitale.
o scanare a translucenței nucale se efectuează între 11 săptămâni și trei zile și 13 săptămâni și șase zile (lungimea coroanei fetale de 45-84mm), în mod ideal ca parte a „screeningului combinat în primul trimestru”. Translucența nucală este un spațiu umplut cu lichid în partea din spate a gâtului fetal care poate fi măsurat prin ultrasunete. Este bine recunoscut faptul că, cu cât transluciditatea nucală este mai mare, cu atât este mai mare riscul de anomalii fetale, inclusiv probleme cromozomiale, cum ar fi sindromul Down, precum și defecte cardiace structurale și unele tulburări ale unei singure gene.
până în prezent, recomandarea a fost ca scanarea translucenței nucale să fie făcută împreună cu un screening biochimic matern ca un ecran combinat de prim trimestru (cFTS), care măsoară PAPP-A și gratuit pentru a îmbunătăți ratele de detectare a Sindromului Down.
singur, scanarea translucenței nucale are o rată de detectare de aproximativ 65% până la 70% pentru sindromul Down și, cu adăugarea de markeri serici, cum ar fi PAPP-A și beta-HCG liber, ambele raportate ca multipli ai medianei (mame), aceasta crește la aproximativ 90% cu o rată fals pozitivă de 5%.
în majoritatea cazurilor, aceste teste vor fi liniștitoare și vor oferi cuplurilor liniște sufletească fără a pune sarcina în pericol, care poate apărea cu teste invazive, cum ar fi CVS sau amniocenteza.odată cu disponibilitatea testelor prenatale neinvazive, au apărut dezbateri cu privire la valoarea screeningului combinat în primul trimestru pentru sindromul Down, deși mulți susțin că scanarea de 12 săptămâni are încă un rol de jucat în identificarea anomaliilor structurale și a altor probleme care ar putea afecta negativ rezultatul sarcinii.2
ecografia morfologică fetală se efectuează la 18 până la 20 de săptămâni și poate detecta până la 50% din anomaliile structurale majore. Nu este recomandat ca test de screening primar pentru sindromul Down. Sensibilitatea scanării în detectarea malformațiilor este influențată de o serie de factori, inclusiv natura malformației, abilitatea și experiența operatorului, calitatea mașinii cu ultrasunete, habitusul corpului matern și poziția placentei.
testarea prenatală neinvazivă
o probă genetică fetală detectabilă în sângele matern, care poate fi testată pentru un diagnostic prenatal precis, a fost mult timp Sfântul Graal al testării prenatale. Îmbunătățirile tehnologiei ADN au dus în cele din urmă la capacitatea de a izola și măsura ADN-ul fetal circulant în sângele matern.3
aproximativ 10% până la 15% din ADN-ul din sângele matern este de origine fetală și provine din celule fetale intacte, precum și din ADN fetal circulant fără celule (ccffDNA), derivat predominant din descompunerea celulelor placentare. CcffDNA este eliminat în câteva ore de la naștere din circulația maternă, iar ADN-ul fetal detectat în timpul unei sarcini, prin urmare, reprezintă ADN-ul fătului actual.
NIPT implică măsurarea fragmentelor cromozomiale fără celule și utilizarea diferențelor cantitative pentru a distinge sarcinile aneuploidice de cele care nu sunt afectate. De exemplu, fetușii cu sindrom Down vor avea o creștere măsurabilă și semnificativă statistic a numărului de fragmente de cromozom 21.
cu toate acestea, la fel ca eșantionarea villusului corionic, ccffDNA reflectă ADN-ul placentar mai degrabă decât fetal, care trebuie luat în considerare la consilierea și discutarea opțiunilor potențiale de testare invazivă. Acest lucru poate returna rezultate ambigue citogenetic cauzate de factori precum mozaicismul placentar.numeroase companii de biotehnologie au lansat diferite platforme NIPT cu nume eufemistice, cum ar fi Harmony și Panorama, permițând testarea prenatală non-invazivă la scară largă pentru aneuploidia fetală, cum ar fi trisomia 13, 18 și 21, și anomalii comune ale cromozomilor sexuali, cum ar fi sindromul Turner.
principalele avantaje ale NIPT sunt că este neinvaziv, disponibil de la nouă săptămâni de gestație și are sensibilitate și specificitate ridicate, deși prin definiție este mai degrabă un screening decât un test de diagnostic. Cu toate acestea, aproximativ 25% din anomaliile cromozomiale nu vor fi detectate prin NIPT și, prin urmare, testarea invazivă ar trebui oferită femeilor cu risc crescut de anomalie cromozomială, de exemplu în cazul măsurării crescute a translucenței nucale sau CFT sau a celor cu o anomalie structurală detectată la ultrasunete.4
există, de asemenea, un dezavantaj practic în setarea Australian ca NIPT nu este finanțat din fonduri publice, ceea ce duce la inechitate de acces. Nu este încă stabilit modul în care NIPT ar trebui încorporat în practica de screening prenatal de rutină sau care este cel mai rentabil mod de a face acest lucru.
mulți experți susțin în prezent modelul de screening contingent prin care toate femeile au CFT, iar celor cu risc ridicat de sindrom Down (>1/50) li se oferă teste invazive; celor cu risc intermediar între 1/50 și 1/300 li se oferă posibilitatea de a alege fie NIPT, fie testarea invazivă; iar celor cu risc scăzut (<1/300) și nu a oferit teste suplimentare.5
testarea invazivă sau diagnostică
în ultimii ani, numărul procedurilor de testare prenatală invazivă a scăzut semnificativ, în principal datorită disponibilității unor teste neinvazive îmbunătățite.6 principalele indicații pentru efectuarea testelor invazive sunt acum pentru diagnosticul prenatal al tulburărilor cu o singură genă (Mendelian), mai degrabă decât pentru detectarea aneuploidiei.
prelevarea de villus corionic este un test invaziv efectuat la 11 până la 13 săptămâni de sarcină, fie printr-o abordare trans-vaginală, fie trans-abdominală, în funcție de preferința operatorului și de localizarea placentei. Rata de avort spontan legată de procedură este scăzută (<1%), dar rămâne totuși o barieră pentru unele femei, în special la cele cu antecedente de infertilitate sau pierderea sarcinii.
există o șansă de 1% de a obține un rezultat neconcludent cu CVS. Acest lucru se datorează, de obicei, mozaicismului placentar limitat, un fenomen bine recunoscut care poate fi asociat cu PAPP-a scăzut și cu rezultate adverse ale sarcinii, inclusiv restricționarea creșterii fetale și pierderea timpurie a sarcinii, chiar dacă fătul are un cariotip normal. Atunci când rezultatele CVS sunt ambigue, se efectuează teste suplimentare – în general amniocenteză – pentru a clarifica dacă anomalia cromozomială este cu adevărat prezentă la făt sau este limitată la placentă.
amniocenteza se efectuează după 15 săptămâni și este, de asemenea, asociată cu un mic (<0.5%) riscul de avort spontan. Amniocenteza este considerată standardul de aur, prin faptul că celulele fetale obținute din lichidul amniotic sunt derivate din mai multe țesuturi fetale, inclusiv tractul urinar și pielea, și sunt astfel mai reprezentative pentru cariotipul fetal decât cele obținute din placentă. Principalul dezavantaj al amniocentezei față de CVS este momentul ulterior și, prin urmare, gestația mai avansată, până la primirea rezultatelor.
în prezent, majoritatea laboratoarelor de diagnostic s-au îndepărtat de analiza citogenetică (cariotip) ca test standard și au adoptat tehnici moleculare, inclusiv reacția cantitativă fluorescentă în lanț a polimerazei (QF-PCR). QF-PCR este mai ieftin și mai puțin intensiv în muncă decât analiza standard a cariotipului, iar rezultatele sunt obținute mai rapid (în 24-48 de ore comparativ cu 10-14 zile), deoarece tehnica nu necesită cultivarea celulelor fetale.în timp ce QF-PCR este capabil să diagnosticheze aneuploidiile comune care implică cromozomii 13, 18, 21 și cromozomii sexuali, nu poate detecta alte anomalii cromozomiale rare. De asemenea, nu poate determina dacă o trisomie se datorează non-disjuncției (adică aneuploidie comună, legată de vârstă) sau translocării, care este mai rară, dar îngrijorătoare, deoarece poate fi moștenită și asociată cu un risc crescut de recurență în viitoarele sarcini.
microarray cromozomial, cunoscut și sub numele de cariotip molecular, este bine stabilit ca una dintre principalele investigații utilizate pentru evaluarea bebelușilor și copiilor cu anomalii structurale și dizabilități intelectuale. Analizează cromozomii la o rezoluție mult mai mare (în general <2,5 kb sau 250.000 perechi de baze) comparativ cu rezoluția de 5 MB până la 10 MB a unui cariotip standard sau studiu citogenetic, pentru a detecta mici duplicări și ștergeri cromozomiale.
Din ce în ce mai mult, microarray-ul este utilizat în cadrul prenatal, unde poate produce rezultate dificil de interpretat, denumite „variante de semnificație incertă”. Din acest motiv, microarray – ul cromozomial trebuie oferit numai cu consiliere adecvată pre-și post-test și numai în situațiile în care este indicat clinic. În cazul sarcinilor cu risc ridicat în care a fost detectată o anomalie structurală sau o măsurare crescută a translucenței nucale, s-a demonstrat că microarray îmbunătățește randamentul diagnosticului cu aproximativ 6%.7
diagnosticul genetic preimplantare este acum disponibil pentru pacienții cu risc crescut de aneuploidie sau o tulburare de genă unică. Ei sunt acum capabili să se supună FIV și au embrioni biopsiați și testați prin diagnostic genetic preimplantare în ziua a cincea, înainte de transferul embrionului în uter.
PGD este utilizat din ce în ce mai mult de cuplurile care doresc să evite o sarcină afectată de o anumită afecțiune genetică sau anomalie cromozomială. Deși nu este 100% exactă, PGD poate reduce semnificativ riscul de a avea o sarcină afectată și, prin urmare, necesitatea de a lua în considerare întreruperea sarcinii.
există două tipuri principale de diagnostic genetic preimplantare:
testarea pentru aneuploidie: aceasta este utilizată pentru cuplurile cu risc de aneuploidie din cauza vârstei materne avansate, translocării echilibrate parentale, avortului spontan recurent și eșecului implantării;
testarea pentru o singură tulburare genică: aceasta este utilizată în cuplurile cu risc de a avea un copil cu o singură tulburare genică, inclusiv condiții autosomale recesive, legate de X sau dominante autosomale. În aceste situații, diagnosticul molecular sau ADN specific trebuie identificat, înainte ca PGD să poată fi oferit.
este vital ca cuplurile care iau în considerare FIV și PGD să fie trimise pentru consiliere adecvată, deoarece trebuie să fie pe deplin conștiente de punctul fizic, emoțional și financiar relevant pentru aceste proceduri.
Dr.Kennedy este Director MOTHERSAFE RHW și lector comun școala de sănătate a femeilor și copiilor la UNSW
1. Mamele și bebelușii Aihw Australia 2013 pe scurt
2. McLennan A, Palma-Dias R, da Silva Costa F și colab. Testarea prenatală neinvazivă în practica clinică de rutină – un audit al NIPT și screening combinat în primul trimestru la o populație australiană neselectată. ANZJOG 2016; 56: 22-28.
3. Lo YMD, Corbetta N, Chamberlain PF, Rai V, Sargent IL, Redman CWG, Wainscoat JS. 1997. Prezența ADN-ului fetal în plasma și serul matern. Lancet 350, 485-4874:
4. Petersen OB1, Vogel i, Ekelund C, Hyett J, Tabor A. consecințele diagnostice potențiale ale aplicării testelor prenatale neinvazive: studiu bazat pe populație dintr-o țară cu screening existent în primul trimestru. Cu Ultrasunete Obstetret Gynecol. 2014 Mar;43 (3):265-71.
5. Hui l, Hyett J testarea prenatală neinvazivă pentru trisomie 21; provocări pentru implementare în Australia. ANZJOG 2013; 53 (5):416-424.
6. Hui L, Muggli EE, Halliday JL. Tendințe bazate pe populație în screeningul prenatal și diagnosticul pentru aneuploidie: o analiză retrospectivă a 38 de ani de date la nivel de stat. BJOG 2016; 123(1):90-7
7. Wapner RJ et al Chromosomal microarray versus karyotyping for prenatal diagnosis N Engl J Med 2012; 367:2175-2184

Leave a Reply