Epigenetica-nu doar genele ne fac
deci, ce este epigenetica?
Un alt mod de a privi epigenetica este așa; în timp ce genetica tradițională descrie modul în care secvențele ADN din genele noastre sunt transmise de la o generație la alta, epigenetica descrie transmiterea modului în care genele sunt utilizate. Pentru a face o analogie computerizată, gândiți-vă la epigenetică ca metadate, informații care descriu și ordonează datele subiacente. Dacă dețineți un player MP3, de exemplu, acesta va conține o mulțime de date, fișierele MP3. Gândiți-vă la acestea ca fiind analoage genelor. Dar, probabil, veți avea și liste de redare sau puteți reda piese după artist sau gen. Aceste informații, playlist, artist, gen etc. este metadate. Determină ce piese sunt redate și în ce ordine, și asta este epigenetica pentru Genetică. Este un set de procese care afectează genele care sunt activate sau „exprimate”, așa cum ar spune biologii moleculari.
cum funcționează epigenetica?
deci epigenetica este despre modul în care genele sunt exprimate și utilizate, mai degrabă decât secvența ADN a genelor în sine, dar cum funcționează acest lucru? Mulți cercetători au studiat epigenetica în ultimele decenii și este în prezent o zonă de activitate intensă de cercetare. Știm că o parte din modul în care funcționează epigenetica este prin adăugarea și eliminarea etichetelor chimice mici la ADN. Vă puteți gândi la aceste etichete ca la note post-it care evidențiază anumite gene cu informații despre dacă ar trebui să fie activate sau dezactivate. De fapt, eticheta chimică în cauză se numește grupare metil (vezi diagrama 1) și este utilizată pentru a modifica una dintre cele patru baze sau „litere chimice”, A, C, T și G, care alcătuiesc codul genetic al ADN-ului nostru. Litera care este etichetată este C sau citozină și atunci când este modificată sau metilată se numește 5-metil citozină. Grupările metil sunt adăugate la ADN de enzime numite ADN metil transferaze (Dnmt).
-
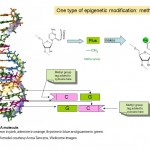
diagrama 1. Două etichete chimice, grupări metil și acetil care sunt centrale pentru fenomenele epigenetice și structura chimică a citozinei și 5-metil citozinei din ADN. Partea pentagonală a moleculei formează „coloana vertebrală” continuă a ADN-ului . Este prezentat doar unul dintre cele două fire de ADN care alcătuiesc dubla helix familiară.
statusul albinei regine este parțial determinat de mai puține etichete de metil
în majoritatea cazurilor, mai mult Cs metilat în ADN-ul unei gene are ca rezultat oprirea genei. Albinele de miere ne oferă un bun exemplu despre cum poate funcționa acest lucru. Albinele lucrătoare și regina au corpuri foarte diferite; Regina este mult mai mare, trăiește mai mult, are abdomenul mărit și depune multe mii de ouă, în timp ce muncitorii mai mici sunt sterili, dar au abilități complexe de hrănire și comunicare. În ciuda acestui fapt, Regina și muncitorii dintr-un stup sunt femei și identice genetic. Indiciul despre cum se întâmplă acest lucru se află în lăptișorul de matcă, o secreție care este alimentată unor larve în curs de dezvoltare și care are ca rezultat ca aceste larve să devină regine, mai degrabă decât muncitori. Vom reveni mai târziu la lăptișorul de matcă și proprietățile sale de fabricare a reginei, dar o cercetare fascinantă a arătat că, dacă cantitatea de grupare metil care adaugă enzima DNMT a fost redusă artificial în larvele de albine, atunci larvele s-au dezvoltat în regine, chiar dacă nu au fost hrănite cu jeleu regal. Astfel, comutatorul dintre regină și lucrător poate fi inversat de abundența etichetelor metil de pe ADN-ul larvelor de albine. Mai puține etichete de metil conduc la pornirea unei gene sau gene speciale în larvele în curs de dezvoltare, ceea ce duce la dezvoltarea larvelor în regine și nu în lucrători.
tag-uri pe cozi funcționează, de asemenea, switch-uri de gene
ADN-ul metil tag-uri sunt doar o parte din poveste, Deși. În celulele tuturor plantelor și animalelor, ADN-ul este ambalat sau înfășurat în nucleozomi unde ADN-ul dublu helix este înfășurat în jurul unui nucleu central de proteine (vezi diagrama 2). Aproximativ 150 de Litere de ADN (sau perechi de baze) sunt înfășurate în jurul fiecărui nucleozom, iar acest lucru ajută la împachetarea celor 3 miliarde de perechi de baze de cod genetic în fiecare dintre celulele noastre. Nucleozomii sunt prea mici pentru a fi văzuți folosind microscoape convenționale, dar biologii folosesc o tehnică numită difracție cu raze X pentru a elabora forma și organizarea obiectelor precum nucleozomii, iar în 1997 această tehnică a dezvăluit structura frumoasă a nucleozomilor la rezoluție înaltă-see (http://www.rcsb.org/pdb/explore/explore.do?structureId=1aoi).
-
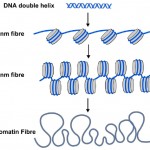
Diagrama 2. Helixul dublu ADN familiar (albastru) este înfășurat în jurul nucleozomilor (cilindri gri) din celule. Șirul de nucleozomi poate fi înfășurat într-un filament mai gros, numit fibră de 30 nm și acesta poate fi înfășurat în continuare într-o fibră de cromatină încă mai groasă. Când genele sunt pornite, nucleozomii lor sunt mai desfăcuți ca fibra de 10nm.
Nucleozomii sunt compacți, dar capetele sau „cozile” proteinelor care alcătuiesc nucleozomul, numite histone, ies din structura nucleozomală altfel compactă. La fel ca etichetele metil de pe ADN, etichete chimice mici pot fi adăugate și la aceste cozi de histone (vezi diagrama 3). Două dintre etichetele chimice care se adaugă la aceste cozi sunt grupările acetil și grupările metil. Metil, acetil și alte câteva tipuri de etichete pot fi adăugate la cozi într-un număr mare de combinații și acest lucru afectează dacă o genă subiacentă este pornită sau oprită. De fapt, genele pot fi oprite imediat (aceasta se numește tăcere), pornite complet sau undeva între ele prin etichete de metil ADN și etichete de coadă de histonă. Combinația de etichete ADN și histone poate afecta, de asemenea, cât de ușor este activată sau dezactivată o genă.
-
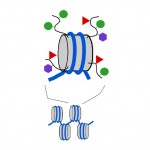
diagrama 3. Etichetele chimice pot fi adăugate la „cozile” proteinelor histonice care alcătuiesc nucleozomii. Cilindru gri, nucleozom; linii negre curbate, cozi de histone; cercuri verzi, etichete metil; triunghiuri roșii, etichete acetil; hexagoane mov, alte tipuri de etichete.
când celulele se divid
când celulele se divid, întreaga secvență de ADN din celula originală (3 miliarde de perechi de baze conținute în 23 de perechi de cromozomi dintr-o celulă umană) este duplicată astfel încât ambele celule fiice să primească o copie exactă. Ce, ați putea întreba, se întâmplă cu toate acele etichete epigenetice? Știm de ceva timp că etichetele ADN-metil sunt copiate, astfel încât ambele celule fiice au același model de metilare a ADN-ului. Acum știm că modelul etichetelor histonice este, de asemenea, în mare parte duplicat pe măsură ce celulele se divid, deși acest lucru este în prezent mai puțin bine înțeles. Cu toate acestea, diviziunea celulară este, de asemenea, un moment în care etichetele epigenetice pot fi schimbate cel mai ușor.
întoarcerea viermelui de lungă durată
chiar la început am dat peste povestea viermilor microscopici de lungă durată caretrecut longevitatea lor descendenților lor, chiar dacă descendenții individuali nu au moștenit gena variantă (mutație) care a provocat inițial durata de viață extinsă. Acum suntem în măsură să explicăm acest rezultat aparent ciudat. În cele mai multe cazuri, genele conțin informații pentru a face o moleculă de proteină, iar moleculele de proteine ar putea fi enzime care efectuează reacții chimice în celulă sau părți ale structurii celulei în sine. Se pare că genele care au fost mutate în studiul viermilor fac proteine care lucrează împreună pentru a adăuga o etichetă de metil nucleozomilor. Această etichetă este un comutator. Când una sau mai multe gene au suferit mutații, această etichetă a fost absentă și mai multe gene care ar trebui să fie activate, inclusiv unele implicate în îmbătrânire, au fost oprite și viermii au avut o durată de viață mai lungă. Lucrul neașteptat este că etichetele epigenetice au fost considerate a fi complet șterse sau resetate în timpul formării spermei și ovulului și, spre deosebire de genele în sine, acestea nu ar trebui transmise generației următoare. Dar acest rezultat și alte cercetări care arată că acest lucru nu este întotdeauna cazul și că, uneori, modelul etichetelor epigenetice este transmis.
cum se face o regină
dacă o albină larvară devine lucrătoare sau regină depinde de un comutator epigenetic, iar acest comutator pare a fi „răsturnat” de lăptișorul de matcă. Dar ce este despre lăptișorul de matcă care conduce o larvă care altfel ar crește pentru a fi muncitoare, pentru a deveni regină? Răspunsul constă în înțelegerea faptului că etichetele chimice individuale care sunt adăugate la cozile histonice ale nucleozomilor sunt în mod constant revizuite de celulă. Etichetele acetil sunt adăugate de enzime numite histone acetil transferaze și sunt îndepărtate sau șterse de un al doilea grup de enzime numite histone Deacetilaze (Hdac). Ambele enzime sunt prezente în majoritatea celulelor și acest lucru permite activarea sau dezactivarea genelor în timp.
Mai multe etichete acetil ajută la obținerea statutului de albină regină
recent, cercetătorii și-au propus să identifice compușii din lăptișorul de matcă care ar putea modifica acest proces, iar ceea ce au descoperit a fost ceva cunoscut sub numele de inhibitor HDAC. Acesta a fost un compus chimic relativ simplu care este prezent în lăptișorul de matcă și care oprește acțiunea enzimelor HDAC care elimină în mod normal etichetele acetil din histone. Acest lucru are ca rezultat o acumulare de etichete acetil în celulele embrionilor de albine și, la fel ca reducerea grupărilor ADN-metil descrise anterior, se crede că aceasta activează genele cheie necesare dezvoltării unei regine. Fără inhibitorul HDAC din lăptișorul de matcă, larvele urmează un set „implicit” de instrucțiuni genetice și se dezvoltă în lucrători.inhibitorii HDAC nu sunt importanți doar pentru albinele regine, ci fac parte și dintr-un număr mic, dar în creștere, de medicamente utile din punct de vedere medical, care vizează etichetele epigenetice și care sunt utile în tratarea unor tipuri de cancer. În plus, Hdac-urile au, de asemenea, un rol în modul în care creierul nostru formează amintiri, iar medicamentele noi care afectează acetilarea histonei pot avea un rol în viitor în tratarea tulburărilor de memorie la pacienții vârstnici.
mediul și epigenetica
am văzut cum diferența dintre o regină și o albină lucrătoare este determinată de expunerea la o substanță chimică care modifică direct etichetele epigenetice, cum ar fi grupările acetil; dar există exemple în care nutriția sau alte aspecte ale mediului afectează populațiile umane într-un mod care poate fi explicat prin epigenetică? Evident, nu putem face experimente pe populațiile umane așa cum putem pe viermi microscopici sau albine, dar uneori istoria umană sau fenomenele naturale o fac pentru noi. Un astfel de exemplu este ceea ce este cunoscut sub numele de iarna foamei Olandeze. În ultimul an al celui de-al doilea Război Mondial din Europa, un embargo alimentar impus de forțele germane ocupante asupra populației civile din Olanda a dus la o foamete severă, coincidând cu o iarnă deosebit de dură. Aproximativ 20.000 de oameni au murit de foame, deoarece rațiile au scăzut sub 1000 kilocalorii pe zi. În ciuda haosului războiului, îngrijirea medicală și înregistrările au rămas intacte, permițând oamenilor de știință să studieze ulterior efectul foametei asupra sănătății umane. Ceea ce au descoperit a fost că copiii care se aflau în pântece în timpul foametei au cunoscut o creștere pe tot parcursul vieții a șanselor lor de a dezvolta diverse probleme de sănătate în comparație cu copiii concepuți după foamete. Perioada cea mai sensibilă pentru acest efect a fost primele câteva luni de sarcină. Astfel, ceva pare să se întâmple la începutul dezvoltării în uter, care poate afecta individul pentru tot restul vieții.
efectele epigenetice pot trece uneori la nepoți
și mai surprinzător, unele date par să sugereze că nepoții femeilor însărcinate în timpul iernii foamei experimentează unele dintre aceste efecte. Din ceea ce am discutat deja, acest lucru sugerează puternic un mecanism epigenetic. De fapt, cercetările cu familiile Olandeze Hunger Winter continuă, iar un studiu recent care a analizat o genă galled IGF2 a găsit niveluri mai scăzute ale etichetei metil în ADN-ul acestei gene la persoanele expuse foametei înainte de naștere. Deși IGF2 nu poate fi el însuși implicat în riscul crescut de sănătate precară la acești oameni, arată că efectele epigenetice (adică reducerea numărului de etichete metil pe anumite gene) care sunt produse înainte de naștere pot dura mai multe decenii. Studiile efectuate pe animale au constatat, de asemenea, că dieta mamei poate avea efecte asupra descendenților ei. De exemplu, hrănirea oilor o dietă lipsită de tipurile de alimente necesare pentru a face grupări metil duce la descendenți cu modele modificate de metilare a ADN-ului și care au rate mai mari decât cele așteptate ale anumitor probleme de sănătate.
epigenetica și imprimarea, de ce genele de la mamă și tată nu sunt întotdeauna echivalente
cu toții avem 23 de perechi de cromozomi în celulele noastre. Pentru fiecare pereche, unul a venit de la mamă și unul de la tată. Astfel, moștenim o copie a fiecărei gene de la fiecare părinte și, în general, presupunem că funcția genei nu depinde de părintele din care provine. Cu toate acestea, pentru genele imprimate lucrurile sunt diferite. Pentru aceste gene, copia maternă sau paternă a genei este activă, în timp ce cealaltă este tăcută. Există cel puțin 80 de gene imprimate la oameni și șoareci, dintre care multe sunt implicate în creșterea embrionului sau a placentei. Cum poate fi oprită o copie a unei gene, în timp ce cealaltă copie din aceeași celulă este pornită? Răspunsul este epigenetica. Probabil cea mai studiată genă imprimată este IGF2(vezi mai sus). O parte din IGF2 funcționează ca un comutator. Dacă ADN-ul este metilat aici, gena IGF2 poate fi exprimată. Comutatorul este metilat numai în copia Tatălui genei și astfel numai această copie este exprimată, în timp ce copia maternă este tăcută. Se crede că acest comutator este instalat în gameți (ouă și spermă), astfel încât chiar de la început, genele primite de la mamă și cele de la tată sunt etichetate diferit cu etichete epigenetice și deci nu sunt echivalente.sindromul Angelmann și sindromul Prader-Willi sunt două afecțiuni genetice distincte, cu simptome diferite, ambele cauzate de pierderea unei părți a cromozomului 15. Copiii care moștenesc o copie a acestui cromozom defect dezvoltă fie sindromul Angelmann, fie sindromul Prader-Willi, în ciuda faptului că au o copie normală a cromozomului de la celălalt părinte. Deci, cum duce aceeași mutație (pierderea unei părți a cromozomului 15) la aceste două condiții diferite? Răspunsul constă în descoperirea faptului că această piesă specială a cromozomului 15 conține o serie de gene care sunt imprimate, deci se exprimă doar copia paternă sau maternă a acestor gene; care dintre cele două sindroame apare depinde de faptul dacă ștergerea a fost în cromozomul matern sau moștenit patern. Când cromozomul defect este moștenit de la tata, nu există o copie funcțională a genelor imprimate care sunt oprite pe cromozomul matern 15 și rezultatul este sindromul Angelmann și invers pentru sindromul Prader-Willi. Acest lucru este destul de diferit de majoritatea afecțiunilor genetice, cum ar fi fibroza chistică, unde un efect asupra dezvoltării sau sănătății este văzut doar atunci când o genă mutantă sau gene este moștenită de la ambii părinți.
Băieți versus fete, cum să oprești un cromozom întreg
un pic de genetică despre care majoritatea dintre noi știm este ceea ce face un băiat un băiat, și o fată o fată. Sunt cromozomii X și Y. La începutul existenței noastre, fiecare dintre noi a primit un cromozom X de la mamele noastre prin ovul, iar în timp ce fetele au primit un alt cromozom X de la tații lor, prin spermă, băieții au primit un cromozom Y. Cromozomul Y din celulele unui embrion masculin îl direcționează să se dezvolte într-un băiat, în timp ce cu doi cromozomi X și fără cromozom Y embrionul feminin se dezvoltă într-o fată. Acum, s-ar putea observa că există un dezechilibru aici. Cu toții avem câte doi dintre toți ceilalți cromozomi, dar pentru cromozomii sexuali (X și Y) fetele au două X-uri, în timp ce băieții au doar un X (și un Y). În timp ce cromozomul Y conține puține gene, majoritatea implicate în „masculinitate”, cromozomul X conține destul de multe gene implicate în procese importante, cum ar fi vederea culorilor, coagularea sângelui și funcția musculară. Pentru a uniformiza „doza” genelor cromozomului X între celulele masculine și feminine, un întreg cromozom X este oprit în celulele feminine. Aceasta se numește inactivare a cromozomului X și se întâmplă foarte devreme în uter. În acest proces, celulele opresc aleatoriu cromozomul X patern sau matern, astfel încât atunci când se naște un copil, corpul ei este un amestec sau o himeră de celule în care cromozomul X matern sau patern este oprit. Modul în care se întâmplă acest lucru implică tipul de etichete epigenetice despre care am discutat și se știe de zeci de ani că celulele feminine conțin un cromozom X foarte compact numit corpul Barr care poate fi văzut la microscop, iar acesta este cromozomul X inactiv.
cazul pisicii cu carapace de broască țestoasă
probabil că suntem cu toții familiarizați cu pisicile cu carapace de broască țestoasă și cu paltoanele lor pestrițe cu petice de blană portocalie și neagră. Ceea ce s-ar putea să nu știți este că aproape toate pisicile cu acest tip de haină sunt femele! Motivul pentru aceasta este că o genă pentru culoarea hainei este localizată pe cromozomul X al pisicii. Există două versiuni ale acestei gene, numite „O” și „o”; una dă blană de ghimbir și cealaltă neagră. Două copii ale aceleiași versiuni la o pisică Feminină au ca rezultat ghimbir sau respectiv blană neagră, dar o copie a fiecăruia dă un efect de coajă de broască țestoasă. Aceasta se reduce la inactivarea cromozomului X. Pielea acestor pisici este compusă din patch-uri de celule în care cromozomul X matern sau patern este inactivat. Acest lucru are ca rezultat pielea cu gena o pornită și o tăcută în unele patch-uri (blană portocalie) și o genă pornită și o tăcută în alte patch-uri (blană neagră), de unde și modelul de broască țestoasă. Deoarece pisicile de sex masculin au doar un cromozom X și nu au inactivat cromozomul X, ele sunt fie portocalii, fie negre peste tot.
moștenirea epigenetică, pot fi transmise stările epigenetice de la o generație la alta?așa cum am văzut din exemplul viermilor rotunzi, efectele epigenetice (în acest caz durata de viață extinsă) pot fi uneori transmise de la o generație la alta, deși efectele par să dureze doar câteva generații. Există exemple în care efectele epigenetice se transmit generațiilor următoare la oameni sau la alte mamifere? Există unele dovezi că efectele iernii foamei Olandeze au afectat nepoții femeilor însărcinate în timpul foametei. În mod similar, într-un studiu al unei populații suedeze din nordul secolului 19, care a suferit cicluri de foamete și abundență, cantitatea de alimente disponibile pare să fi afectat sănătatea și longevitatea generației următoare.
Culoarea părului la șoarece poate fi determinată de un efect epigenetic
probabil cel mai cunoscut exemplu de efecte epigenetice transgeneraționale este furnizat de gena agouti de șoarece. Această genă controlează culoarea părului și este activată la momentul potrivit în celulele foliculului de păr pentru a produce o dungă galbenă în firele de păr altfel întunecate, rezultând ceea ce se numește un strat agouti. Dar șoarecii cu o variantă specială a genei Agouti numită Avy au straturi care sunt oriunde între modelul galben și cel întunecat normal (agouti) al șoarecilor de tip sălbatic. Șoarecii galbeni devin, de asemenea, obezi și suferă alte probleme de sănătate. Deci, gena Avy pare să aibă un efect variabil (de fapt, Avy înseamnă galben Avariabil). Modul în care funcționează acest lucru i-a nedumerit pe geneticieni de ani de zile, dar acum putem recunoaște acest lucru ca un efect epigenetic. Blana galbenă apare deoarece versiunea Avy a genei Agouti are controale defecte și este pornită tot timpul. Cu toate acestea, etichetele de metil sunt adesea adăugate la secvența ADN de control defectuoasă și acest lucru tinde să oprească gena, rezultând blană agouti pestriță sau întunecată la șoareci individuali. Puii născuți la baraje cu gena Avy variază de la galben la întuneric, dar proporția depinde de culoarea hainei mamei; puii de femele întunecate (agouti) sunt mai predispuși să conțină pui întunecați. Mai mult, se observă o proporție mai mare de descendenți întunecați dacă atât mama, cât și bunica au culoarea închisă. Deci, colorarea agouti, care este determinată epigenetic (prin numărul de etichete metil pe gena Avy) poate, într-o oarecare măsură, să treacă de la o generație la alta.deși putem găsi cazuri în care efectele epigenetice durează aparent de la părinți la descendenți, acest lucru nu este de obicei cazul și aproape toate comutatoarele sau semnele epigenetice sunt resetate în celulele germinale (ouă și spermă) și în primele etape de dezvoltare a unui embrion. De fapt, dacă nu era cazul, dezvoltarea uimitoare a unui ovul fertilizat într-o creatură complet formată ar fi imposibilă.până acum am descris câteva cazuri specifice de reglare epigenetică, dar acum știm că epigenetica în sensul său larg (modul în care genele sunt exprimate și utilizate, mai degrabă decât secvența ADN a genelor în sine) este esențială pentru modul în care un ovul fertilizat poate da naștere unui întreg organism și modul în care celulele, să spunem pielea, rămân celule ale pielii și sunt diferite de celulele creierului, în ciuda faptului că conțin exact aceleași gene. La scurt timp după fertilizare, un embrion uman în curs de dezvoltare constă dintr-o minge de celule numite celule stem embrionare. Fiecare dintre aceste celule are capacitatea de a da naștere la oricare dintre tipurile de celule din organism pe măsură ce embrionul crește (de exemplu, celulele creierului, celulele pielii sau celulele sanguine). În schimb, 9 luni mai târziu, când se naște un copil, majoritatea celulelor care alcătuiesc corpul său se angajează să fie un tip specific de celule cu funcții specifice. Deci, pe măsură ce celulele se divid, bila celulelor stem embrionare se dezvoltă treptat în toate tipurile și structurile celulare ale copilului la termen. Pentru ca acest lucru să se întâmple, mii de gene trebuie să fie activate sau dezactivate la momentul potrivit și în celulele potrivite pe măsură ce un embrion crește. De exemplu, genele care produc proteina fibroasă de cheratină care conferă pielii noastre puterea, sunt activate doar în celulele pielii și nu în creierul în curs de dezvoltare, iar genele necesare pentru ca celulele creierului să se dezvolte și să își facă interconexiunile sunt activate în creier, dar nu și în piele.
în timpul dezvoltării, genele trebuie activate și dezactivate. Tag-uri epigenetice ajuta cu acest
un domeniu foarte mare de cercetare astăzi se referă la modul în care toate aceste gene de comutare pe un off lucrări, și o mare parte a acestui proces utilizează tag-uri chimice epigenetice, în special acetil și metil histonă tag-uri. Pentru ca acele celule stem embrionare să poată da naștere tuturor celorlalte tipuri de celule, comutatoarele lor epigenetice sunt (aproape) complet resetate în comparație cu celulele adulte. Am pus” aproape ” între paranteze după cum știm din genele imprimate și moștenirea epigenetică transgenerațională că există excepții.
epigenetica, Oaia Dolly și prietenii
în februarie 1997, o oaie numită Dolly a devenit cel mai faimos exemplu al speciei sale, devenind pentru scurt timp chiar o celebritate TV. Motivul faimei sale este că a fost primul mamifer care a fost „creat” printr-un proces numit transfer nuclear de celule somatice sau, cu alte cuvinte, prima clonă creată de om (creată de om pentru a fi distinctă de gemenii identici, care sunt clone naturale). Procesul care a dus la nașterea ei a necesitat un ovocit matur (un ou nefertilizat) de la o oaie femelă și o celulă obișnuită din ugerul unei a doua oi. Mai întâi nucleul (partea care conține ADN-ul) a fost îndepărtată din ovocit. Acest lucru a fost făcut folosind un microscop special, deoarece, deși ovocitele sunt destul de mari în comparație cu alte celule, ele sunt încă prea mici pentru a vedea cu ochiul liber. Apoi, nucleul din celula ugerului a fost introdus în ovocitul enucleat. Astfel, Dolly a avut trei „mame”: donatorul ovocitului, donatorul celulei ugerului și oile care au purtat embrionul în curs de dezvoltare la termen. Nici un tată nu a fost implicat. Deși acest proces a fost și rămâne foarte ineficient, a fost prima dovadă că genele dintr-o celulă mamiferă adultă pot fi „reprogramate epigenetic” înapoi la starea celulelor stem embrionare care se pot dezvolta în orice alt tip de celulă. Ulterior, același proces a fost aplicat altor specii și poate avea utilizări medicale în generarea de celule care ar putea repara țesuturile deteriorate de leziuni sau boli.
rezumat: epigenomul și proiectul ENCODE – ” Large Hadron Collider „al biologiei
în timp ce termenul” genom ” se referă la întreaga secvență ADN a unui organism (trei miliarde de litere ale acestuia pentru oameni), epigenomul se referă la întregul model de modificări epigenetice în toate genele, inclusiv etichetele ADN metil, etichetele histonei metil, etichetele acetil histonei și alte etichete chimice pe care nu le-am menționat, în fiecare tip de celulă a unui organism. Aceasta reprezintă o cantitate aproape inimaginabilă de informații, depășind chiar și Proiectul genomului uman. Cu toate acestea, cunoașterea epigenomului este esențială pentru a răspunde pe deplin la unele dintre cele mai mari întrebări din biologie, cum ar fi: cum ne dezvoltăm dintr-o minge de celule identice într-un întreg organism? de ce îmbătrânim? și cum putem înțelege mai bine bolile precum cancerul? Nu este surprinzător atunci, epigenetica și epigenomul reprezintă un domeniu mare de cercetare. Unele dintre cercetările din acest domeniu sunt cuprinse de proiectul ENCODE (Encyclopedia of ADN Elements), un proiect continuu de identificare a tiparelor de etichete epigenetice în multe tipuri diferite de celule pentru întregul genom uman (http://genome.ucsc.edu/ENCODE/). Proiectul ENCODE este uneori asemănat cu Large Hadron Collider sau LHC din Elveția. LHC este cel mai mare echipament științific construit vreodată, iar experimentele pe care fizicianul le efectuează cu scopul de a cerceta detaliile fundamentale ale materiei care alcătuiește universul nostru. Deși biologii nu au (sau au nevoie) de o piesă atât de spectaculoasă pentru cercetarea lor, efortul de a examina complexitatea epigenomului uman a fost asemănat cu proiectul LHC datorită amplorii, complexității și cantității de informații create.
Erorile epigenetice
epigenetica este un domeniu în care cunoștințele noastre științifice cresc rapid. Un lucru pe care oamenii de știință l-au descoperit este că erorile epigenetice sunt frecvente în boli precum cancerul și în celulele îmbătrânite. Drept urmare, oamenii de știință dezvoltă medicamente care vizează epigenomii defecți și unul dintre primele exemple este utilizarea inhibitorilor HDAC, similar cu compusul găsit în lăptișorul de matcă. Din studiul unor modele ciudate de moștenire, cum ar fi imprimarea genetică, șoarecele Galben/agouti Avy, populația de pisici de broască țestoasă și alte fenomene conexe, biologii au descoperit un nou strat de informații care se află „deasupra” secvenței ADN a genelor noastre. Aceste noi descoperiri explică aceste observații nedumerite anterioare, dar au, de asemenea, un mare potențial pentru noi înțelegeri și tratamente pentru bolile umane.
lecturi suplimentare:
- Bird, Adrian. Epigenetica. Expert Instant nr. 29′ , New Scientist, 5 ianuarie 2013, nr.2898.Carey, Nessa. Revoluția epigenetică: modul în care biologia modernă rescrie înțelegerea noastră despre genetică, boală și moștenire. Editor: Icon Cărți. Paperback 1 martie 2012. ISBN-10: 1848313470. Preț RRP 9-99.
influențe epigenetice și boli la site-ul:
- http://www.nature.com/scitable/tpicpage/epigenetic-influences-and-disease-895
Leave a Reply