care este cel mai reactiv Element din tabelul Periodic?
fluorul este identificat ca fiind cel mai reactiv nemetal și cel mai electronegativ element din tabelul periodic, făcându-l cel mai puternic agent oxidant. Cesiul este cel mai reactiv metal din tabelul periodic, atât de mult încât lucrul cu acest metal se termină adesea în explozii!
ce i-a spus un chimist altuia când l-a găsit rănit? „De ce sunteți în dificultate de sodiu? Cred că exagerezi!”Vezi ce am făcut acolo? Uneori mă întreb De ce – în ciuda ilarității mele-mi se pare foarte greu să-mi fac prieteni…
oricum, în afară de notele mele slabe, primul lucru care îmi vine în minte când mă gândesc la chimie sunt paltoanele de laborator, vasele cu formă ciudată, ca și cum ar fi reflecții din oglinzile carnavalului și explozii aprinse. Din când în când, cineva mormăie „reacție” sau „reactivitate”, termeni atât de omniprezenți încât îi veți găsi infiltrându-se în cărțile de chimie până la ultima lor pagină. Aceasta este exact ceea ce ne preocupă acum.

lipsit de orice jargon tehnic, o „reacție” este exact ceea ce înseamnă, un răspuns. Reactivitatea, pe de altă parte, poate fi definită ca măsura cât de ușor o specie chimică va participa la o reacție și va forma legături chimice. Deci, întrebarea devine – care element este cel mai ușor de incitat? Dar mai întâi…
ce determină reactivitatea unui element?
în termeni simpli, o reacție chimică este oportunitatea perfectă pentru cumpărători și vânzători de a cumpăra și vinde bunuri. Cumpărătorii și vânzătorii sunt elemente chimice. Bunurile sunt electroni, iar moneda schimbată este energia.
scopul acestui comerț este de a atinge stabilitatea, o configurație optimă a electronilor, care se realizează atunci când învelișul de valență (exterior) al unui element este complet umplut sau golit. Practic, un element poate cumpăra mai mulți electroni pentru a-și umple penultima coajă sau pentru a-i vinde pentru a-l goli.

cu cât electronii implicați sunt mai puțini, cu atât consumul de energie este mai mic. Oricine este familiarizat cu modul de funcționare parsimonios al naturii va ghici că tranzacțiile care necesită cea mai mică cantitate de energie sunt cele care sunt cel mai probabil să apară. Acest lucru are sens, deoarece un element ar prefera să piardă electroni și să se golească dacă învelișul său exterior este mai puțin de jumătate umplut sau să câștige ceva pentru a se umple, dacă este mai mult de jumătate umplut. Cumpararea șase atunci când puteți pierde pur și simplu două ar fi pur și simplu o prostie, dar mai important, scump!
astfel, reactivitatea este o funcție a cât de ușor un element pierde sau câștigă electroni.
cum estimăm stimulentele unui element?
tabelul periodic și „tendințele” acestuia
cum aflăm dacă un element este cumpărător sau vânzător? Ne referim la tabelul periodic.
tabelul periodic este un memento că oamenii de știință sunt toc limită și nu pot să nu organizeze totul într-un mod extrem de îngrijit și ordonat. Tabelul periodic organizează fiecare element pe care îl cunoaștem într-o manieră colocată.
tabelul aranjează elementele în funcție de numărul lor atomic, care este același cu numărul de protoni sau electroni pe care îi cuprind. (Nu este ciudat că tind să fie exact la fel?)
Trend 1
numărul de electroni din învelișul de valență crește cu unul pe măsură ce analizăm fiecare element dintr-un rând, deși numărul de cochilii rămâne același. Numărul de cochilii poate fi dedus din numărul rândului. De exemplu, fiecare element din al doilea rând va conține doar două cochilii și așa mai departe.
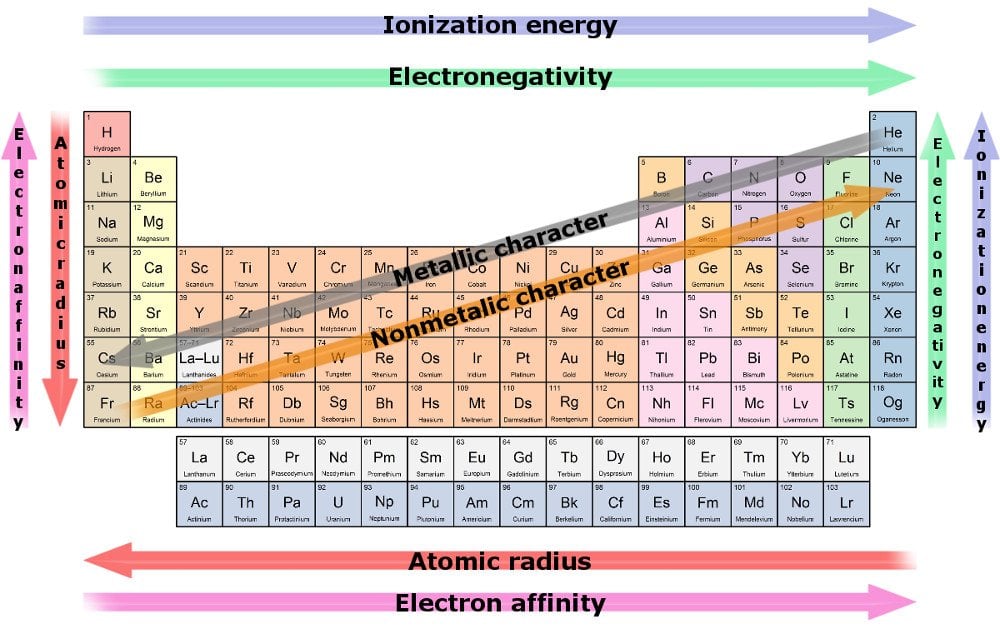
o consecință a acestei tendințe este că raza atomică scade pe măsură ce ne îndreptăm spre ultimul rezident al unui rând. Motivul fiind că creșterea electronilor este reflectată de creșterea protonilor din centru, în timp ce primii trebuie să se înghesuie în aceeași coajă. În războiul tug-o ‘ dintre protonii care trag și electronii în creștere, primul câștigă, rezultând o atracție nucleară mai mare, trăgându-și toate cochiliile mai aproape de el.
prin urmare, datorită unei puternice atracții, un element este mai probabil să cumpere sau să câștige electroni pe măsură ce ne deplasăm de-a lungul unui rând. Măsura capacității unui element de a trage electroni spre el este cunoscută sub numele de electronegativitate. Cel mai electro-negativ element este cel mai probabil să fure electroni și să reacționeze cel mai rapid.
Trend 2
o altă tendință este creșterea razei elementelor pe măsură ce ne deplasăm în jos pe o coloană, în timp ce numărul de electroni de valență rămâne același, chiar dacă numărul atomic continuă să crească. Acest lucru se datorează faptului că creșterea electronilor este paralelă cu o creștere a cochiliilor. Metalele grele au o rază crescută, în special cele de pe fundul cel mai înalt. Ele ilustrează cea mai săracă atracție nucleară și, prin urmare, au o slabă reținere a electronilor lor exteriori.

măsura capacității unui element de a pierde electroni este cunoscută sub numele de electro-pozitivitate și crește pe măsură ce ne deplasăm în jos pe o coloană. Din nou, cel mai electropozitiv element este cel mai probabil să renunțe la electronii săi și să reacționeze cel mai rapid.
acum că știm regulile, să dezvăluim câștigătorii.
cel mai reactiv non-metal – fluor
fluorul este primul element din grupul halogen. Este un gaz galben pal, diatomic, foarte coroziv, inflamabil, cu un miros înțepător. Numărul său atomic este 9 și are un blocaj de 7 electroni în învelișul său de valență. Mai mult, se află în al doilea rând, ceea ce implică faptul că toți cei 9 electroni ai săi sunt înghesuiți cumva în doar 2 cochilii.
un înveliș de valență cu 7 electroni îi cere să câștige doar un singur electron pentru a-și finaliza învelișul final și pentru a obține stabilitate, ceea ce nu este o mare ispravă atunci când iei în considerare dimensiunea sa mică și atracția nucleară viguroasă. Fluorul este identificat ca fiind cel mai electronegativ element din tabelul periodic, făcându-l cel mai puternic agent oxidant. Este cel mai reactiv nemetalic.

fluorul este atât de reactiv încât poate arde substanțe pe care, în general, le-am considera neinflamabile! Poate arde sticlă, apă și chiar nisip! Promiscuitatea sa face imposibilă stocarea sau izolarea acesteia în forma sa cea mai pură. Datorită reactivității sale sălbatice, istoria sa timpurie de izolare și experimentare este plină de accidente fatale. Da … fatal.
cel mai reactiv metal – cesiu
cesiul este un metal de culoare aurie care reacționează exploziv cu aerul și apa. Numărul său atomic este de 55. Cesiul se află în prima coloană și al doilea până la ultimul rând. După cum am discutat, raza unui element atât de scăzut în coloană este destul de mare în comparație cu elementele de mai sus.

(Credit Foto : Dnn87 / Wikimedia Commons)
raza mare face ca tragerea sa nucleară să fie ineficientă și o face extrem de stângace. Dimensiunile sale mari îl fac foarte susceptibil la ionizare. Este foarte acceptat și renunță cu ușurință la singurul electron din învelișul său de valență pentru a atinge stabilitatea, făcându-l foarte reactiv. Cesiul este cel mai reactiv metal din tabelul periodic, atât de mult încât lucrul cu acest metal se termină adesea în explozii!
franciu
Franciul este ultimul element din prima coloană, așezat chiar sub cesiu, făcându-l cel mai mare atom din coloană. În mod logic, s-ar deduce că Franciul trebuie să aibă o reactivitate superioară în comparație cu Cesiul, dar acest lucru nu este cazul.
se estimează că nu există mai mult de o uncie din aceasta în scoarța Pământului la un moment dat. Deoarece este atât de rar în mod natural, oamenii de știință trebuie să o producă pentru a o studia.

(Credit Foto : MarlonMarin1 / Wikimedia Commons)
cu toate acestea, chiar și atunci când este cumva izolat, nu durează foarte mult. Franciul este radioactiv în natură, având un timp de înjumătățire de numai 22 de minute, așa că se descompune înainte de a avea șansa de a reacționa! Mai mult, prezența atâtor protoni face ca electronii săi să se deplaseze la viteze incredibil de mari. După cum și — a dat seama Einstein, la scări atât de mici și viteze atât de mari, încep să apară lucruri ciudate-electronii se strâng puțin mai aproape de nucleu decât s-ar aștepta logic, făcându-i ușor mai greu de scăpat.
deci, se pare că Franciul este cel mai reactiv element, din păcate teoretic.
alertă Spoiler!
s — ar putea să fi observat că cele două elemente considerate a fi cele mai reactive sunt câștigătoare numai în categoriile lor specifice-metale și nemetale. Ne pare rău să fie un buzzkill, dar nu există nici un răspuns definitiv la care-este-cel-cel-reactiv-element-printre-toate, pentru că este nevoie de doi la tango.
s-ar putea întreba care element este cel mai reactiv cu sodiul? Răspunsul este atunci fluor, nu cesiu. Sau, poate doriți să știți care element este cel mai reactiv cu azotul. Este Litiu! Șocant!
termenul de reactivitate este adesea interpretat greșit. Întrebarea este ambiguă și oarecum incompletă, așa cum arată sperăm acest articol.
Leave a Reply