Servier – Phlebolymphology
Baixar esse assunto de Volta ao sumário
trombose de membros inferiores:
update e atual
recomendações
Bourgoin-Jallieu, França
Resumo
Inicialmente, superficial, trombose venosa (SVT) foi considerada uma doença benigna ou uma complicação comum das varizes. Estudos recentes demonstraram a gravidade potencial da TVM e definiram o seu lugar nas doenças tromboembólicas venosas (TEV), juntamente com trombose venosa profunda (TVP) e embolia pulmonar (EP). Foi identificada uma TVP Concomitante em 25% a 30% dos doentes na apresentação e uma EP em 4% a 7% dos doentes. Foram notificadas DTV subsequentes em 3 a 20% dos doentes, dependendo da duração de seguimento. Até recentemente, foram testadas numerosas estratégias anticoagulantes, sem qualquer benefício clínico claramente demonstrado. No entanto, a recente CALISTO estudo (Comparação de Arixtra no Membro inferior Superficial, Trombose venosa com placebo) validado uma terapia anticoagulante protocolo baseado em fondaparinux, 2,5 mg diariamente durante 45 dias, resultando em recomendações actualizadas para a gestão da SVT. Este artigo irá apresentar uma atualização sobre a gestão da SVT de baixa perna e as recomendações e diretrizes atuais. Resumidamente, todos os pacientes com SVT devem ter uma varredura duplex bilateral para confirmar o diagnóstico de SVT, determinar a localização precisa e extensão da SVT, e diagnosticar ou descartar a presença de um DVT. Para doentes com TVM sintomática com pelo menos 5 cm de comprimento, recomenda-se prescrever uma dose profiláctica de fondaparinux ou heparina de baixo peso molecular durante 45 dias sem anticoagulação (grau 2B), e quando o custo do tratamento com fondaparinux é aceitável, recomenda-se a utilização de 2, 5 mg diários vs heparina de baixo peso molecular (grau 2C). No entanto, as recomendações e diretrizes têm atribuído estes tratamentos com um baixo grau, e as perguntas permanecem sobre a gestão SVT. Foram identificados alguns factores de risco para o desenvolvimento subsequente de uma TEV, mas é necessária investigação adicional para definir subgrupos de doentes com uma maior incidência de TEV após TEV.
introdução
trombose venosa Superficial (TEV) foi considerada uma doença benigna ou uma complicação comum das veias varicosas; contudo, estudos recentes demonstraram a sua gravidade potencial e definiram o seu lugar nas doenças tromboembólicas venosas (TEV), juntamente com trombose venosa profunda (TVP) e embolia pulmonar (EP). a terapêutica anticoagulante é amplamente utilizada hoje em vez de anti-inflamatórios não esteróides (AINE), que foram comumente usados até a última década. Um estudo recente validou, pela primeira vez, um protocolo terapêutico.1 no entanto, subsistem questões relativas à gestão da TVM: (i) é necessária terapêutica anticoagulante para tratar todos os doentes com TVM dos Membros inferiores?* devem ser utilizadas doses profilácticas ou terapêuticas? qual é a duração de tratamento recomendada?* iv) o tratamento deve ser o mesmo para a TVM que ocorre nas veias varicosas e nas veias não varicosas?; (v) podem ser previstos os fatores de risco de complicações VTE após SVT?; and (vi) is surgery still indicated for the management of an acute SVT?
Este artigo irá apresentar a lógica por trás da atualização para a gestão de SVTs das pernas e as recomendações e diretrizes atuais.
a incidência de trombose venosa superficial dos Membros inferiores
SVT é considerada uma doença comum, mas a incidência real na população adulta permanece desconhecida. Um estudo recente, realizado em França (2), mostrou que a taxa de diagnóstico anual era de 0,6%. Foi maior nas mulheres e aumentou com o avanço da idade, independentemente do sexo. Surpreendentemente, a taxa de diagnóstico anual da tvm foi menor do que o esperado e menor do que a taxa de diagnóstico anual da TVE (cerca de metade da TVE). De acordo com outro estudo francês, realizado com métodos comparáveis, a incidência anual de uma TVP dos Membros inferiores e PE foi de 1,24% e 0,6%, respectivamente.3
Superficial, trombose venosa, com concomitante de trombose venosa profunda na apresentação
O POST (Observacional Prospectivo Tromboflebite Superficial) e OPTIMEV estudos (Optimização de l”Interrogatoire dans l”évaluation du risque trombo – Embolique Veineux), dois grandes observacionais e estudos epidemiológicos, publicou recentemente dados essenciais sobre SVT.4,5 com Um total de 844 pacientes com SVT das pernas, foram analisados no POST de estudo,4 e uma TVP ou PE foi identificado em 25% dos pacientes com SVT na apresentação e uma TVP proximal foi diagnosticada em 9,7% dos pacientes. Devemos enfatizar que a TVP não foi contígua com SVT em 41,9% dos pacientes com TVP. Um total de 788 pacientes com SVT foram inscritos no OPTMEV estudo,5, onde um SVT foi associado com uma TVP na inclusão em 29% dos pacientes com TVP distal ocorrendo em 59.5% dos pacientes (128/215; o local exato da TVP estava faltando em 12 pacientes).
estes dados confirmam estudos anteriores que a TVP foi associada à TVM em 23% a 36% dos doentes e mostram coerência entre os diferentes estudos (Tabela I).2,4-10
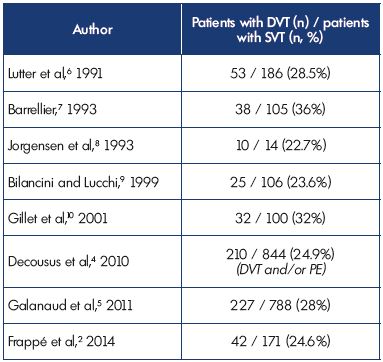
quadro I. trombose venosa Superficial com trombose venosa profunda concomitante na apresentação.
abreviaturas: TVP, trombose venosa profunda; PE, embolia pulmonar; SVT,
trombose venosa superficial.
trombose venosa Superficial associada a embolia pulmonar na apresentação
na inclusão, foi diagnosticada EP sintomática em 3, 9% e 6.9% dos doentes nos estudos pós e OPTIMEV, respectivamente. No entanto, a SVT com PE, mas sem DVT, representou apenas 2,2% de todos os SVTs com DVT ou PE. Estes dados corroboram os resultados de estudos anteriores (Quadro II).2,4-7,9,10
Na prática, uma digitalização duplex de exame é obrigatório em pacientes com SVT para confirmar o diagnóstico (Figura 1), determinar com precisão o local e a extensão da SVT, e diagnosticar ou descartar a presença de uma TVP.
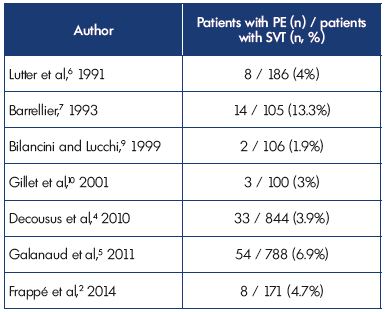
quadro II. trombose venosa Superficial com embolia pulmonar concomitante na apresentação.abreviaturas: PE, embolia pulmonar; TVM, trombose venosa superficial.
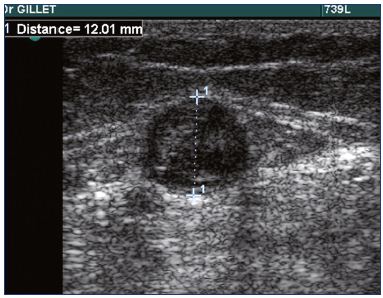
Figura 1. Ecografia de trombose da veia safena pequena.

Resultado e tromboembólicos venosos recorrência
Na literatura, a taxa de tromboembólicos recorrência varia de 3% a 20%, dependendo da duração do seguimento. Num estudo pessoal, 13 notificámos a ocorrência de Eti sintomática em 16, 4% dos doentes com TVM isolada, com um seguimento médio de 14, 5 meses. Os eventos VTE incluíram DVT (31%), PE (6%), outro SVT em um sistema safeno diferente (37,5%), e um SVT recorrente no mesmo sistema safeno (25%). 8.3% dos pacientes com isolados SVT a inclusão desenvolvido, pelo menos, 1 TEV sintomático evento em 3 meses (TVP sintomática, de 2,8%; sintomático PE, a 0,5%; sintomático extensão da SVT, de 3,3%; e recorrência sintomática da SVT, 1.9%). No estudo OPTIMEV, 5 3% dos doentes com TVM isolado e 5, 4% dos doentes com TVM associado à TVP na apresentação desenvolveram TV aos 3 meses; a taxa de TV foi de 12, 5% no seguimento de 3 anos. No estudo realizado por Dewar e Pampher,ocorreu TVP sintomática em 4% dos doentes com TVM isolada no período de acompanhamento de 6 meses. estes resultados epidemiológicos mostram a potencial gravidade da TVM. Eles não devem mais ser considerados uma condição benigna. Consequentemente, o seu lugar foi agora claramente definido no âmbito das doenças VTE.
fatores de Risco para o desenvolvimento de um evento tromboembólico
Uma análise multivariada de PÓS study4 identificados do sexo masculino, história de TVP ou EP, anterior câncer, e sem varizes como fatores de risco para TEV sintomático em 3 meses, incluindo a recorrência ou a extensão da SVT. No estudo STENOX (tromboflebite Superficial tratada com enoxaparina),15 história de TEV (TVP ou EP), sexo masculino e insuficiência venosa crónica grave foram identificados como factores preditivos independentes para uma TEV aos 3 meses. Apenas a insuficiência venosa crónica grave foi um factor preditivo independente para TVP ou EP. Em uma análise conjunta do POST e OPTIMEV estudos,16 Galanaud et al mostraram que o sexo masculino, o câncer, a história pessoal de TEV, e saphenofemoral ou saphenopopliteal participação aumentou significativamente o risco de uma subseqüente TEV ou TVP/ PE em uma análise univariada. Em análises multivariadas, apenas o sexo masculino aumentou significativamente o risco de uma recorrência de DTV/EP subsequente. Para o câncer e uma história pessoal de TEV, ajustado hazard ratios foram apenas ligeiramente abaixo do nível de significância estatística (P=0,06 para ambos), sugerindo que, para esses fatores, o estudo simplesmente não dispunha de suficiente poder estatístico.
No STEFLUX estudo (Superficial Tromboembolismo FLUXum),17 de ter um índice de massa corporal (IMC) entre 25 e 30 kg/m2 e composto de um anterior SVT e/ou TEV e/ou história familiar de TEV foram identificados como significativos, independente de fatores de risco para TEV evento (composto de sintomáticos e assintomáticos TVP, PE, e SVT de recorrência ou de extensão). o estado da veia
estado da veia varicosa influenciou o risco de exposição da TVP na apresentação. Nos estudos POST4 e OPTIMEV,5 SVTs que ocorreram numa veia não varicosa (NVVV–SVT) foram mais frequentemente associados a uma TVP concomitante ou EP do que SVTs que ocorreram numa veia varicosa (VV-SVT). Resultados semelhantes foram comunicados por Gorty et al.18
no seguimento de 3 meses do estudo OPTIMEV, o VV-SVT isolado não foi associado a um maior risco de resultados adversos (ou seja, morte, recorrência de TEV e hemorragia). O nvvv-SVT isolado teve uma associação mais elevada com recorrência sintomática de TVP ou Ep (2, 7% vs 0, 6%), mas este resultado não atingiu significado estatístico (P=0, 07). no estudo pós-estudo, a ausência de varizes foi identificada como um factor de risco para o desenvolvimento subsequente de uma TEV sintomática em doentes com TVM sintomática isolada na apresentação (P=0, 049). No estudo STEFLUX,a ausência de varizes foi um factor de risco para a TEV (P=0, 004) após a interrupção do tratamento com heparina de baixo peso molecular.
No grupo placebo do CALISTO estudo (Comparação de Arixtra no Membro inferior Superficial, Trombose venosa com placebo),de 1 de complicações tromboembólicas ocorreu com mais freqüência quando o SVT envolveu a grande veia safena (GSV), foi estendido para no prazo de 10 cm de saphenofemoral de junção (SFJ), envolvidos veias acima do joelho, e em pacientes com história de TEV. a estase venosa é o principal mecanismo da TVM em doentes com varizes. A inflamação pode desempenhar um papel essencial na formação de trombos em doentes sem varizes; consequentemente, conferindo um risco mais elevado para um tromboembolismo clinicamente mais grave. O rastreio da trombofilia não é recomendado para o controlo de rotina de doentes com SVT-NVV, embora os dados da literatura tenham demonstrado que a trombofilia foi frequente nesta situação. Num estudo pessoal prospectivo, identificámos 10 trombofilia em 50% dos doentes com NVVV-SVT, enquanto apenas 15% dos doentes com VV-SVT tiveram trombofilia. Num outro estudo prospectivo envolvendo 42 doentes com NVVV-SVT,identificámos 19 trombofilia em 20 (47, 6%) doentes. A trombofilia mais comum deveu-se à mutação heterozigótica do factor V Leiden. Num estudo que envolveu 63 doentes com SVT-VV isolado,20 Martinelli e al identificaram trombofilia em 30% dos doentes. Recomenda-se o rastreio da trombofilia, após exclusão de um cancro oculto, especialmente em doentes com progressão de trombos, apesar da terapêutica anticoagulante adequada.11,21
tratamento de trombose venosa superficial
tratamento da TVM sempre foi um tema controverso. São notificadas grandes variações no tratamento, especialmente no que respeita à terapêutica anticoagulante. O estudo POST, 4, realizado em França entre Março de 2005 e outubro de 2006, forneceu informações interessantes sobre o tratamento da TVM. Um total de 634 doentes tiveram uma TVM isolada na inclusão. A informação sobre o tratamento que receberam durante o período de observação de 3 meses estava disponível para 597 doentes, tendo 90, 5% dos doentes recebido um ou mais fármacos anticoagulantes. Dos doentes a receber terapêutica anticoagulante, 63% receberam doses terapêuticas, 36, 7% doses profilácticas e 16, 8% antagonistas da vitamina K. A duração do tratamento foi altamente variável. Um total de 47.2% dos doentes receberam um AINE tópico, 8, 2% um AINE oral, e 10% tiveram cirurgia venosa (stripping ou High-ligation). estes dados mostraram a necessidade de clarificar o papel da terapêutica anticoagulante no tratamento da TVM. O uso de terapia anticoagulante em pacientes com tvm foi relatado pela primeira vez em 1962 por Zollinger et al,22 após observar a ocorrência de um EP, que foi fatal em 34 (10, 1%) de uma série de 335 pacientes com TVM. Até recentemente, embora tenham sido testadas numerosas estratégias anticoagulantes, incluindo heparina não fraccionada ou heparina de baixo peso molecular, em doses profilácticas ou terapêuticas durante várias durações, nenhuma demonstrou claramente qualquer benefício clínico.
O estudo STENOX study23 foi um ensaio aleatorizado em dupla ocultação envolvendo 427 doentes, comparando heparina de baixo peso molecular (enoxaparina em doses terapêuticas e profilácticas) com AINEs e placebo. Os doentes foram tratados durante 10 dias, com um acompanhamento de 3 meses. Ao fim de 10 dias, houve mais Eti no grupo placebo (P24 comparou as doses terapêuticas vs profilácticas de nobraparina em 163 doentes com TVM isolada no GSV, e os doentes foram tratados durante 1 mês. Em 3 meses de seguimento, os resultados foram semelhantes em ambos os grupos (de 7,2% e 8,6% de ocorrência de TEV, respectivamente; P=0.7), mostrando que não há benefício da terapêutica dose. Foi observado um fenómeno de” recuperação “ou de” rebound ” durante o seguimento, dado que foram notificados muitos Eti, especialmente no grupo de doentes tratados com a dose terapêutica. Foi também observado um fenómeno” catch-up ” após a interrupção do tratamento com heparina de baixo peso molecular após 1 mês no estudo STEFLUX.Estas conclusões, tal como as do julgamento STENOX, defendem a escolha de doses profilácticas de heparina de baixo peso molecular na TVM. A ocorrência da maioria dos Eti durante os 2 e 3 meses após a interrupção do tratamento com heparina de baixo peso molecular no grupo a receber doses terapêuticas, realça mais uma vez a questão da duração óptima da terapêutica anticoagulante.
A CALISTO study1 randomizada e duplamente cega comparou fondaparinux 2, 5 mg diários durante 45 dias com placebo em 3002 doentes com uma TVM sintomática isolada nos membros inferiores com pelo menos 5 cm de comprimento. Os principais critérios de exclusão foram o tratamento de câncer nos últimos 6 meses, TVP ou PE nos últimos 6 meses, SVT localizado dentro de 3 cm do SFJ, e insuficiência renal grave (depuração da creatinina 26 a 2,5 mg dose de fondaparinux foi selecionado na ideia de que uma dose profilática seria suficiente para o tratamento de pacientes com SVT. Além disso, esta dose mostrou-se mais eficaz na prevenção de vampire: the eternal struggle depois de uma grande cirurgia ortopédica do que uma dose profilática de baixo peso molecular, heparina, e tão eficaz quanto a dose terapêutica de baixo peso molecular da heparina em pacientes com síndromes coronárias agudas, sugerindo que fondaparinux 2,5 mg correspondem a 2008 American College of Chest Physicians (ACCP) recommendations27, que defendem o uso de profiláticos ou intermediário doses de baixo peso molecular heparina para o tratamento de pacientes com SVT. A duração de 45 dias foi escolhida porque um período de tratamento de 30 dias ou menos pode ser demasiado curto, uma vez que a maioria dos Eti sintomáticos ocorre após a interrupção do tratamento. O resultado primário da eficácia foi um composto de morte por qualquer causa, uma EP sintomática, uma TVP sintomática, uma extensão sintomática para a SFJ, ou uma recorrência sintomática da TVM no dia 47. Houve um período de acompanhamento de 77 dias para os pacientes.
O resultado primário de eficácia ocorreu em 0, 9% dos doentes no grupo de fondaparinux e em 5.9% no grupo placebo (P28
é interessante notar a mudança de recomendações a partir de 2008 ACCP diretrizes.No entanto, temos de ter em conta que se trata de recomendações de baixa qualidade (Grau 2B ou 2C). na atualização da Base de dados Cochrane Systematic Review on “Treatment for superficial trombophlebitis of the leg”, 29,30 Di Nisio et al chegaram às mesmas conclusões. Esta revisão foi baseada na análise de 30 ensaios controlados aleatórios envolvendo 6507 participantes com SVT das pernas. Os autores concluem que uma dose profilática de fondaparinux, administrada durante 6 semanas, parece ser uma opção terapêutica válida para a TVM das pernas. A evidência sobre tratamentos orais, tratamentos tópicos ou cirurgia é muito limitada e não fornece informações para uso na prática clínica sobre os efeitos destes tratamentos em termos de TEV e progressão SVT. cirurgia versus terapêutica anticoagulante uma revisão dos estudos comparando cirurgia com terapêutica anticoagulante não mostra qualquer benefício para o tratamento cirúrgico. As taxas de progressão da TVM foram semelhantes, enquanto a incidência de TEV e complicações foram maiores com a cirurgia.Lozano et al não mostraram diferença entre cirurgia e enoxaparina durante 4 semanas.32
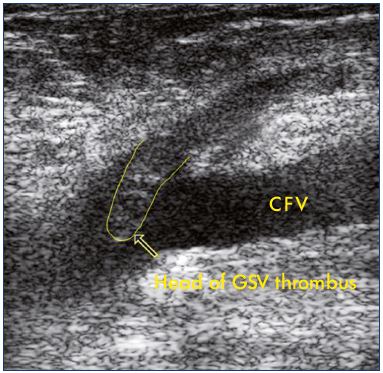
Figura 2. Ecografia de uma extensão de uma trombose da veia safena na veia femoral comum.
abreviaturas: CFV, common femoral vein; GSV, great saphenous vein
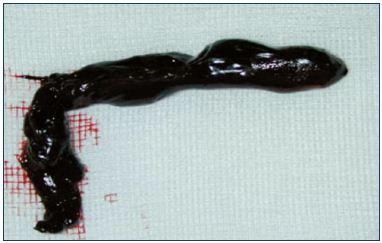
Figura 3. Trombose da junção safenofemoral.
Imagem cortesia do Dr. Nicolini.

Na prática, a maioria dos especialistas recomendam o tratamento de doentes com SVT prolongada no SFJ ou SPJ com terapêutica anticoagulante em doses terapêuticas durante 3 meses.
conclusão
SVT não deve mais ser considerada uma doença benigna. Estudos epidemiológicos recentes, que incluíram um grande número de pacientes, mostraram a gravidade potencial da SVTs e definiram claramente o seu lugar nas doenças VTE. Foi identificada uma TVP Concomitante em 25% a 30% dos doentes na apresentação e uma EP em 4% a 7% dos doentes. Consequentemente, todos os pacientes com SVT devem ter varredura duplex bilateral para confirmar o diagnóstico de SVT, determinar a localização precisa e extensão da SVT, e diagnosticar ou descartar a presença de um DVT. Hoje, a gestão da TVM mudou, com a terapia anticoagulante sendo amplamente utilizada em vez dos AINEs. Até ao recente estudo de CALISTO, nenhum protocolo anticoagulante demonstrou um benefício clínico claro. As recomendações foram actualizadas após o estudo CALISTO validar o protocolo de terapêutica anticoagulante com base em 2, 5 mg diários de fondaparinux durante 45 dias. Para doentes com TVM sintomática das pernas com pelo menos 5 cm de comprimento, recomenda-se uma dose profiláctica de fondaparinux ou heparina de baixo peso molecular durante 45 dias durante a ausência de anticoagulação (grau 2B). Quando o custo do tratamento com fondaparinux é aceitável, recomenda-se a utilização de 2, 5 mg diários de fondaparinux numa dose profiláctica de heparina de baixo peso molecular (grau 2C). No entanto, as recomendações e orientações são de baixa qualidade, e subsistem questões relativas à gestão da SVT. Foram identificados alguns factores de risco para o desenvolvimento subsequente de uma TEV, mas é necessária investigação adicional para definir claramente subgrupos de doentes com uma maior incidência de TEV após TEV.
1. D ecousus H, Prandoni P, Mismetti P, et al; grupo de estudo CALISTO. Fondaparinux para o tratamento de trombose venosa superficial das pernas. N Engl J Med. 2010;363:1222-1232.
2. Frappé P, Buchmuller-Cordier a, Bertoletti L, et al; STEPH Study Group. Taxa de diagnóstico anual de trombose venosa superficial dos Membros inferiores: o estudo da STEPH baseado na comunidade. J Thromb Haemost. 2014;12:831-838.
3. Grupo de estudo EPI-GETBO. Incidência de tromboembolismo venoso: um estudo de base comunitária no oeste da França. Thromb Hemost. 2000;83:657- 660.
4. D ecousus H, Quéré i, Presles e, et al; grupo pós-estudo. Trombose venosa Superficial e tromboembolismo venoso: um grande estudo epidemiológico prospectivo. Ann Intern Med. 2010;152:218-224.
5. G alanaud JP, Genty C, Sevestre MA, et al; Optimev Sfmv Investigators. Factores preditivos para trombose da profunda concomitante e recorrência tromboembólica venosa sintomática em caso de trombose venosa superficial. Thromb Hemost. 2011;105:31-39.
6. Lutter KS, Kerr TM, Roedersheimer R, Lohr JM, Sampson MG, Cranley JJ. Tromboflebite Superficial diagnosticada por varrimento duplex. Cirurgiao. 1991;100:42-46.
7. Barrellier MT. Tromboses veineuses superficielles des membres inférieurs . Vasc Int. 1993;17:7-9.
8. Jorgensen JO, Hanel KC, Mogan AM, Hunt JM. A incidência de trombose venosa profunda em doentes com tromboflebite superficial dos Membros inferiores. J Vasc Surg. 1993; 18: 70-73.
9. Bilancini S, Lucchi M. Les tromboses veineuses superficielles sont-elles polymorphes ? Phlébologie. 1999;52:41-43.
10. Trombose venosa Superficial dos Membros inferiores: análise prospectiva em 100 doentes . J Mal Vasc. 2001;26:16-22.
11. Kalodiki E, Stvrtinova V, Allegra C, et al. Trombose venosa Superficial: uma declaração consensual. Int Angiol. 2012;31:203-216.
12. Nicolaides A. Trombose venosa Superficial na prevenção e tratamento de tromboembolismo venoso. Int Angiol. 2013;32:237-242.
13. G illet JL, Perrin M, Cayman R. recorrência tromboembólica após tromboflebite superficial dos Membros inferiores. J Flebologia. 2002;2:103-118.
14. D ewar C, Panpher S. incidência de trombose venosa profunda em doentes diagnosticados com tromboflebite superficial após apresentação a um serviço de trombose venosa profunda no ambulatório do serviço de Urgências. Emerg Med J. 2010; 27: 758-761.
15. Quenet S, Laporte S, Décousus H, Leizorovicz a, Epinat M, Mismetti P; STENOX Group. Factores preditivos de complicações trombóticas venosas em doentes com trombose venosa superficial isolada. J Vasc Surg. 2003; 38: 944-949.
16. G alanaud JP, Bosson JL, Genty C, et al. Trombose venosa Superficial e tromboembolismo venoso recorrente: uma análise conjunta de dois estudos observacionais. J Thromb Haemost. 2012;10:1004-1011.
17. Cosmi B, Filippini M, Campana F, et al; STEFLUX Investigators. Factores de risco para acontecimentos recorrentes em indivíduos com trombose venosa superficial no ensaio clínico aleatorizado SteFlux (tromboembolismo Superficial Fluxum). Thromb Res. 2014;133:196-202.
18. G orty S, Patton-Adkins J, DaLanno M, Starr J, Dean S, Satiani B. trombose venosa Superficial das extremidades inferiores: análise dos factores de risco e recorrência e papel da anticoagulação. Vasc Med. 2004;9:1-6.
19. Ad tromboflebite Superficial nas veias não varicosas dos Membros inferiores. Uma análise prospectiva em 42 doentes . J Mal Vasc. 2004;29:263-272.
20. Martinelli I, Cattaneo M, Taioli e, de Stefano V, Chiusolo P, Mannucci PM. Factores de risco genéticos para trombose venosa superficial. Thromb Hemost. 1999;82:1215-1217.
21. Milio G, Siragusa S, Malato a, Grimaudo S, Pinto A. trombose venosa Superficial: papel da deficiência hereditária de anticoagulantes naturais em extensão às veias profundas. Int Angiol. 2009;28:298- 302.
22. Zollinger RW, Williams RD, Briggs DO. Problemas no diagnóstico e tratamento da tromboflebite. Arch Surg. 1962; 85: 34-40.
23. D ecousus H; grupo de estudo da enoxaparina. Uma comparação piloto aleatorizada, em dupla ocultação, de uma heparina de baixo peso molecular, um agente anti-inflamatório não esteróide e placebo no tratamento da trombose venosa superficial. Arch Int Med. 2003;163:1657-1663.
24. Prandoni P, Tormene D, Pesavento R; Vesalio Investigators Group. Doses elevadas vs. baixas de heparina de baixo peso molecular para o tratamento da trombose venosa superficial das pernas: um ensaio duplamente cego e aleatório. J Thromb Haemost. 2005;3:1152-1157.
25. Cosmi B, Filippini M, Tonti D, Avruscio G, Ghirarduzzi a, Bucherini E; STEFLUX Investigators. Um estudo Aleatório com dupla ocultação da heparina de baixo peso molecular (parnaparina) para trombose venosa superficial: STEFLUX (tromboembolismo Superficial e Fluxum). J Thromb Haemost. 2012;10:1026-1035.
26. D ecousus H, Frappé P, Accassat S, et al. Epidemiologia, diagnóstico, tratamento e gestão da trombose venosa superficial das pernas. Best Prat Res Clin Haematol. 2012;25:275-284.
27. Kearon C, Kahn SR, Agnelli G, Goldhaber s, Raskob GE, Comerota AJ; American College of Chest Physicians. Terapêutica antitrombótica para doença tromboembólica venosa: American College of Chest Physicians Evidence – Based Clinical Practice Guidelines (8.A edição). Peito. 2008; 133 (suppl 6): 454S-545S.
28. Kearon C, Akl EA, Comerota AJ, et al; American College of Chest Physicians. Terapêutica antitrombótica para a doença DTV: Terapêutica antitrombótica e prevenção de trombose, 9.a ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Peito. 2012; 141(suppl 2): e419s-e494s.
29. D I Nisio M, Wichers IM, Middeldorp S. tratamento para tromboflebite superficial da perna. Cochrane Database Syst Rev. 2013; 30; 4: CD004982.
30. Tratamento da extremidade inferior tromboflebite superficial. JAMA. 2014;311:729- 730.
31. Sullivan V, Denk PM, Sonnad SS, Eagleton MJ, Wakefield TW. Ligação versus anticoagulação: tratamento de tromboflebite superficial acima do joelho que não envolva o sistema venoso profundo. J Am Coll Surg. 2001; 193: 556-562.
32. Lozano FS, Almazan A. heparina de baixo peso molecular versus safenofemoral desconectada para o tratamento de tromboflebite safena superior acima do joelho: um estudo prospectivo. Vasc Endovascular Surg. 2003; 37: 415-420.
33. Chengelis DL, Bendick PJ, Glover JL, Brown OW, Ranval TJ. Progressão de trombose venosa superficial para trombose venosa profunda. J Vasc Surg 1996; 24: 745-749.
34. Hingorani A, Ascher E. tromboflebite venosa Superficial. Em: Gloviczki P, ed. Manual of Venous Disorders. Directrizes do American Venous Forum. 3rd ed. London, UK:Hodder Arnold; 2009: 314-319.
Leave a Reply