Gestão de Quimioterapia Extravasations
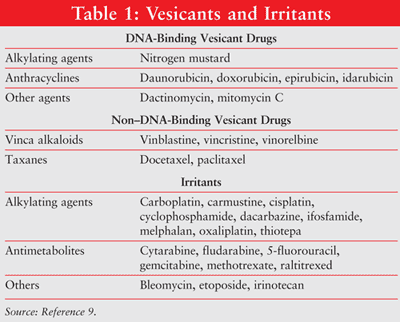
NOS Pharm. 2009; 34 (9) (Oncology suppl): 3-11. resumo: os medicamentos quimioterapêuticos intravenosos (IV) têm o potencial de causar lesão por extravasamento ou necrose tecidular no local de administração. Embora a maioria das extravasações possa ser prevenida através de uma administração de perfusão adequada e completa, vários antídotos foram reconhecidos e estudados para prevenir lesões tecidulares posteriores. infiltração e extravasamento são duas complicações distintas e bem conhecidas da terapêutica para perfusão intravenosa. De acordo com a Infusion Nurse Society e a Oncology Nursing Society, ambas as complicações envolvem a fuga inadvertida de uma solução IV para o tecido circundante; no entanto, o tipo de solução difere. Infiltração é a administração inadvertida de uma solução nãovésica ou irritante ou medicação nos tecidos circundantes.1,2 Nonvesicants são agentes que raramente produzem reacções agudas ou destroem o tecido quando se infiltram. Os agentes irritantes podem induzir dor no local da injecção ou ao longo da veia, com ou sem uma reacção inflamatória, normalmente sem lesões persistentes nos tecidos. No entanto, os irritantes só podem causar úlceras nos tecidos moles se uma grande quantidade de solução concentrada for inadvertidamente extravasada para induzir reacções inflamatórias sem danos nos tecidos persistentes.3,4 extravasamento refere-se à instilação inadvertida ou fuga de material vesicante para os espaços perivasculares e subcutâneos durante a administração da medicação.1, 2 extravasamento resulta em reacções locais que vão desde irritação local até necrose tecidular grave da pele, vasculatura circundante e estruturas de suporte.5-8 os agentes quimioterapêuticos podem ser classificados, com base no seu potencial para causar lesões tecidulares locais, como vesicantes, irritantes ou não-cancerígenos. (Vários vesicantes e irritantes são descritos no quadro 1.9) a extravasação acidental de medicamentos por via intravenosa ocorre em aproximadamente 0.1% a 6% das perfusões por via intravenosa periféricas e 0.3% a 4.7% das perfusões por porta de acesso venoso implantadas.10-12
Fisiopatologia da lesão tecidular
a extensão da lesão tecidular depende da capacidade de ligação do agente quimioterapêutico ao ADN. Os agentes de ligação ao ADN incluem antraciclinas, antibióticos antitumores, análogos de platina e alguns agentes alquilantes.Os 3,4 antineoplásticos de ligação ao ADN causam danos nos tecidos através da propagação de ligações letais ao ADN ou de quebras da cadeia causadas por radicais livres, que levam à apoptose celular.13-17 antineoplásticos não ligados ao ADN (ex., alcalóides da vinca, taxanos, inibidores da topoisomerase) interferem com a mitose. Os agentes não ligados ao ADN são eliminados mais facilmente dos locais de extravasamento e causam menos danos nos tecidos do que os agentes ligados ao ADN.17
os factores de risco para a extravasação
os riscos para a extravasação são multifactoriais e são em grande medida modificáveis. Muitos destes riscos resultam de erros na utilização e colocação dos dispositivos. Os fatores do dispositivo IV que afetam o risco de extravasamento incluem material da agulha (ou seja, metal), Tamanho da cânula (plástico Grande vs. plástico pequeno) e tipo de cateter (ou seja, cateter venoso central). As agulhas de Metal podem causar mais danos na inserção e são inflexíveis no interior do recipiente, enquanto as agulhas de grande calibre podem impedir o fluxo sanguíneo, atrasando a diluição do infusato.Pode ocorrer extravasamento do CVCs com uma deslocação da agulha de uma porta de acesso venoso implantada (IVAP), oclusão mecânica e subsequente lesão do CVC, migração do cateter ou formação de mangas fibrina e trombose. É mais provável que ocorra uma colocação incorrecta do IVAP em doentes com novos dispositivos, doentes com edema pós-operatório significativo e doentes obesos ou mulheres de peito grande.As oclusões mecânicas podem dever-se à formação de trombos, precipitado do fármaco, deslocação retrógrada do cateter ou pinch-off (isto é, uma oclusão intermitente e posicional do cateter; deve suspeitar-se se a oclusão da perfusão puder ser aliviada por o doente mover o seu posicionamento do braço).2, 21, 22 evitar o extravasamento depende muito da manutenção adequada do local IV e da garantia de que a velocidade de perfusão correcta está a ser implementada. Estes factores de risco estão relacionados com os antineoplásticos utilizados, os doentes e o clínico que administra o medicamento. a monitorização cuidadosa dos doentes e a educação dos doentes e dos profissionais sobre os riscos e a gestão do extravasamento vesicante parecem ser as pedras angulares da prevenção. Enquanto os médicos assumem a responsabilidade de escrever ordens precisas, os enfermeiros são responsáveis por garantir a colocação hábil e adequada de dispositivos e monitoramento de infusões de quimioterapia visualmente e através de entrevistas aos pacientes. Durante a administração do vesicante, o local deve ser monitorizado quanto a inchaço, vermelhidão e dor. Os vesicantes devem ser administrados de acordo com as recomendações dos fabricantes (por exemplo, diluição adequada, tempo de administração especificado). As vias IV devem ser lavadas antes e depois da administração de quimioterapia. O papel do farmacêutico seria ajudar a desenvolver políticas que garantam a verificação adequada, rotulagem e dispensa de agentes quimioterapêuticos. Uma maneira de isso ser executado é usar uma rotulagem discriminativa ao dispensar antineoplásticos vesicantes para que os enfermeiros usem as medidas de precaução adequadas. Os farmacêuticos podem desempenhar um papel integral na educação, fornecendo informação sobre drogas e serviços de rotina a todos os membros da equipa de cuidados de saúde sobre o uso e administração adequados dos vários agentes quimioterapêuticos. Deve ser adoptada uma abordagem colaborativa multidisciplinar para garantir a aplicação de práticas seguras. A administração de quimioterapia em pacientes requer a formação adequada de pessoal e educação de pacientes e apoio administrativo através da implementação de políticas.2, 23
documentação dos acontecimentos
cada incidente de extravasamento deve ser cuidadosamente documentada e comunicada. A documentação serve vários propósitos, incluindo fornecer uma descrição precisa do que aconteceu, proteger os profissionais de saúde envolvidos, recolher informações sobre extravasamentos e destacar déficits na prática.A documentação e a comunicação às entidades competentes de reacções adversas medicamentosas e erros de medicação é outra forma de os farmacêuticos ajudarem a prevenir acontecimentos futuros. Os dados recolhidos a partir das reacções adversas medicamentosas notificadas e dos erros de medicação podem ser utilizados como ferramentas de aprendizagem para examinar sistemicamente os meios pelos quais estes acontecimentos ocorrem. Os procedimentos e protocolos locais são fundamentais para o reconhecimento e gestão atempados da extravasação e para a prevenção de danos graves nos tecidos. Devem ser envidados esforços de colaboração para assegurar tentativas multidisciplinares atempadas de educar todos os membros da equipa de cuidados de saúde envolvidos na gestão destes doentes, uma vez que o evento tenha ocorrido. Devem ser envidados esforços adicionais para iniciar políticas que impeçam novos acontecimentos. Se estiverem em vigor Políticas, estas deverão ser prontamente disponibilizadas e actualizadas de modo a reflectir as práticas actuais. As orientações de extravasamento de 2007 da European Oncology Nursing Society (EONS) fornecem dados e modelos sugeridos que podem ser utilizados para recolher informações em caso de ocorrência de um caso.Os sinais e sintomas de extravasamento
os sinais e sintomas de extravasamento vesicante incluem inchaço, vermelhidão e/ou desconforto que são frequentemente descritos como queimadura ou picadas. Resistência durante a administração do fármaco, uma perfusão lenta ou lenta, e falta ou perda de retorno de sangue da cânula IV, Porto implantado, ou outro dispositivo Central de acesso venoso podem ser indicadores de que está ocorrendo um extravasamento vesicante.A descoloração e as indurações cutâneas podem progredir ainda mais com o desenvolvimento de bolhas ou necrose e possivelmente ulceração e lesão tecidular profunda. Pode levar vários dias para que toda a extensão do dano epitelial seja realizada. as modalidades de tratamento utilizadas para a gestão do extravasamento vesicante incluem a interrupção imediata da quimioterapia e arrefecimento ou a diluição do local do extravasamento. Para reduzir a morbilidade associada ao extravasamento, é vital que os médicos estejam bem informados sobre os tratamentos disponíveis e trabalhem rapidamente para evitar mais danos aos pacientes. O manejo de extravasamento nãovesicante normalmente inclui a elevação do Membro e resfriamento e geralmente não inclui o uso de terapia farmacológica.A facilidade de intervenção precoce pode ser facilitada pela disponibilização de um kit de extravasamento na instituição. A maioria dos kits de extravasamento contém seringas e cânulas descartáveis, embalagens quentes a frio, gaze, gesso adesivo, Luvas esterilizadas e protectoras e medicamentos para o tratamento da extravasação (por exemplo, hialuronidase, sulfóxido de dimetilo 99%, dexrazoxano). Deve ser incluída no kit uma lista do conteúdo do kit e a verificação regular do conteúdo do medicamento com datas de validade actualizadas deve ser mantida regularmente pelo farmacêutico.2
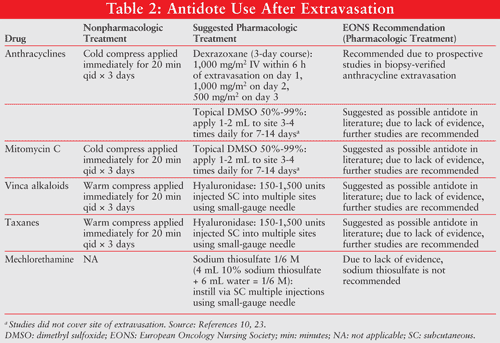
Uma vez que ocorra extravasamento vesicante, o clínico deve interromper imediatamente a perfusão; no entanto, a cânula ou a agulha portadora não corante devem ser mantidas no local e deve ser feita uma tentativa de aspirar o vesicante com uma seringa de 10 mL. A zona de extravasamento deve ser marcada e fotografada; em seguida, a cânula ou agulha deve ser removida e o médico deve ser notificado. Os doentes podem necessitar do uso de analgésicos para ajudar a controlar a dor que possam sentir. Uma vez que as medidas iniciais foram tomadas, é muito importante documentar cuidadosamente a reação adversa ao medicamento e / ou erro de medicação que ocorreu.23 para os alcalóides da vinca, em que é indicada a dispersão ou diluição do vesicante, aplicar calor local durante 20 minutos 4 vezes por dia durante 1 dia durante 2 dias. Para outras extravasações vesicantes, incluindo antraciclinas, o tratamento inicial é orientado para a localização e neutralização do agente extravasado com compressas frias durante 20 minutos 4 vezes por dia durante 1 a 2 dias, limitando a absorção celular destes agentes.23
Tratamento Farmacológico
DMSO: o DMSO é um solvente comum que penetra nos tecidos e aumenta a permeabilidade da pele, o que pode facilitar a absorção de um fármaco extravasado. Quando aplicado topicamente, tem propriedades antioxidantes de radicais livres que podem acelerar a remoção da droga extravasada. DMSO (Rimso-50) está disponível apenas para compra de varejo nos Estados Unidos em uma solução de 50% (vol/vol) em água. Esta solução é aprovada pela FDA apenas para o tratamento da cistite intersticial recorrente.A eficácia do DMSO no tratamento da extravasação por quimioterapia foi descrita pela primeira vez em vários casos notificados e pequenos estudos clínicos.
num caso, uma extravasação de 10 mg de daunorubicina num homem de 42 anos de idade foi tratada com bicarbonato de sódio, dexametasona (4 mg), embalagens de gelo e 1, 5 mL de DMSO tópico 70%, que foi aplicado a cada 3 a 4 horas durante 10 dias. Este regime proporcionou alívio da dor e prevenção de úlceras.25
Olver e Schwarz relataram três casos de resolução de extravasamento com uso de DMSO.Num caso, a aplicação diária de DMSO a 99% durante 14 dias resultou numa resolução completa da dor num período de 2 dias sem ulceração num doente com extravasamento da doxorrubicina. O doente também recebeu bicarbonato de sódio 8, 4% e o tratamento não farmacológico apropriado. (Ver Tabela 2 para Opções não farmacológicas.) Num outro caso, um homem de 49 anos a receber 4 a 6 mg de doxorrubicina foi tratado para extravasamento da doxorrubicina com 5 mL de 8.4% de bicarbonato de sódio, embalagens de gelo e 99% de DMSO aplicados diariamente durante 14 dias. Não ocorreu ulceração; no entanto, ocorreu uma área de 3 x 2, 5 cm de extensão limitante do cotovelo.Num terceiro caso, uma aplicação tópica de 99% DMSO (cada 6 horas durante 1 semana e depois duas vezes por dia durante outra semana) preveniu ulceração; no entanto, a pigmentação residual permaneceu.Berghammer et al também relataram um caso de extravasamento do docetaxel.O extravasato foi diluído com solução salina normal (0, 9%) e tratado com embalagens de gelo. O DMSO foi aplicado 3 vezes a cada 45 minutos, tendo sido administrados corticosteróides orais e diclofenac no dia da extravasação. Todos os sintomas desapareceram em 24 horas; contudo, os sintomas retardados (descoloração castanha, hiperplasia cutânea) apareceram no dia 5 e aumentaram posteriormente. Não foi necessária intervenção cirúrgica plástica. Embora o DMSO em combinação com hipotermia e solução salina isotónica não tenha sido eficaz na prevenção dos sintomas retardados, restringiu a inflamação e a necrose do tecido. Ludwig et al relataram que a utilização de uma mistura de DMSO a 90% e alfa-tocoferol a 10% nas 48 horas seguintes à extravasação de antraciclinas ou mitomicina C em 8 doentes não resultou em ulceração cutânea ou compromisso funcional ou neurovascular.Infelizmente, o alfa-tocoferol não é um agente medicinal facilmente disponível e devem ser realizados outros ensaios aleatórios para validar a sua utilização. num estudo prospectivo com 20 doentes com extravasamentos de antraciclina, 99% DMSO foi administrado duas vezes, 6 vezes por dia durante 2 semanas.Não foram descritas úlceras após o tratamento com DMSO, embora fosse evidente inchaço inicial (85%), eritema (75%) e dor (60%). Após um período de acompanhamento de 3 meses em 16 doentes, 6 (38%) doentes não apresentaram sintomas aparentes e 10 (63%) apresentaram indurações pigmentadas. Bertelli também realizou um estudo prospectivo para avaliar os efeitos do DMSO sobre as extravasamentos de antraciclina.30 a doxorrubicina foi responsável por 11 casos e a epirrubicina foi responsável por 46 casos. Os doentes foram tratados com DMSO 99% a cada 8 horas durante 7 dias. Setenta por cento dos doentes (40/57) apresentaram resolução completa de extravasamento em 1 semana, um doente teve endurecimento residual dos tecidos moles e um doente teve hiperpigmentação residual. nestes casos notificados e em pequenos estudos, as extravasações foram diagnosticadas clinicamente e não por biopsia. O DMSO pode ser uma opção para o tratamento de antraciclinas extravasadas, mitomicina C e actinomicina D. recomenda-se a aplicação de uma camada fina de DMSO na zona extravasada e a sua secagem. Deve aplicar-se um penso não exclusivo dentro de 10 a 25 minutos. Estes passos devem ser repetidos a cada 8 horas durante 7 dias.23 embora o DMSO tenha sido utilizado na prática como uma opção para o tratamento, a falta de ensaios prospectivos pode limitar o seu uso. As orientações para o extravasamento de 2007 da EONS recomendam a realização de estudos adicionais; no entanto, DMSO de 50% a 99% pode ser considerado para uso a critério do clínico.23 é importante notar que nenhum dos estudos prospectivos DMSO utilizou uma ligadura para permitir que a pele absorvesse completamente o DMSO. hialuronidase: Pensa-se que a hialuronidase é capaz de quebrar a matriz extracelular que subjaz às células epiteliais. A matriz mantém grandes quantidades de moléculas de água, e após sua decomposição, é capaz de liberar o fluido para o meio extracelular. No caso de extravasamento, permite o aumento do fluido para o local, diluindo assim a concentração real da pele no local de contato.31,32 hialuronidase foi utilizada no tratamento de extravasamentos de alcalóides da vinca e de taxanos.Foram utilizadas Doses de hialuronidase de 150 a 1500 unidades diluídas em 1 mL de solução salina normal por via subcutânea ou intradérmica no período de 1 hora após a extravasação. num pequeno estudo clínico com 6 doentes com vinblastina (n = 1), vincristina (n = 1) e vinorelbina (n = 4) extravasamento, foram injectadas 250 unidades de hialuronidase no cateter de extracção, ou por via subcutânea (6 injecções) em caso de lesão. Não foram aplicados esteróides ou embalagens frias. A dor resolveu-se nos dias seguintes ao tratamento com hialuronidase em todos os doentes. Um doente queixou-se de uma ligeira endurecimento doloroso 3 meses após a extravasação da vincristina.Estes relatórios revelam informações promissoras; no entanto, existe ainda uma falta global de evidência para o uso de hialuronidase para o tratamento de extravasamentos de alcalóides da vinca. Devem ser realizados mais estudos prospectivos. As orientações para o extravasamento de EONS de 2007 recomendam a realização de estudos adicionais; no entanto, a hialuronidase pode ser considerada como uma opção às doses sugeridas, à discrição do clínico.23 Tiossulfato de sódio: O tiossulfato de sódio previne a alquilação e a destruição dos tecidos, fornecendo um substrato para a alquilação no tecido subcutâneo. Demonstrou-se que o tiossulfato de sódio é eficaz em experiências em animais e, num caso, num relatório para o tratamento da extravasação da mecloretamina (mostarda azotada).33,34 A dose sugerida é de 2 mL de 0,17 M (uma solução de 4 mL de 10% de tiossulfato de sódio e 6 mL de água estéril para injeção). Devido à falta de provas, as orientações para o extravasamento de 2007 da EONS não recomendam este facto como antídoto.22
dexrazoxano: O dexrazoxano (Totect) foi recentemente aprovado pela FDA para o tratamento de extravasamentos induzidos pela antraciclina. O dexrazoxano tem um mecanismo de Acção duplo: 1) actua como quelante do ferro, impedindo a formação de complexos de ferro-antraciclina e radicais hidroxilo mediados pelo ferro que causam danos oxidativos; e 2) estabiliza a topoisomerase II e torna-a inacessível à quimioterapia com antraciclinas. O dexrazoxano bloqueia a enzima de modo a que esta deixe de ser afectada pela antraciclina e previne danos nas células saudáveis do tecido.A eficácia do dexrazoxano foi demonstrada em dois ensaios clínicos realizados na Europa.Ambos os ensaios clínicos foram prospectivos, abertos, multicêntricos, de braço único, conduzidos de julho de 2001 a agosto de 2005, com um total de 80 doentes envolvidos. O primeiro estudo incluiu doentes de 17 locais de cancro na Dinamarca e o segundo envolveu doentes de 34 locais de cancro na Dinamarca, Alemanha, Itália e Países Baixos. A extravasação da antraciclina foi diagnosticada e confirmada através de microscopia de fluorescência do tecido biopsiado, tomada nas 6 horas seguintes ao dexrazoxano. Uma amostra de 32 pacientes avaliáveis foi necessária para mostrar uma redução de 70% ou maior na incidência de cirurgia (teste binomial unilateral, a = .025, ß=.20). O ponto final primário foi a taxa de ressecção cirúrgica e necrose. Cinquenta e quatro dos 80 doentes (estudo 1: n = 18; estudo 2: n = 36) foram avaliáveis (n = 13 biópsias negativas; n = 4 não foram realizadas biopsias; n = 8 violações do protocolo), com uma idade média de 56 anos (intervalo de 34-81 anos). Sessenta e nove por cento (n = 37) dos doentes avaliados eram do sexo feminino. O dexrazoxano foi administrado por perfusão intravenosa durante 1 a 2 horas.; 1.000 mg/m2 em 6 horas; 1. 000 mg/m2 em 24 horas; e 500 mg/m2 em 48 horas de extravasamento.Os doentes com
foram avaliados quanto à eficácia e segurança nos dias 7, 14, 21 e 28, e quanto à eficácia no dia 90, 36 o diagnóstico de cancro mais frequente foi o cancro da mama (50%), seguido de linfoma (39%) e outros tipos de cancro (9%). Os doentes apresentaram extravasamentos de doxorrubicina (n = 23) ou epirrubicina (n = 31). A área média de extravasamento foi de 23, 6 cm2 no estudo 1 e 39 cm2 no estudo 2. Onze doentes apresentaram áreas de extravasamento superiores a 75 cm2. Não houve incidência de cirurgia no estudo 1 e 1 incidente (2, 8%, IC 95% 0, 1% – 14, 5%) no estudo 2. O doente que desenvolveu necrose tecidular devido a extravasamento teve uma área muito grande de extravasamento da doxorrubicina com 253 cm2. Os sintomas aumentaram nos dias após o extravasamento, a necrose do tecido começou a ocorrer 9 dias após o extravasamento do doente, e a necrose foi cirurgicamente excisada. No estudo 1, ocorreu 1 (5, 6%) incidente de necrose devido à biópsia, 6 (33.3%) incidentes de adiamento ou cancelamento do tratamento de câncer programado, e 9 (50%) hospitalizações devido à extravasação. No estudo 2, foi de 1 (2.8%) incidente de necrose devido ao extravasamento, 3 (8.3%) incidentes de necrose devido à biópsia, 10 (27.8%) incidentes de recusa ou de cancelamento do agendada tratamento de câncer, devido ao extravasamento, e 13 (36.1%) incidentes de hospitalização devido ao extravasamento. Em 3 meses de seguimento, de 88,9% (n = 16) não teve sequelas negativas no estudo 1 e 63.9% (n = 23) no estudo 2. Quinze dos 80 doentes apresentaram perturbações sensoriais (n = 9), atrofia cutânea (n = 5), dor (n = 10), desfiguração (n = 1) e limitação (n = 3). A maioria dos doentes (71%) foi capaz de receber tratamento adicional de quimioterapia de acordo com o esquema terapêutico.
Os efeitos adversos mais comuns incluída uma diminuição da contagem de glóbulos brancos (72.5%), diminuição da hemoglobina (42.5%), diminuição da contagem de plaquetas (26%), aumento da aspartato aminotransferase (36.8%), aumento da alanina aminotransferase (23.9%), local de injecção, reacção (27.5%) e náuseas (18.8%).Os resultados dos ensaios clínicos revelaram que o dexrazoxano é um agente eficaz no tratamento de extravasamentos agudos de antraciclinas e na prevenção de sintomas retardados. o quadro 2 apresenta um resumo destas recomendações de tratamento, incluindo as orientações EONS de 2007.
Papel do Farmacêutico
os Farmacêuticos devem estar intimamente envolvidos na avaliação e gestão de todos os induzida por quimioterapia extravasations. Eles podem desempenhar um papel integral de várias maneiras, incluindo: 1) Desenvolvimento de políticas e protocolos; 2) educação do paciente, da família e multidisciplinar; 3) documentação e notificação de extravasamentos e outras reações adversas de medicamentos após a terapia; e 4) monitoramento da dosagem adequada, administração e eficácia do tratamento.
conclusão
todos os estudos analisados envolveram adultos, uma vez que os doentes pediátricos teriam tido um risco aumentado de agitação e tracção das linhas. Até à data, o dexrazoxano é o único agente de extravasamento que foi estudado em grandes, multicêntricos, ensaios prospectivos que utilizaram testes objetivos e confiáveis para diagnosticar casos de extravasamento, o que fornece fortes evidências da utilidade do dexrazoxano. Apesar dos seus usos comuns na prática, outros tratamentos farmacológicos, tais como DMSO e hialuronidase, não foram estudados extensivamente; portanto, faltam recomendações baseadas em evidências. A gestão do extravasamento deve ser conduzida à discrição do clínico, em colaboração com todos os membros da equipa de cuidados de saúde. 1. Infusion Nurse Society. Infusion nursing standards of practice. J Infus Nurs. 2006; 29(suppl 1): S1-S92.
2. Polovich M, White J, Kelleher L. quimioterapia e Biotherapy Guidelines and Recommendations for Practice. 2nd ed. Pittsburgh, PA: Oncology Nursing Society; 2005.
3. Ener RA, Meglathery SB, Styler M. extravasamento de terapias hematocológicas sistémicas. Ann Oncol. 2004;15:858-862.
4. Sauerland C, Egelking C, Wickman R, Corbi D. Vesicant extravasation part I: mechanisms, pathogenesis, and nursing care to reduce risk. Fórum Oncol Nurs. 2006;33:1134-1141.
5. Cassagnol M, Cohen H. Dermatologic toxicities of chemotherapeutic agents. US Pharm. 2008;33(1)(Oncology suppl):10-20.
6. Schulmeister L. Extravasation management. Semin Oncol Nurs. 2007;23:184-190.
7. Viale P. Chemotherapy and cutaneous toxicities: implications for oncology nurses. Semin Oncol Nurs. 2006;22:144-151.
8. Cox K, Stuart-Harris R, Abdini G, et al. The management of cytotoxic-drug extravasation: guide-lines drawn up by a working party for the Clinical Oncological Society of Australia. Med J Aust. 1988;148:185-189.
9. Schrijvers DL. Extravasation: uma terrível complicação da quimioterapia. Ann Oncol. 2003; 14 (suppl 3): iii26-iii30.
10. O Serviço Nacional De Informação Sobre O Extravasamento. www.extravasation.org.uk/home.html. Accessed March 25, 2009.
11. Lemmers N, Gels M, Sleijfer D, et al. Complicações de portas de acesso venoso em 132 doentes com cancro testicular disseminado tratados com poliquemoterapia. J Clin Oncol. 1996;14:2916-2922.
12. Shetty PC, Mody MK, Kastan DJ. Resultado de 350 portas torácicas implantadas por radiologistas interventivos. J Vasc Interv Radiol. 1997;8:991-995.
13. Dorr RT. Antídotos para extravasamentos de quimioterapia vesicante. Blood Rev. 1990; 4: 41-60.
14. Langer SW, Sehested M, Jensen PB. Tratamento da extravasação de antraciclina com dexrazoxano. Clin Cancer Res. 2000;6:3680-3686.
15. Raymond E, Faivre s, Woynarowski JM, Chaney SG. Oxaliplatina: mecanismo de acção e actividade antineoplásica. Semin Oncol. 1998; 2 (suppl 5):4-12.
16. Rivory LP. Novos medicamentos para o cancro colorectal-mecanismos de Acção. Aust Prescr. 2002;25:108-110. www.australianprescriber.com/magazine/25/5/108/10/. Accessed March 25, 2009.
17. Skeel RT. Handbook of Cancer Chemistion. 5th ed. New York, NY: Lippincott Williams & Wilkins; 1999.
18. Boyle DM, Engelking C. Vesicant extravasation: myths and realities. Fórum Oncol Nurs. 1995;22:57-67.
19. Hadaway LC. Prevenção e gestão do extravasamento periférico. Enfermagem. 2004;34:66-67.
20. Shulmeister L, Camp-Sorrell D. extravasamento de quimioterapia de portos implantados. Fórum Oncol Nurs. 2000;27:531-538.
21. Debets JM, Wils JA, Schlangen JT. Uma complicação rara dos dispositivos de acesso central-venoso implantados: fractura do cateter e embolização. Apoio Ao Cancro. 1995;3:432-434.
22. Gorski LA. Oclusões do dispositivo venoso Central. Parte 2: Causas Não-trombóticas e tratamento. Enfermeira Caseira. 2003;21:168-171.
23. Orientações de extravasamento de 2007. European Oncology Nursing Society. www.cancerworld.org/CancerWorld/getStaticModFile.aspx?id=2340. Accessed March 25, 2009.
24. Folheto informativo Rimso-50 (sulfóxido de dimetilo). Lake Forest, IL: Bioniche Pharma USA LLC; 2009.
25. Lawrence HJ, Goodnight SH. Lesão tecidular limitante de sulfóxido de dimetilo causada por extravasamento de agentes doxorrubicina. Ann Intern Med. 1983;98:1025.
26. Olver IN, Schwarz MA. Use of dimethyl sulfoxide in limiting tissue damage caused by extravasation of doxorubicin . Cancer Treat Rep. 1983;67:407-408.
27. Berghammer P, Pohnl R, Baur M, Dittrich C. Docetaxel extravasation. Support Care Cancer. 2001;9:131-134.
28. Ludwig CU, Stoll HR, Obrist R, Obrecht JP. Prevention of cytotoxic drug-induced skin ulcers with dimethyl sulfoxide (DMSO) and alpha-tocopherole. Eur J Cancer Clin Oncol. 1987;23:327-329.
29. Olver IN, Aisner J, Hament A, et al. A prospective study of topical dimethyl sulfoxide for treating anthracycline extravasation. J Clin Oncol.1988;6:1732-1735.
30. Bertelli G. Prevention and management of extravasation of cytotoxic drugs. Drug Saf. 1995;12:245-255.
31. Balazs EA, Laurent TC, Jeanloz RW. Nomenclature of hyaluronic acid. Biochem J. 1986;235:903.
32. Girish KS, Kemparaju K. The magic glue hyaluronan and its eraser hyaluronidase. Life Sci. 2007;80:1921-1943.
33. Dorr T. Antidotes to vesicant chemotherapy extravasations. Blood Rev. 1990;4:41-60.
34. Owen OE, Dellatorre DL, Van Scott EJ, Cohen MR. Accidental intramuscular injection of mechlorethamine. Cancer. 1980;45:2225-2226.
35. Totect (dexrazoxane for injection) package insert. Copenhagen, Denmark: TopoTarget A/S; October 2007.
36. Mouridsen HT, Langer SW, Buter J, et al. Treatment of anthracycline extravasation with Savene (dexrazoxane). Results from two prospective clinical multicenter studies. Ann Oncol. 2007;18:546-550.
Leave a Reply