3.4: o Experimento de Rutherford – O Modelo Nuclear do Átomo
e Átomos de Ouro
Em 1911, Rutherford e colegas de trabalho Hans Geiger e Ernest Marsden iniciou uma série de experiências inovadoras que iria mudar completamente o modelo aceito de um átomo. Bombardearam folhas muito finas de folha de ouro com partículas alfa em movimento rápido.


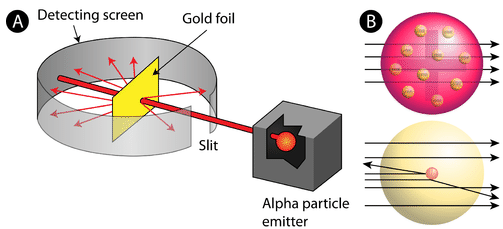
Figura \(\PageIndex{2}\) (A) A configuração do experimento de Rutherford com a folha de ouro experimento: Um elemento radioativo que emite partículas alfa foi dirigido para uma folha fina folha de ouro, que estava cercado por uma tela que permita a detecção do desviou de partículas. B) de acordo com o modelo de pudim de ameixa (top), todas as partículas alfa deveriam ter passado pela folha de ouro com pouca ou nenhuma deflexão. Rutherford descobriu que uma pequena percentagem de partículas alfa eram deflectidas em grandes ângulos, o que poderia ser explicado por um átomo com um núcleo muito pequeno, denso e positivamente carregado no seu centro (fundo).de acordo com o modelo atômico aceite, no qual a massa e carga de um átomo são uniformemente distribuídas por todo o átomo, os cientistas esperavam que todas as partículas alfa passassem pela folha de ouro com apenas uma ligeira deflexão ou nenhuma. Surpreendentemente, como mostrado na figura \(\PageIndex{2}\) (enquanto a maioria das partículas alfa não foram detectadas, uma percentagem muito pequena (cerca de 1 em 8000 partículas) saltou da folha de ouro em ângulos muito grandes. Alguns até foram redirecionados para a fonte. Nenhum conhecimento prévio os tinha preparado para esta descoberta. Em uma famosa citação, Rutherford exclamou que era “como se você tivesse disparado uma concha de 15 polegadas em um pedaço de tecido e ele voltou e bateu em você.”
Rutherford neededed to come up with an entirely new model of the atom in order to explain his results. Como a grande maioria das partículas alfa tinha passado pelo ouro, ele argumentou que a maior parte do átomo era espaço vazio. Em contraste, as partículas que foram altamente deflectidas devem ter experimentado uma força tremendamente poderosa dentro do átomo. Ele concluiu que toda a carga positiva e a maioria da massa do átomo devem ser concentradas num espaço muito pequeno no interior do átomo, que ele chamou de núcleo. O núcleo é o minúsculo, denso, núcleo central do átomo e é composto por prótons e nêutrons.o modelo atômico de Rutherford ficou conhecido como o modelo nuclear. No átomo nuclear, os prótons e nêutrons, que compõem quase toda a massa do átomo, estão localizados no núcleo no centro do átomo. Os elétrons são distribuídos em torno do núcleo e ocupam a maior parte do volume do átomo. Vale a pena enfatizar quão pequeno o núcleo é comparado com o resto do átomo. Se pudéssemos explodir um átomo para ser do tamanho de um grande estádio de futebol profissional, o núcleo seria do tamanho de um mármore.o modelo de Rutherford provou ser um passo importante para a plena compreensão do átomo. No entanto, não abordou completamente a natureza dos elétrons e a forma como ocupavam o vasto espaço em torno do núcleo. Por este e outros insights, Rutherford foi premiado com o Prêmio Nobel de Química em 1908. Infelizmente, Rutherford teria preferido receber o Prêmio Nobel de Física porque considerava a física superior à química. Em sua opinião, ” toda a ciência é física ou coleta de selos.”
Leave a Reply