13.7: Compostos Aromáticos – Benzeno
os Objectivos de Aprendizagem
- Para descrever a ligação em benzeno e a forma como as reações típicas de benzeno diferentes daqueles dos alcenos.
em seguida, consideramos uma classe de hidrocarbonetos com fórmulas moleculares como as dos hidrocarbonetos insaturados, mas que, ao contrário dos alcenos, não sofrem prontamente reações de adição. Estes compostos compreendem uma classe distinta, denominada hidrocarbonetos aromáticos, com estruturas e propriedades únicas. Começamos com o mais simples destes compostos. O benzeno (C6H6) é de grande importância comercial, mas também tem efeitos notáveis na saúde.
a fórmula C6H6 parece indicar que o benzeno tem um alto grau de insolação. (Hexano, the saturated hydrocarbon with six carbon atoms has the formula C6H14—eight more hydrogen atoms than benzene.) No entanto, apesar do aparente baixo nível de saturação, o benzeno é pouco reativo. Não reage facilmente, por exemplo, com o bromo, que é um teste de não-maturação.
benzeno é um líquido que cheira a gasolina, ferve a 80°C, e congela a 5,5°C. É o hidrocarboneto aromático produzido no maior volume. Foi usado anteriormente para descafeinar café e foi um componente significativo de muitos produtos de consumo, tais como decapantes de tinta, cimentos de borracha, e removedores de locais de limpeza a seco em casa. Ele foi removido de muitas formulações de produtos na década de 1950, mas outros continuaram a usar benzeno em produtos até a década de 1970, quando foi associado com mortes de leucemia. O benzeno ainda é importante na indústria como um precursor na produção de plásticos (como o isopor e nylon), drogas, detergentes, borracha sintética, pesticidas e corantes. É usado como solvente para coisas como limpeza e manutenção de equipamentos de impressão e para adesivos, tais como os utilizados para prender solas aos sapatos. Benzeno é um constituinte natural de produtos petrolíferos, mas por ser um carcinógeno conhecido, seu uso como aditivo na gasolina é agora limitado.
para explicar as surpreendentes propriedades do benzeno, os químicos supõem que a molécula tem uma estrutura cíclica, hexagonal, planar de seis átomos de carbono com um átomo de hidrogênio ligado a cada um. Podemos escrever uma estrutura com ligações simples e duplas alternadas, seja como uma fórmula estrutural completa ou como uma fórmula de ângulo de linha:

No entanto, estas estruturas não explicam as propriedades únicas do benzeno. Além disso, evidências experimentais indicam que todas as ligações carbono-carbono no benzeno são equivalentes, e a molécula é anormalmente estável. Químicos muitas vezes representam benzeno como um hexágono com um círculo inscrito:
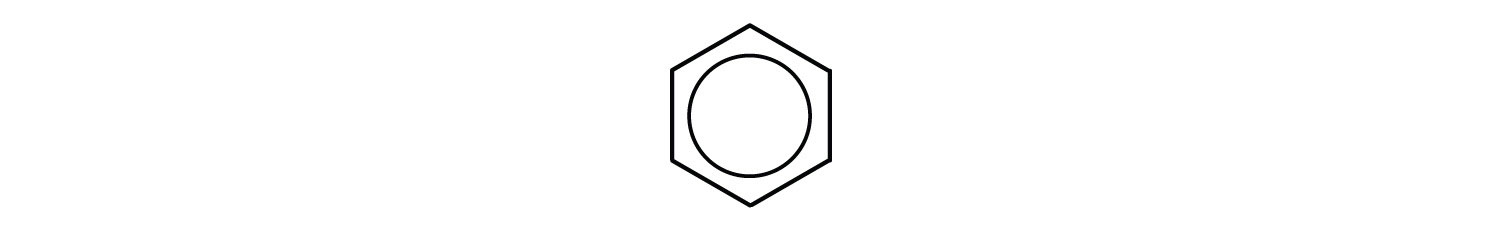
o círculo interno indica que os elétrons de Valência são compartilhados igualmente por todos os seis átomos de carbono (ou seja, os elétrons são deslocalizados, ou espalhados, sobre todos os átomos de carbono). Entende-se que cada canto do hexágono é ocupado por um átomo de carbono, e cada átomo de carbono tem um átomo de hidrogénio ligado a ele. Qualquer outro átomo ou grupos de átomos substituídos por um átomo de hidrogênio deve ser mostrado ligado a um canto particular do hexágono. Nós usamos esse simbolismo moderno, mas muitos cientistas ainda usam a estrutura anterior com ligações duplas e únicas alternativas.A maior parte do benzeno utilizado comercialmente provém do petróleo. É utilizado como material de base para a produção de detergentes, drogas, corantes, insecticidas e Plásticos. Uma vez amplamente utilizado como um solvente orgânico, o benzeno é agora conhecido por ter efeitos tóxicos a curto e longo prazo. A inalação de grandes concentrações pode causar náuseas e até mesmo morte devido a insuficiência respiratória ou cardíaca, enquanto a exposição repetida leva a uma doença progressiva na qual a capacidade da medula óssea para fazer novas células sanguíneas é eventualmente destruída. Isto resulta em uma condição chamada anemia aplástica, na qual há uma diminuição no número de glóbulos vermelhos e brancos.como é que as reacções típicas do benzeno diferem das dos alcenos?
Answers
- benzeno is rather unreactive toward addition reactions compared to an alkene.elétrons de Valência são compartilhados igualmente por todos os seis átomos de carbono (ou seja, os elétrons são deslocalizados).os seis elétrons são compartilhados igualmente por todos os seis átomos de carbono.os hidrocarbonetos aromáticos parecem não saturados, mas têm um tipo especial de ligação e não sofrem reacções de adição.exercícios
- desenhar a estrutura do benzeno como se tivesse ligações únicas e duplas alternativas.
- desenhe a estrutura do benzeno como os químicos geralmente o representam hoje em dia.

Leave a Reply