węgiel: podstawowe
węgiel jest pierwiastkiem grupy 14 i jest szeroko rozpowszechniony w przyrodzie. Występuje w obfitości w słońcu, gwiazdach, kometach i atmosferach większości Planet. Węgiel jest obecny w atmosferze jako dwutlenek węgla i rozpuszcza się we wszystkich naturalnych wodach. Jest składnikiem skał jako węglany wapnia (wapienia), magnezu i żelaza. Atmosfera Marsa jest bardzo cienka, ale to, co tam jest, zawiera około 95% CO2.
węgiel, ropa naftowa i gaz ziemny to głównie węglowodory. Węgiel jest unikalny wśród pierwiastków w ogromnej liczbie różnorodnych związków, które może tworzyć. Chemia organiczna, 1/112 podzbiór chemii nieorganicznej, to badanie węgla i jego związków. Chociaż krzem może zastąpić węgiel w tworzeniu wielu pokrewnych związków, obecnie nie jest możliwe tworzenie stabilnych związków o bardzo długich łańcuchach atomów krzemu.
węgiel znajduje się wolny w przyrodzie w trzech formach alotropowych: amorficznym, Grafitowym i diamentowym. Grafit jest jednym z najdelikatniejszych znanych materiałów, podczas gdy diament jest jednym z najtrudniejszych. Węgiel, jako mikroskopijne diamenty, znajduje się w niektórych meteorytach. Naturalne diamenty znajdują się w starożytnych wulkanicznych „rurach”, takich jak Znalezione w RPA. Diamenty są również odzyskiwane z dna oceanu przy Przylądku Dobrej Nadziei.

pierścionek z brylantem.
niedawno odkryto inną formę węgla, buckminsterfullerene, C60. Ta forma węgla jest dziś przedmiotem wielkiego zainteresowania laboratoriów badawczych.
Czysty węgiel jest dostępny w wielu różnych formach (alotropach). Najczęstszą formą czystego węgla jest α-grafit. Jest to również najbardziej stabilna termodynamicznie forma. Diament jest drugą formą węgla, ale jest znacznie mniej powszechny. Inne formy węgla obejmują fulereny. Podczas gdy diament i grafit są nieskończonymi kratami, fulereny, takie jak buckminsterfullerene, C60, są dyskretnym gatunkiem molekularnym. Amorficzne formy węgla, takie jak sadza i lampblack, są materiałami składającymi się z bardzo małych cząstek grafitu.
Większość grafitu jest α-grafitem i posiada strukturę warstwową, w której każdy węgiel jest bezpośrednio związany z trzema innymi atomami węgla w odległości 141,5 pm. Delokalizacja w wiązaniu jest widoczna, ponieważ odległości C-C są równe i krótsze niż normalne wiązania pojedyncze węgiel-węgiel (typowo 154 pm). Odległość między warstwami atomów węgla wynosi 335,4 pm. W większości grafitów (α-grafit) warstwy atomów są ułożone w ABABAB… powtórz modę, ale forma β (rombohedralna) układanie jest ABCABCABC… chociaż odległości węgiel-węgiel i odstęp między warstwami pozostają takie same jak w postaci α. Różnica entalpii między α-i α-grafitem jest mniejsza niż 1 kJ mol-1 (0,59 ± 0,17 kJ mol-1. Formy cięższych pierwiastków odpowiadających grafitowi nie są znane, a struktury krzemu, germanu i szarej cyny są związane ze strukturą diamentu (poniżej).

układy atomowe w najczęstszych przydziałach węgla: α-grafit.
ponieważ diament ma nieco bardziej zwartą strukturę, jego gęstość jest większa niż grafitu. Wygląd diamentu jest dobrze znany i jest również jednym z najtwardszych znanych materiałów. Podobnie jak grafit, jest stosunkowo niereaktywny, ale pali się w powietrzu w temperaturze 600-800°C. Każdy atom węgla jest związany z czterema sąsiadami w odległości 154,45 pm w sposób czworościenny, więc każdy diamentowy kryształ jest pojedynczą gigantyczną strukturą sieciową. W zasadzie (i w praktyce!) grafit można przekształcić w diament poprzez zastosowanie ciepła i ciśnienia. Komórka jednostkowa diamentu jest sześcienna z a = 356,68 pm. Prawie wszystkie diamenty posiadają tę strukturę, ale bardzo mały procent wykazuje sześciokątną strukturę związaną z wurtzytem i są one nazywane lonsdaleitem.

Struktura kryształu diamentu.
Ostatnio scharakteryzowano inną alotropę węgla. Podczas gdy diament i grafit są nieskończonymi kratami, buckminsterfullerene, C60, jest dyskretnym gatunkiem molekularnym. Cząsteczka buckminsterfullerene to sieć 12 pięciokątów i 20 sześciokątów złożonych w kulę. Efekt jest bardzo podobny do patchworku z 12 pięciokątnych i 20 sześciokątnych kawałków skóry, które zszyte razem tworzą piłkę nożną (piłkę nożną). Nazwa buckminsterfullerene (lub buckyball została wymyślona ze względu na związek między konstrukcją kopuł geodezyjnych C60 a projektami kopuł geodezyjnych R. Buckminster Fuller. Buckminsterfullerene jest obecnie dostępny na rynku i został również zidentyfikowany w przestrzeni międzygwiezdnej i sadzy.
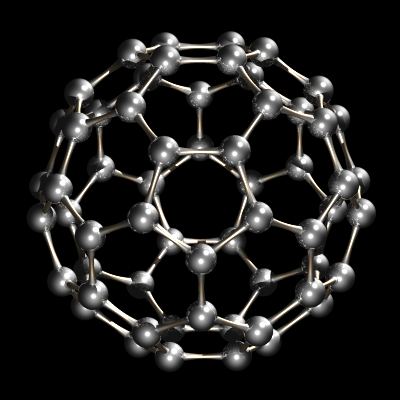
C60, Buckminsterfullerene.
Inne fulereny (zamknięte klatki węglowe), takie jak C60 i C84, są również znane i dostępne w handlu. Najmniejszym możliwym fulerenem jest dwunastościan C20, składający się z 12 pięciokątów i żadnego sześciokąta. Nanorurki są związane z fulerenami. Są to rury dające wygląd walcowanego grafitu, chociaż są wykonane z grafitu. Są one otwarte, podczas gdy fulereny są strukturami zamkniętymi.
ciekawą cechą fulerenów jest ich zdolność do zamykania atomów takich jak potas i inne metale alkaliczne w celu tworzenia struktur endohedrycznych oznaczonych jako K@C60.
w 1961 roku Międzynarodowa Unia Chemii Czystej i Stosowanej (IUPAC) przyjęła izotop 12C jako podstawę masy atomowej. Węgiel-14, 14C, izotop o okresie półtrwania 5730 lat, jest używany do datowania takich materiałów jak drewno, okazy archeologiczne itp. Węgiel-13, 13C, jest szczególnie przydatny w badaniach znakowania izotopowego, ponieważ nie jest radioaktywny, ale jest jądrem spinu i = 1/2, a zatem dobrym jądrem NMR.
Leave a Reply