Leczenie pierwszego rzutu raka prostaty opornego na kastrat z przerzutami
w 2019 r.rak prostaty (PCA) stanowi prawie 1 na 5 nowych diagnoz raka u mężczyzn w USA.1 w ciągu ostatnich kilku lat ogólny wskaźnik zachorowalności na raka prostaty (PCA) zmniejszył się o około 7% rocznie.1 gwałtowny spadek częstości występowania jest powszechnie przypisywany zmniejszonemu testowi antygenu specyficznego dla prostaty (PSA) w latach 2008-2013. Zmniejszenie stosowania badań przesiewowych PSA było spowodowane zaleceniami United States (US) Preventive Services Task Force przeciwko rutynowym badaniom przesiewowym PSA. Było to zalecenie Klasy D szczególnie u mężczyzn w wieku 75 lat i starszych, które zostało ogłoszone w 2008 r., a później rozszerzone na wszystkich mężczyzn w 2011 r., z powodu rosnących obaw związanych z nadmierną diagnozą i nadmiernym leczeniem.2 chociaż częstość występowania testów PSA przestała się zmniejszać i ustabilizowała w latach 2013-2015, 3 wpływ zmniejszenia badań przesiewowych na częstość występowania zaawansowanej choroby jest nadal niejasny. Analiza dużego Rejestru Nowotworów obejmującego 89% populacji Stanów Zjednoczonych wykazała, że ogólny spadek zachorowalności na PCa jest w rzeczywistości maskowaniem wzrostu diagnoz w odległym stadium od 2010 r. w każdym wieku i rasy.
niezależnie od zastosowanego leczenia, około 20% – 30% pacjentów z miejscową PCa przechodzi w chorobę przerzutową, często leczoną terapią hormonalną.5 można to podać poprzez chirurgiczną kastrację (obustronna orchiektomia) lub kastrację medyczną z zastosowaniem terapii deprywacji androgenów (ADT). Obie metody osiągają poziom kastratu testosteronu w surowicy, który jest uważany za standard opieki w leczeniu PCA wrażliwego na hormony z przerzutami (mHSPC). Jednak mHSPC jest przeznaczony do postępu do przerzutowego raka prostaty opornego na kastrat (mCRPC).6 Stan opornego na kastrat raka prostaty (CRPC) definiuje się jako progresję choroby pomimo osiągnięcia poziomu testosteronu w surowicy (testosteron w surowicy < 50 ng/dL lub 1.7 nmol / L) i może występować jako ciągły wzrost stężenia PSA w surowicy, progresja istniejącej wcześniej choroby i (lub) pojawienie się nowych przerzutów.Mediana przeżycia CRPC wynosi około trzech lat8 i wiąże się ze znacznym pogorszeniem jakości życia.9 dokładny mechanizm przejścia z mHSPC do mCRPC jest nadal niejasny. Wiadomo jednak, że pomimo poziomu androgenów kastratu, receptor androgenowy (AR) pozostaje aktywny i nadal napędza progresję PCa w CRPC.10 doprowadziło to do opracowania nowych środków mających na celu dalsze zmniejszenie produkcji androgenów lub blokowanie funkcji AR. Istnieją jednak inne szlaki biologiczne, które działają niezależnie od sygnalizacji androgenowej, a także powodują CRPC.
w opcjach leczenia przestrzeni mHSPC wystąpiło kilka istotnych zmian, które przyniosły znaczne korzyści w zakresie przeżycia (patrz link „szybko rozwijająca się strategia zarządzania przerzutowym hormonalnym rakiem gruczołu krokowego”), w tym wprowadzenie chemioterapii w badaniu CHAARTED11 i badaniu STAMPEDE,12 dodanie octanu abirateronu i prednizonu w badaniu LATITUDE,13 i badaniu STAMPEDE, 14 dodanie enzalutamidu w badaniu ARCHES15 i badaniu ENZAMET, 16 i wreszcie dodanie octanu abirateronu i prednizonu w badaniu Stampede, 14 dodanie enzalutamidu w badaniu ARCHES apalutamid, doustny niesteroidowy antyandrogen, który jak enzalutamid wiąże się bezpośrednio z domeną wiążącą ligand AR i zapobiega translokacji AR, wiązaniu DNA i transkrypcji za pośrednictwem AR.Badanie TITAN wykazało korzyść z przeżycia całkowitego (OS) u pacjentów z mHSPC leczonych apalutamidem.Apalutamid wykazywał również korzyść w porównaniu z placebo w badaniu klinicznym bez przerzutów CRPC (NMCRP) w badaniu kontrolowanym placebo fazy 3 SPARTAN,19 podobnie jak korzyść wykazywana u pacjentów bezmetastatycznego opornego na kastrat raka prostaty (nmcrpc) leczonych enzalutamidem, w badaniu PROSPER20 (patrz „nowe metody leczenia raka prostaty opornego na kastrat bez przerzutów” link). Te postępy w leczeniu mHSPC i nmcrpc wzbudziły pytanie, jakie opcje leczenia powinny być oferowane pacjentom w leczeniu mCRPC.
leczenie mężczyzn z CRPC zmieniło się diametralnie w ciągu ostatnich 15 lat. Przed 2004 r., gdy pacjenci nie wykonywali pierwotnej ADT, leczenie stosowano wyłącznie w celu paliacji. Przełomowe próby Tannocka i wsp.22 oraz Petrylak i in.W 2004 r.po raz pierwszy wprowadzono chemioterapię docetakselem u pacjentów z mCRPC, u których wykazano poprawę przeżycia. Jednakże, ponieważ docetaksel został zatwierdzony przez FDA, na podstawie randomizowanych badań klinicznych zatwierdzono pięć dodatkowych korzystnych czynników wykazujących przewagę przeżycia (Tabela 1). Należą do nich enzalutamid i abirateron, które szczególnie wpływają na oś androgenową, sipuleucel-T, który stymuluje układ odpornościowy; 24 kabazytaksel, który jest innym chemioterapeutykiem; 25 i rad-223, terapia radionuklidem.26 Inne metody leczenia mCRPC wykazały poprawę wyników, ale zostały jeszcze zatwierdzone przez FDA i zostaną omówione w innym przeglądzie. Ze względu na znaczny wzrost liczby zatwierdzonych przez FDA środków terapeutycznych u pacjentów z CRPC, klinicyści są kwestionowani z mnóstwem opcji leczenia i mnogością potencjalnych sekwencji tych środków, co znacznie bardziej złożone jest podejmowanie decyzji klinicznych w mCRPC.
Tabela 1. Środki zatwierdzone do leczenia opornego na kastrat raka prostaty z przerzutami w USA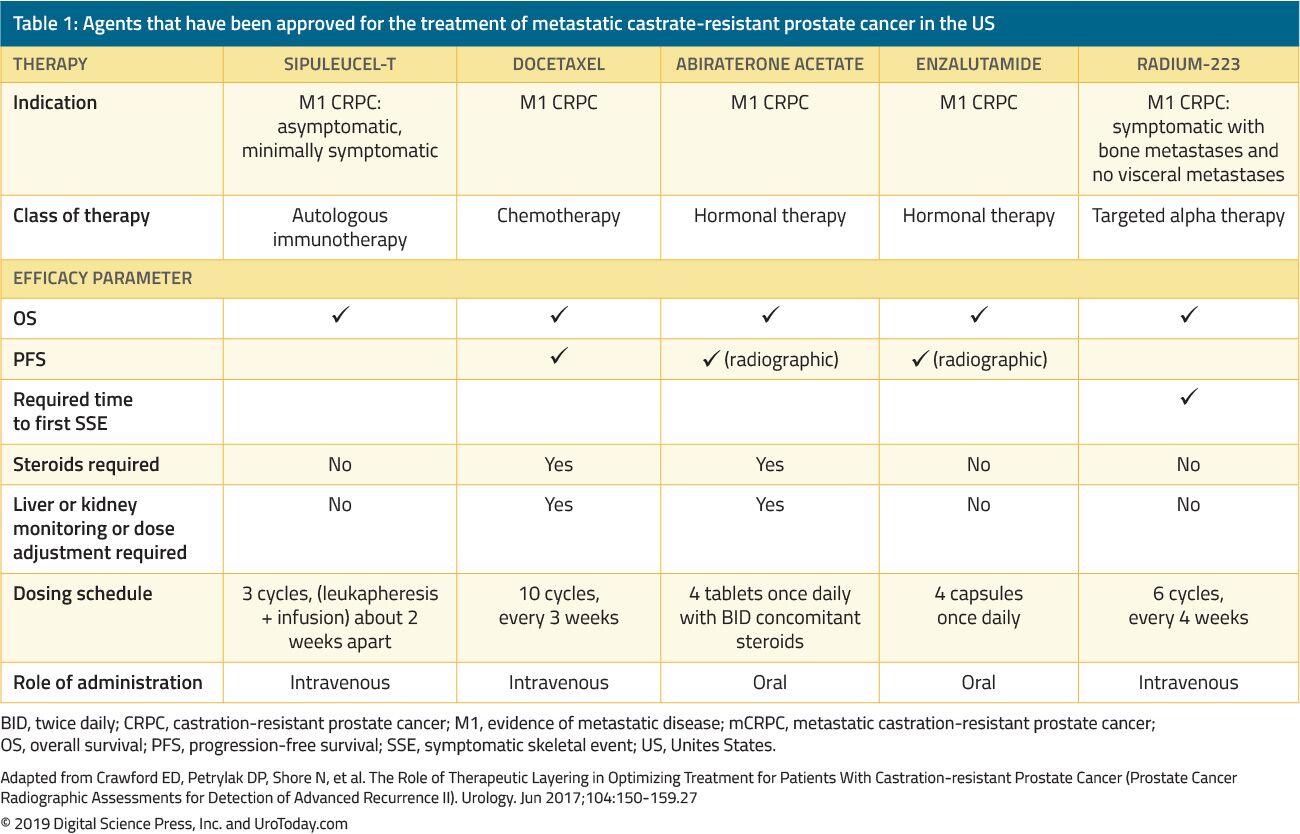
mCRPC jest zwykle chorobą wyniszczającą, a pacjenci najprawdopodobniej skorzystają ze strategii zarządzania sformalizowanej przez multidyscyplinarny zespół składający się z urologów, onkologów medycznych, onkologów radiologicznych, pielęgniarek, psychologów i pracowników socjalnych.Konieczne jest omówienie możliwości leczenia paliacji, rozważając dodatkowe leczenie ogólnoustrojowe, w tym leczenie bólu, zaparć, anoreksji, nudności, depresji i zmęczenia.
innym ważnym punktem do rozważenia przy ustalaniu odpowiedniej sekwencji leczenia w tej przestrzeni choroby jest związany z tym koszt. Stosując modele obejmujące dodatkowe linie leczenia przed lub po docetakselu, średni koszt leczenia mCRPC w średnim okresie 28,1 miesiąca wynosił około 48 000 USD na pacjenta.Koszt ten jest dość wysoki ze względu na fakt, że pacjenci mogą otrzymywać wiele linii terapii i ponosić bieżące usługi medyczne w trakcie choroby.
tylko w dwóch badaniach wykazano marginalną korzyść z przeżycia u pacjentów pozostających na analogach LHRH zamiast dodawać terapię drugiego i trzeciego rzutu.31, 32 badania wykazały, że CRPC nie jest oporny na ADT, ale raczej nadwrażliwy na niego.Ciśnienie selekcyjne zależne od leczenia podczas ADT powoduje wzmocnienie AR i zapewnia, że sytuacja nie ulegnie eskalacji, ADT jest nadal podawany w Warunkach mCRPC. Presja selekcji mediowana przez leczenie trwa również przez cały okres życia guza, nasilając potrzebę prawidłowej sekwencji terapii. Jednak ze względu na brak danych prospektywnych, potencjalne korzyści wynikające z kontynuowania kastracji nadal przewyższają minimalne ryzyko związane z tym leczeniem. Ponadto, wszystkie następnie zatwierdzone terapie zostały zbadane u mężczyzn z trwającą ADT, dodając kolejny powód, dla którego należy kontynuować leczenie.
przed zagłębianiem się w faktyczne dostępne opcje leczenia, ważne jest, aby uznać, że nadal nie jest jasne, kiedy rozpocząć leczenie u pacjentów z mCRPC, którzy są całkowicie bezobjawowi. Nie wiadomo jeszcze, czy wcześniejsze leczenie jest lepsze, czy też należy poczekać, aż pacjent stanie się objawowy i rozwinie ból. Przed rozpoczęciem leczenia należy wziąć pod uwagę istniejące choroby współistniejące pacjenta i spodziewane niepożądane skutki rozpoczęcia leczenia. Pacjenci z mCRPC we wczesnym stadium zaawansowania w badaniu COU-AA-302, którzy otrzymywali abirateron, zazwyczaj przeżywali prawie rok dłużej niż pacjenci, którzy otrzymywali placebo (mediana OS, odpowiednio 53,6 miesiąca w porównaniu do 41,8 miesiąca, HR, 0,61; 95% CI, 0,43 do 0,87; p = .006).Tak więc, pacjenci we wczesnym stadium mCRPC odnosili korzyści z wcześniejszego rozpoczęcia stosowania abirateronu. W tym samym badaniu pacjenci z bezobjawowym lub lekko objawowym mCRPC, z wyjściowym stężeniem PSA < 15,6 ng/mL abirateron również powodowali szybsze tempo i większy stopień spadku stężenia PSA niż placebo.Chociaż obecnie dostępne dane są ograniczone, najprawdopodobniej sugerują, że rozpoczęcie leczenia wcześniej niż później jest bardziej korzystne.33,34
zatwierdzone opcje leczenia pierwszego rzutu raka gruczołu krokowego opornego na kastrat z przerzutami
Abirateron
Abirateron jest antyandrogenem, który jest inhibitorem enzymu 17α-hydroksylazy/C17, 20-liazy (CYP17). W badaniu III fazy COU-AA-302 oceniano abirateron u 1 088 wcześniej nieleczonych chemio, bezobjawowych lub lekko objawowych pacjentów z mCRPC bez przerzutów do narządów wewnętrznych. W tym badaniu pacjentów randomizowano do grupy otrzymującej octan abirateronu lub placebo, oba w skojarzeniu z prednizonem 35 (rycina 1). Pacjenci byli stratyfikowani przez Eastern Cooperative Oncology Group (ECOG) w stanie sprawności 0 LUB 1 oraz przez chorobę bezobjawową lub lekko objawową.35 OS i radiograficzne przeżycie wolne od progresji (rpfs) były głównymi punktami końcowymi. W badaniu wykazano, że po medianie okresu obserwacji wynoszącej 22,2 miesięcy wystąpiła znacząca poprawa rPFS w grupie otrzymującej abirateron(mediana 16,5 w porównaniu do 8,2 miesiąca, HR 0,52, p < 0,001). W końcowej analizie po medianie obserwacji wynoszącej 49,2 miesięcy, punkt końcowy OS był istotnie dodatni (34,7 vs. 30,3 miesięcy, HR: 0,81, 95% CI: 0,70-0,93, p = 0,0033).Należy pamiętać, że mCRPC obejmuje szerokie spektrum prognostyczne, nawet jeśli nie był wcześniej leczony chemioterapią.W analizie grupy abirateronu w badaniu COU-AA-302, mediana OS wynosiła 42,6 miesiąca u pacjentów, u których nie stwierdzono bólu na początku badania, prawidłowej aktywności fosfatazy zasadowej i LDH oraz mniej niż 10 przerzutów do kości.Jednak u pacjentów z większą liczbą czynników ryzyka progresji mediana OS była istotnie krótsza.Oceniając profil toksyczności abirateronu, wydawało się, że wywołuje on Więcej działań niepożądanych związanych z nadmiarem mineralokortykoidów i zaburzeniami czynności wątroby, ale były to głównie działania niepożądane o nasileniu 1-2. Wreszcie, abirateron okazał się równie skuteczny w populacji osób w podeszłym wieku (> 75 lat).38
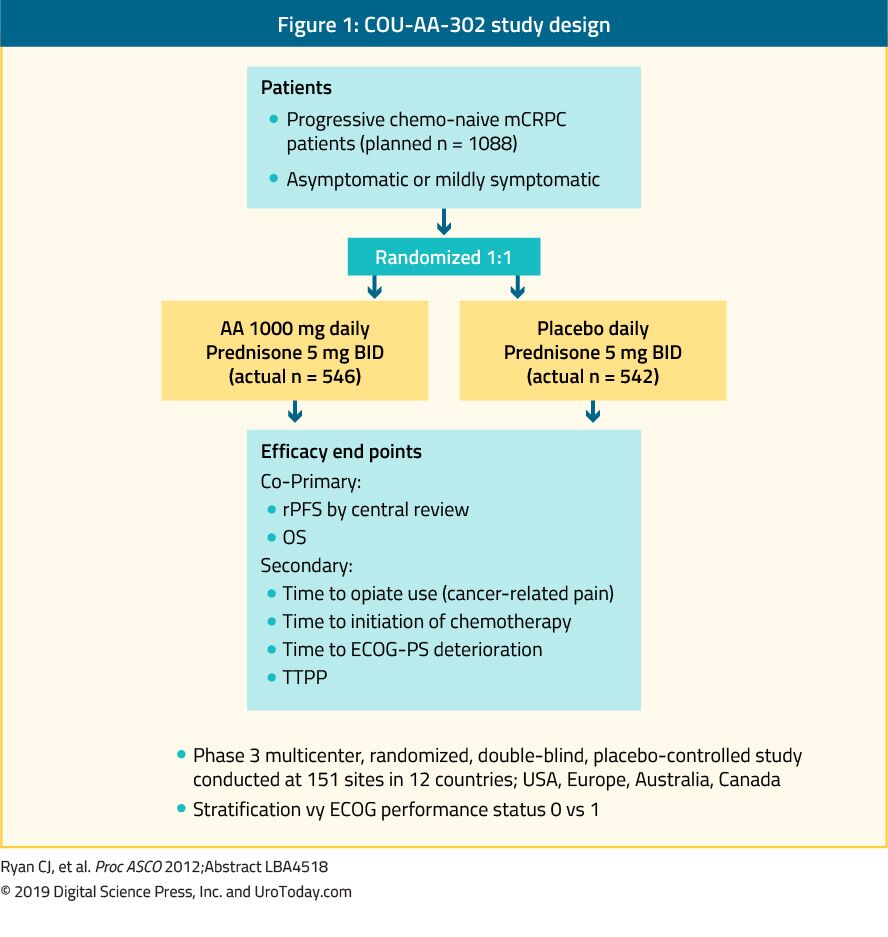
Rysunek 1. Projekt badania COU-AA-302
Enzalutamid
Enzalutamid jest niesteroidowym antyandrogenem. Do badania PREVAIL, które jest randomizowanym badaniem III fazy, zakwalifikowano 1717 pacjentów z mCRPC nieleczonych wcześniej chemioterapią oraz pacjentów z przerzutami do narządów wewnętrznych.W badaniu tym porównywano enzalutamid z placebo (rycina 2). W badaniu PREVAIL wykazano istotną poprawę u pacjentów leczonych enzalutamidem w obu pierwotnych punktach końcowych, w tym rPFS (HR: 0,186; CI: 0,15-0,23, p < 0,0001) i OS (HR: 0,706; CI: 0,6-0,84, p < 0, 001). Przedłużona obserwacja i analiza końcowa potwierdziły korzyść w OS i RPF dla enzalutamidu.U 78% pacjentów leczonych enzalutamidem odnotowano zmniejszenie stężenia PSA o ponad 50%. Najczęstszymi klinicznie istotnymi działaniami niepożądanymi były zmęczenie i nadciśnienie tętnicze. Enzalutamid był równie skuteczny i dobrze tolerowany u starszych mężczyzn (> 75 lat)41 oraz u osób z przerzutami do narządów wewnętrznych lub bez nich.Jednak u mężczyzn z przerzutami do wątroby nie było widocznych korzyści.W badaniu TERRAIN porównywano enzalutamid z bikalutamidem, starszym lekiem antyandrogenowym, w randomizowanym badaniu fazy II z podwójnie ślepą próbą, wykazując znaczącą poprawę PFS (15.7 months vs. 5.8 months, HR: 0.44, p < 0.0001) in favor of enzalutamide.44
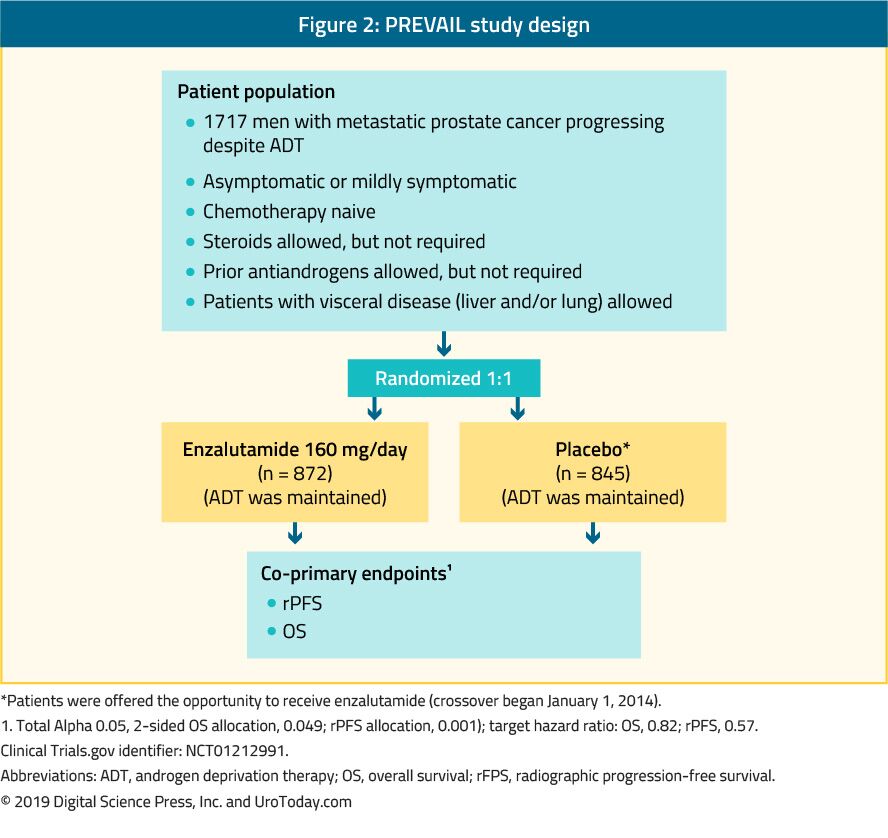
Figure 2. PREVAIL study design
Docetaxel
The landmark trial TAX 327 showed a significant improvement in median OS of 2-2.9 months in mCRPC patients treated with docetaxel-based chemotherapy when compared to patients who were treated with mitoxantrone plus prednisone therapy.22 The SWOG 9916 trial compared mitoxantrone to docetaxel and showed similar results23 (Figure 3). Standardową chemioterapią pierwszego rzutu jest docetaksel w dawce 75 mg / m2 pc. w trzech dawkach tygodniowych w skojarzeniu z prednizonem w dawce 5 mg dwa razy na dobę, do dziesięciu cykli. Podczas podawania docetakselu należy wziąć pod uwagę kilka ważnych czynników prognostycznych: przerzuty trzewne, ból, niedokrwistość (Hb < 13 g/dL), progresję skanów kości i wcześniejsze leczenie estramustyną. Te czynniki prognostyczne mogą przyczynić się do rozwarstwienia odpowiedzi na docetaksel. Korzystając z tych czynników prognostycznych, chorobę można podzielić na niskie, pośrednie i wysokie ryzyko, przy czym mediana OS różni się znacząco od 25.Odpowiednio 7, 18, 7 i 12, 8 miesiąca.Chociaż sam wiek nie jest przeciwwskazaniem do leczenia docetakselem, pacjenci muszą być wystarczająco sprawni, aby wytrzymać ten rodzaj leczenia, a choroby współistniejące należy ocenić przed rozpoczęciem leczenia. U mężczyzn, u których uważa się, że nie są w stanie tolerować standardowej dawki i schematu leczenia docetakselem, można ją zmniejszyć z 75 do 50 mg/m2 pc.co dwa tygodnie, wykazując mniej działań niepożądanych stopnia 3-4 i dłuższy czas do niepowodzenia leczenia.46
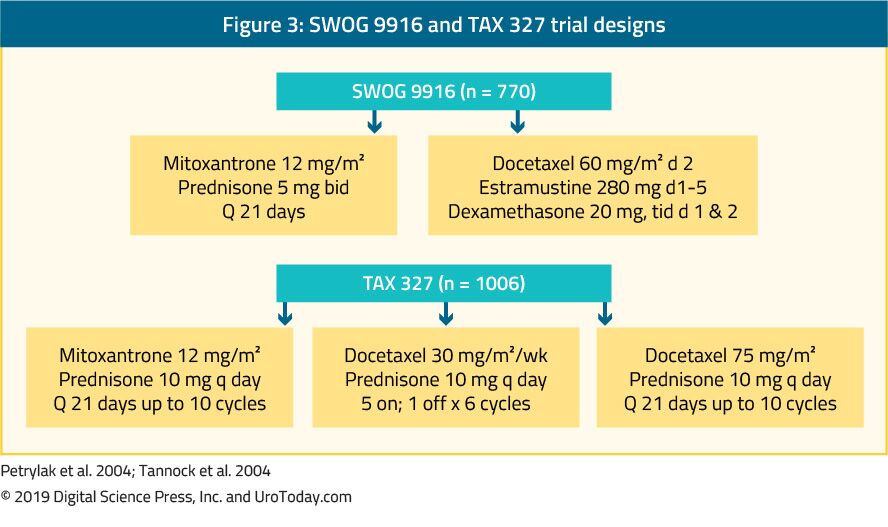
Rysunek 3. SWOG 9916 i tax 327 wzory badań
Sipuleucel-t
Sipuleucel-t, autologiczna aktywna immunoterapia komórkowa, wykazano w badaniu III fazy (IMPACT trial) w celu uzyskania korzyści w zakresie przeżycia u 512 bezobjawowych lub minimalnie objawowych pacjentów z mCRPC w porównaniu z placebo24 (rycina 4). Po medianie obserwacji wynoszącej 34 miesiące mediana przeżycia była istotnie większa w grupie otrzymującej sipuleucel-T (25,8 vs 21,7 miesiąca, z HR 0,78, p = 0,03).Co ważne, nie zaobserwowano zmniejszenia stężenia PSA w trakcie leczenia ani po jego zakończeniu, a PFS był podobny w obu ramionach. Ogólna tolerancja na sipuleucel-T była bardzo dobra, z występowaniem głównie zdarzeń niepożądanych stopnia 1-2. Obecnie zabieg ten jest dostępny tylko w USA i nie jest już dostępny w Europie.
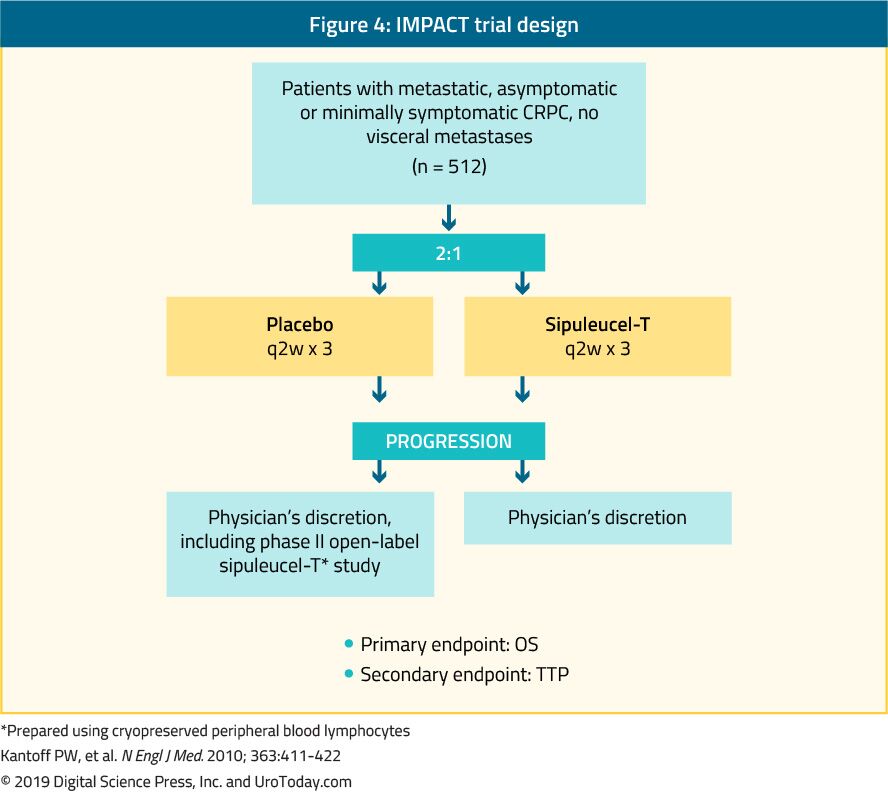
Rysunek 4. Projekt badania IMPACT trial
wnioski
w ciągu ostatnich 15 lat nastąpił znaczny postęp naukowy i inwestycje w rozwój leków dla pacjentów z mCRPC. Doprowadziło to do zatwierdzenia przez FDA kilku linii terapii systemowych ze względu na łagodzenie bólu, minimalizowanie niepożądanych skutków choroby i wydłużenie OS. Do tej pory zgłaszany wpływ na OS u pacjentów z mCRPC z każdego z tych pojedynczych leków jest nadal niewielki, co skutkuje dodaniem tylko kilku miesięcy. Konieczne jest lepsze zrozumienie biologii choroby mCRPC, zintegrowanie kompleksowego molekularnego zrozumienia oporności na kastrację i analiza mechanizmów oporności na obecne terapie w celu poprawy przyszłego rozwoju leczenia. Ważne jest również inwestowanie i opracowywanie biomarkerów prognostycznych, aby pomóc w personalizacji terapii. Wreszcie, w bardziej praktycznej uwadze, potrzebne są więcej danych na temat odpowiednich terapii drugiego i trzeciego rzutu oraz sekwencjonowania i kombinacji dostępnych leków, omówionych bardziej szczegółowo w następnym artykule przeglądowym („Beyond first line treatment of metastatic castrate-resistant prostate cancer”).
Data publikacji: 19/11/19
Leave a Reply