Chemia nieorganiczna
opisowa Chemia nieorganiczna skupia się na klasyfikacji związków na podstawie ich właściwości. Po części klasyfikacja koncentruje się na pozycji w układzie okresowym najcięższego pierwiastka (pierwiastka o najwyższej masie atomowej) w związku, po części grupując związki według ich podobieństw strukturalnych.
klasyfikacje chemii nieorganicznej:
związki Koordynacyjneedit
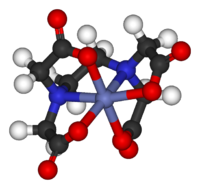
Klasyczne związki koordynacyjne zawierają metale związane z „samotnymi parami” elektronów przebywających na głównych atomach grupy ligandów, takich jak H2O, NH3, CL− i CN−. We współczesnych związkach koordynacyjnych prawie wszystkie związki organiczne i nieorganiczne mogą być stosowane jako ligandy. „Metal” zwykle jest metalem z grup 3-13, a także trans-lantanowcami i trans-aktynowcami, ale z pewnej perspektywy wszystkie związki chemiczne można opisać jako kompleksy koordynacyjne.
stereochemia kompleksów koordynacyjnych może być dość bogata, jak sugeruje rozdzielenie przez Wernera dwóch enancjomerów 6+, wczesny pokaz, że chiralność nie jest nieodłączna związkom organicznym. Tematem przewodnim tej specjalizacji jest chemia koordynacji supramolekularnej.
- przykłady:−, 3+, TiCl4 (THF)2.
główne składy grupoweedit

gatunki te posiadają pierwiastki z grup i, II, III, IV,V, VI, VII, 0 (z wyłączeniem wodoru) układu okresowego. Ze względu na ich często podobną reaktywność, pierwiastki z grupy 3 (Sc, Y i La) i grupy 12 (Zn, Cd i Hg) są również ogólnie włączone, a lantanowce i aktynowce są czasami włączone.
związki z grupy głównej znane są od początków chemii, np. Siarka elementarna i destylowany fosfor biały. Eksperymenty Lavoisiera i Priestleya na tlen, O2, nie tylko zidentyfikowały ważny Gaz dwuatomowy, ale otworzyły drogę do opisu związków i reakcji zgodnie ze współczynnikami stechiometrycznymi. Odkrycie praktycznej syntezy amoniaku przy użyciu katalizatorów żelazowych przez Carla Boscha i Fritza Habera na początku XX wieku głęboko wpłynęło na ludzkość, demonstrując znaczenie nieorganicznej syntezy chemicznej.Typowe związki z grupy głównej to SiO2, SnCl4 i N2O. Wiele związków z głównych grup można również zaklasyfikować jako” organometaliczne”, ponieważ zawierają one grupy organiczne, np. B(CH3)3). Związki z grupy głównej występują również w przyrodzie, np. fosforany w DNA, dlatego mogą być klasyfikowane jako bioorganiczne. Odwrotnie, związki organiczne pozbawione (wielu) ligandów wodorowych można klasyfikować jako” nieorganiczne”, takie jak fulereny, buckytubes i podwójne tlenki węgla.
- przykłady: tetrasulfur tetranitride S4N4, diboran B2H6, silikony, buckminsterfullerene C60.
związki metali Przejściowychedit
związki zawierające metale z grupy 4 do 11 są uważane za związki metali przejściowych. Związki z metalem z grupy 3 lub 12 są czasami również włączane do tej grupy, ale często klasyfikowane jako związki z grupy głównej.
związki metali przejściowych wykazują bogatą chemię koordynacyjną, różniącą się od czworościennego dla tytanu (np. TiCl4) do kwadratowego planarnego dla niektórych kompleksów niklu do ośmiościanowego dla kompleksów koordynacyjnych kobaltu. Szereg metali przejściowych można znaleźć w biologicznie ważnych związkach, takich jak żelazo w hemoglobinie.
- przykłady: pentakarbonyl żelaza, tetrachlorek tytanu, cisplatyna
związki Metaloorganiczneedit

zwykle uważa się, że związki metaloorganiczne zawierają grupę m-c-H. Metal (M) u tych gatunków może być głównym elementem grupy lub metalem przejściowym. Operacyjnie definicja związku metaloorganicznego jest bardziej swobodna, aby obejmować również wysoce lipofilowe kompleksy, takie jak karbonyle metali, a nawet alkoksydy metali.
związki metaloorganiczne są głównie uważane za specjalną kategorię, ponieważ ligandy organiczne są często wrażliwe na hydrolizę lub utlenianie, co wymaga, aby Chemia metaloorganiczna stosowała bardziej wyspecjalizowane metody preparatywne niż tradycyjne w kompleksach typu Wernera. Metodologia syntetyczna, zwłaszcza zdolność do manipulowania kompleksami w rozpuszczalnikach o niskiej mocy Koordynacyjnej, umożliwiła eksplorację bardzo słabo koordynujących ligandów, takich jak węglowodory, H2 i N2. Ponieważ ligandy są w pewnym sensie petrochemiczne, obszar chemii metaloorganicznej znacznie skorzystał z jego znaczenia dla przemysłu.
- przykłady: Cyclopentadienyliron dicarbonyl dimer (C5H5)Fe(CO)2CH3, ferrocene Fe(C5H5)2, molybdenum hexacarbonyl Mo(CO)6, triethylborane Et3B, Tris(dibenzylideneacetone)dipalladium(0) Pd2(dba)3)
Cluster compoundsEdit
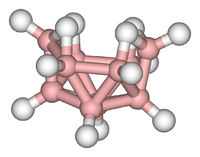

Clusters można znaleźć we wszystkich klasach związków chemicznych. Zgodnie z powszechnie przyjętą definicją klaster składa się w minimalnym stopniu z trójkątnego zestawu atomów, które są bezpośrednio związane ze sobą. Ale kompleksy dimetaliczne związane metal-metal są bardzo istotne dla tego obszaru. Klastry występują w „czystych” układach nieorganicznych, chemii metaloorganicznej, chemii grupy głównej i Chemii Bioorganicznej. Rozróżnienie między bardzo dużymi skupiskami a bryłami sypkimi jest coraz bardziej niewyraźne. Ten interfejs jest chemiczną podstawą nanonauki lub nanotechnologii i wynika w szczególności z badań nad skutkami wielkości kwantowych w klastrach selenku kadmu. Tak więc, duże skupiska mogą być opisane jako szereg wiązanych atomów pośrednich w charakterze między cząsteczką a ciałem stałym.
- przykłady: Fe3(CO)12, B10H14, 2−, 4Fe-4S
związki Bioorganiczneedit

z definicji związki te występują w przyrodzie, ale subfield obejmuje gatunki antropogeniczne, takie jak zanieczyszczenia (np. metylortęć) i leki (np. cisplatyna). Dziedzina, która obejmuje wiele aspektów biochemii, obejmuje wiele rodzajów związków, np. fosforany w DNA, a także kompleksy metali zawierające ligandy, które wahają się od biologicznych makrocząsteczek, powszechnie peptydów, do źle zdefiniowanych gatunków, takich jak kwas humusowy i woda (np. skoordynowane z kompleksami gadolinowymi stosowanymi do MRI). Tradycyjnie Chemia bioorganiczna koncentruje się na przenoszeniu elektronów i energii w białkach istotnych dla oddychania. Lecznicza Chemia nieorganiczna obejmuje badanie zarówno elementów nieistotnych, jak i istotnych z zastosowaniami do diagnostyki i terapii.
- przykłady: hemoglobina, metylortęć, karboksypeptydaza
związki półprzewodnikowe
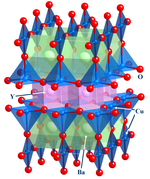
ten ważny obszar koncentruje się na strukturze, klejeniu i właściwościach fizycznych materiałów. W praktyce, ciało stałe Chemia nieorganiczna używa technik, takich jak krystalografia, aby uzyskać zrozumienie właściwości, które wynikają z kolektywnych oddziaływań między podjednostkami ciała stałego. Do chemii ciał stałych zalicza się Metale i ich stopy lub pochodne międzymetaliczne. Pokrewnymi dziedzinami są fizyka materii skondensowanej, Mineralogia i materiałoznawstwo.
- przykłady: chipy krzemowe, zeolity, YBa2Cu3O7
Leave a Reply